题目内容
16.下列有关物质的性质与用途对应关系错误的是( )| A. | SO2具有氧化性,可用于漂白纸浆 | |
| B. | NaHCO3受热易分解,可通过加热方法除去碳酸钠中的碳酸氢钠杂质 | |
| C. | Na2O2能与水或二氧化碳反应产生氧气,可用作宇航员的供氧剂 | |
| D. | Al2O3熔点高,可用作耐高温材料 |
分析 A.二氧化硫具有漂白性,用于漂白纸浆;
B.碳酸氢钠加热分解生成碳酸钠;
C.Na2O2能与水或二氧化碳反应产生氧气,且固体运输方便;
D.熔点高的物质可作耐高温材料.
解答 解:A.二氧化硫具有漂白性,用于漂白纸浆,与其氧化性无关,故A错误;
B.碳酸氢钠加热分解生成碳酸钠,则通过加热方法除去碳酸钠中的碳酸氢钠杂质,故B正确;
C.Na2O2能与水或二氧化碳反应产生氧气,且固体运输方便,则可用作宇航员的供氧剂,故C正确;
D.熔点高的物质可作耐高温材料,则Al2O3熔点高,可用作耐高温材料,故D正确;
故选A.
点评 本题考查物质的性质及应用,为高频考点,把握物质的性质、发生的反应、性质与用途等为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的应用,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
6.常温下,对于醋酸溶液的下列说法中,正确的是( )
| A. | 0.1 mol•L-1的醋酸溶液中加水稀释,溶液中c(OH-)减小 | |
| B. | 醋酸溶液中离子浓度的关系满足:c(H+)=c(OH-)+c(CH3COO-) | |
| C. | 与同浓度的盐酸比较,分别加水稀释100倍,稀释后溶液中c(H+)醋酸>c(H+)盐酸 | |
| D. | 0.1 mol•L-1的醋酸与等浓度等体积的NaOH溶液反应后的溶液中:c(CH3COO-)+c(CH3COOH)=0.1mol/L |
7.下列各组物质的晶体中,化学键类型相同、晶体类型也相同的是( )
| A. | SO2和SiO2 | B. | CO2和HClO | C. | NaCl和HCl | D. | CCl4和KCl |
4.从海带中提取碘要经过灼烧、浸取、过滤、氧化、萃取、分液、蒸馏等操作,下列对应的装置合理,操作规范的是( )
| A. | 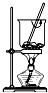 海带灼烧成灰 | B. | 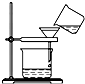 过滤含I-溶液 | C. | 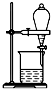 放出碘的苯溶液 | D. | 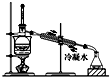 分离碘并回收苯 |
8.甲醇燃料电池的总反应为:2CH3OH+3O2═2CO2↑+4H2O,如图是该电池的示意图.下列说法正确的是( )

| A. | a 是氧气,b 是甲醇 | |
| B. | 质子从 N 电极区穿过质子交换膜移向 M 电极区 | |
| C. | 正极反应为:O2+2H2O+4e-═4OH- | |
| D. | 当电路中有 3mole-转移时,电池中n(H+)变化为 0 |
5.下列说法中正确的是( )
| A. | NO2、SO2、BF3分子中所有原子的最外层电子都满足了8e-稳定结构 | |
| B. | NaCl晶体中与每个Na+距离相等且最近的Na+共有12个 | |
| C. | 在同一能级上运动的电子,其运动状态可能相同 | |
| D. | 若ABn的中心原子A上没有未用于形成共价键的孤对电子,当n=3,则分子结构为三角锥形 |
20.下面关于硅的叙述中,正确的是( )
| A. | 硅的化学性质稳定,常温下不与任何物质反应 | |
| B. | 硅是构成矿物和岩石的主要元素,硅元素在地壳中的含量居第一位 | |
| C. | 硅在自然界中可以以游离态存在 | |
| D. | 高纯度的单质硅被广泛用于制作计算机芯片 |
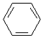 、④HCHO.其中碳原子采取sp2杂化的分子有①③④(填物质序号),HCHO分子的立体结构为平面三角,它加成产物的熔、沸点比CH4的熔、沸点高,其主要原因是加成产物CH3OH分子之间能形成氢键.
、④HCHO.其中碳原子采取sp2杂化的分子有①③④(填物质序号),HCHO分子的立体结构为平面三角,它加成产物的熔、沸点比CH4的熔、沸点高,其主要原因是加成产物CH3OH分子之间能形成氢键.