题目内容
19.铁铝矾[Al2Fe(SO4)4•xH2O]有净水作用,将其溶于水中得到浅绿色溶液,有关该溶液的叙述正确的是( )| A. | 该溶液显中性 | |
| B. | 该溶液中:2 c(Al3+)+c(Fe2+)+c(H+ )=4 c(SO42-)+c(OH-) | |
| C. | 在空气中蒸干并灼烧该溶液,最后所得的残留固体为Al2O3、Fe2O3 | |
| D. | 向该溶液中加入Ba(OH)2溶液,当SO42-完全沉淀时,Al3+、Fe2+恰好被完全沉淀 |
分析 铁铝矾[Al2Fe(SO4)4•xH2O]有净水作用,将其溶于水中得到浅绿色溶液,可知溶液中含Al3+、Fe2+,Al3+水解生成胶体可净化水,结合溶液为电中性及离子反应来解答.
解答 解:A.Al3+、Fe2+水解使溶液显酸性,故A错误;
B.由电荷守恒可知,该溶液中:3c(Al3+)+2c(Fe2+)+c(H+ )=2c(SO42-)+c(OH-),故B错误;
C.水解生成的硫酸不挥发,则在空气中蒸干并灼烧该溶液,最后所得的残留固体为Al2Fe(SO4)4,故C错误;
D.向该溶液中加入Ba(OH)2溶液,当SO42-完全沉淀时,铁铝矾与Ba(OH)2物质的量比为1:4,Al3+、Fe2+恰好被完全沉淀,故D正确;
故选D.
点评 本题考查盐类水解及应用,为高频考点,把握盐中的阳离子、电荷守恒、水解规律为解答的关键,侧重分析与应用能力的考查,注意离子反应中物质的量关系,题目难度不大.

练习册系列答案
相关题目
9.下列离子方程式错误的是( )
| A. | 氧化铁与稀硫酸反应:Fe2O3+6H+═2Fe3++3H2O | |
| B. | 小苏打溶液中加入过量石灰水:2HCO3-+Ca2++2OH-═CaCO3↓+CO32-+2H2O | |
| C. | 硫酸与氯化钡反应:SO42-+Ba2+═BaSO4↓ | |
| D. | 氯化铝溶液中加入过量氨水:Al3++3NH3•H2O═Al(OH)3↓+3NH4+ |
10.下列溶液中微粒浓度关系一定正确的是( )
| A. | pH=4的盐酸与pH=10的氨水溶液等体积混合后pH>7 | |
| B. | 氯水中:c(Cl2)=2[c(ClO-)+c(Cl-)+c(HClO)] | |
| C. | pH=11的NaOH和pH=11的氨水分别稀释100倍后的pH前者一定大于后者 | |
| D. | 0.10 mol•L-1 Na2CO3溶液:c(Na+)+c(H+)=c(OH-)+c(HCO3-)+c(CO32-) |
7.如图所示,在101kPa时,△H1=-393.5kJ•mol-1,△H2=-395.4kJ•mol-1,下列说法正确的是( )
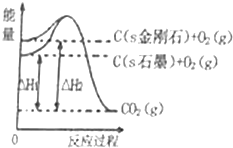

| A. | 石墨的燃烧热为393.5kJ/mol | |
| B. | 石墨转变成金刚石需要吸收能量,是物理变化 | |
| C. | 石墨比金刚石稳定 | |
| D. | 1mol金刚石与1molO2的总能量低于1molCO2的总能量 |
14.南海争端、南海仲裁案一直牵动国人的心,南海是一个巨大的资源宝库,海水开发利用的部分过程如下图所示.下列有关说法正确的是( )
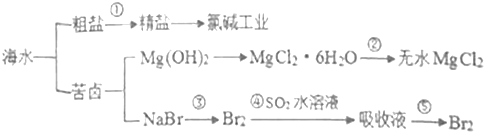

| A. | 第①步中除去粗盐中的SO42-、Ca2+、Mg2+等杂质,加入药品的顺序为:Na2CO3溶液、NaOH溶液、BaCl2溶液、过滤后加盐酸 | |
| B. | 第②步的关键要低温小火烘干 | |
| C. | 氯碱工业的阴极产物是Cl2 | |
| D. | 第③步到第⑤步的目的是为了富集溴元素 |
11.下列物质的水溶液因水解而呈碱性的是( )
| A. | NaOH | B. | (NH4)2SO4 | C. | Na2O | D. | CH3COONa |
8.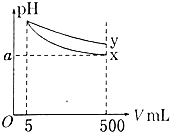 pH=11的x、y两种碱溶液各5ml,分别稀释至500ml,其pH与溶液体积(V)的关系如图所示,下列说法正确的是( )
pH=11的x、y两种碱溶液各5ml,分别稀释至500ml,其pH与溶液体积(V)的关系如图所示,下列说法正确的是( )
 pH=11的x、y两种碱溶液各5ml,分别稀释至500ml,其pH与溶液体积(V)的关系如图所示,下列说法正确的是( )
pH=11的x、y两种碱溶液各5ml,分别稀释至500ml,其pH与溶液体积(V)的关系如图所示,下列说法正确的是( )| A. | x是强碱,y是弱碱 | |
| B. | 若x、y是一元碱,则等物质的量浓度的x的硝酸盐溶液的pH比y的硝酸盐溶液大 | |
| C. | 若x、y是一元碱,室温下pH=11的x、y两种碱溶液的浓度相同 | |
| D. | 完全中和x、y两溶液时,消耗同浓度稀硫酸的体积V(x)>V(y) |
11.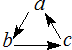 下列各组物质中,物质之间通过一步反应,能实现如图所示转化的是( )
下列各组物质中,物质之间通过一步反应,能实现如图所示转化的是( )
 下列各组物质中,物质之间通过一步反应,能实现如图所示转化的是( )
下列各组物质中,物质之间通过一步反应,能实现如图所示转化的是( )| a | b | c | |
| A | Cl2 | HClO | HCl |
| B | Si | SiO2 | H2SiO3 |
| C | Cu | CuSO4 | Cu(OH)2 |
| D | Na | NaOH | NaHCO3 |
| A. | A | B. | B | C. | C | D. | D |
 .
.