题目内容
下列说法中不正确的是( )
| A、NaOH溶液和AlCl3溶液相互滴加的现象不同 |
| B、向淀粉碘化钾溶液中加溴水,溶液变为蓝色,说明Br2的氧化性强于I2 |
| C、氧化铁和氧化亚铁都是碱性氧化物,和硝酸反应都只生成盐和水 |
| D、NH4Cl和HCl溶于水后滴加石蕊都变红色,说明溶液中c(H+)>c(OH-) |
考点:镁、铝的重要化合物,盐类水解的应用,氯、溴、碘及其化合物的综合应用
专题:
分析:A.前者逐滴滴入后者,发生AlCl3+4NaOH═3NaCl+NaAlO2+H2O、3NaAlO2+AlCl3+6H2O═4Al(OH)3↓+3NaCl,后者逐滴滴入前者发生Al3++3OH-═Al(OH)3↓、Al(OH)3+OH-═AlO2-+2H2O;
B.卤素单质的氧化性顺序是:Br2>I2,离子的还原性顺序是:I->Br-,Br2强氧化性比碘强,可与KI发生氧化还原反应生成I2;碘遇淀粉显蓝色;
C.氧化亚铁和硝酸之间的反应产物是硝酸铁和一氧化氮、水;
D.NH4Cl和HCl溶于水后滴加石蕊都变红色,说明溶液都成酸性;
B.卤素单质的氧化性顺序是:Br2>I2,离子的还原性顺序是:I->Br-,Br2强氧化性比碘强,可与KI发生氧化还原反应生成I2;碘遇淀粉显蓝色;
C.氧化亚铁和硝酸之间的反应产物是硝酸铁和一氧化氮、水;
D.NH4Cl和HCl溶于水后滴加石蕊都变红色,说明溶液都成酸性;
解答:
解:A.因前者逐滴滴入后者,发生AlCl3+4NaOH═3NaCl+NaAlO2+H2O、3NaAlO2+AlCl3+6H2O═4Al(OH)3↓+3NaCl,现象为先没有沉淀后有沉淀生成;
而后者逐滴滴入前者发生Al3++3OH-═Al(OH)3↓、Al(OH)3+OH-═AlO2-+2H2O,现象为先有沉淀生成后沉淀逐渐消失,则现象不同,故A正确;
B.碘遇淀粉显蓝色,说明有碘单质生成,这是因为溴强氧化性比碘强,可与KI发生氧化还原反应生成I2,反应的离子方程式为Br2+2I-=2Br-+I2,故B正确;
C.氧化铁和氧化亚铁都是碱性氧化物,但是氧化亚铁和硝酸之间的反应产物是硝酸铁和一氧化氮、水,故C错误.
D.NH4Cl和HCl溶于水后滴加石蕊都变红色,说明溶液都成酸性,所以溶液中c(H+)>c(OH-),故D正确;
故选C.
而后者逐滴滴入前者发生Al3++3OH-═Al(OH)3↓、Al(OH)3+OH-═AlO2-+2H2O,现象为先有沉淀生成后沉淀逐渐消失,则现象不同,故A正确;
B.碘遇淀粉显蓝色,说明有碘单质生成,这是因为溴强氧化性比碘强,可与KI发生氧化还原反应生成I2,反应的离子方程式为Br2+2I-=2Br-+I2,故B正确;
C.氧化铁和氧化亚铁都是碱性氧化物,但是氧化亚铁和硝酸之间的反应产物是硝酸铁和一氧化氮、水,故C错误.
D.NH4Cl和HCl溶于水后滴加石蕊都变红色,说明溶液都成酸性,所以溶液中c(H+)>c(OH-),故D正确;
故选C.
点评:本题考查了铝盐的性质、二价铁的强还原性、盐类的水解、碘遇淀粉显蓝色等知识点,掌握基础知识是解题关键,题目难度不大.

练习册系列答案
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案
相关题目
配制一定物质的量浓度溶液时,下列操作会使配得溶液物质的量浓度偏高的是( )
| A、没有洗涤烧杯和玻璃棒 |
| B、定容时凹液面最低点低于刻度线 |
| C、容量瓶用蒸馏水洗涤干净后没有进行干燥就移入所配制溶液 |
| D、转移过程中有少量溶液溅出 |
在一定温度下,在一个密闭容器中加入H2和I2蒸气各0.5mol,发生反应H2+I2?2HI,达到平衡时,生成HI 0.8mol,若其它条件不变,开始充入的H2为2mol,则达到平衡时生成的HI可能是下列中的( )
| A、1.1 mol |
| B、0.87 mol |
| C、0.8 mol |
| D、0.5 mol |
根据陈述的知识,类推得出的结论正确的是( )
| A、镁条在空气中燃烧生成的氧化物是MgO,则钠在空气中燃烧生成的氧化物是Na2O |
| B、已知ⅣA沸点CH4<SiH4<GeH4,则ⅤA族沸点 NH3<PH3<AsH3 |
| C、已知Fe与S直接化合生成FeS,则Cu与S直接化合生成Cu2S |
| D、已知Ca(HCO3)2+2NaOH(过量)=CaCO3↓+Na2CO3+2H2O,则Mg(HCO3)2+2NaOH(过量)=MgCO3↓+Na2CO3+2H2O |
室温时,下列说法中,正确的是( )
| A、0.l mol/L醋酸钙溶液中,c(Ca2+)>c(CH3COO-)>c(OH-)>c(H+) |
| B、体积和pH都相同的NH4Cl溶液、盐酸,完全溶解少量且等质量的锌粉,前者所用时间少 |
| C、将n mol H2(g)、n mol I2(g)和2n mol H2 (g)、2n mol I2(g)分别充入两个恒温恒容的容器中,平衡时H2的转化率前者小于后者 |
| D、某物质的溶液中由水电离出的c(H+)=1×10-a mol?L-1,若a>7时,则该溶液的pH一定为14-a |
下列说法正确的是( )
| A、从海水提取物质都必须通过化学反应才能实现 |
| B、“地沟油”经过加工处理后,可以用来制肥皂和生物柴油 |
| C、“绿色化学”的核心是利用化学原理进行环境治理 |
| D、生石灰、铁粉、硅胶是食品包装中常用的干燥剂 |
下列物质的水溶液能够导电,但属于非电解质的是( )
| A、四氯化碳 | B、二氧化硫 |
| C、氯化氢 | D、氯气 |
低温脱硝技术可用于处理废气中的氮氧化物,发生的化学反应为:2NH3(g)+NO(g)+NO2(g)
2N2(g)+3H2O(g)△H<0,在恒容的密闭容器中,下列有关说法正确的是( )
| 130℃ |
| 催化剂 |
| A、平衡时,其他条件不变,升高温度可使该反应的平衡常数增大 |
| B、平衡时,其他条件不变,增加NH3的浓度,废气中氮氧化物的转化率减小 |
| C、单位时间内消耗NO和N2的物质的量比为1:2时,反应达到平衡 |
| D、其他条件不变,使用高效催化剂,废气中氮氧化物的转化率增大 |
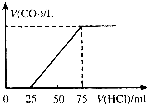 有10mL NaOH溶液,向其中通入一定量的CO2,得到了Na2CO3和NaHCO3的混合溶液.向所得溶液中逐滴加入0.1mol/L的盐酸,边加边振荡,使其充分反应,产生CO2气体的体积(标准状况)与所加盐酸体积之间的关系如图所示.
有10mL NaOH溶液,向其中通入一定量的CO2,得到了Na2CO3和NaHCO3的混合溶液.向所得溶液中逐滴加入0.1mol/L的盐酸,边加边振荡,使其充分反应,产生CO2气体的体积(标准状况)与所加盐酸体积之间的关系如图所示.