题目内容
9.纯锌和稀硫酸反应速率很小,为了加快锌的溶解和放出H2的速率,可以加入少量( )| A. | 硫酸铜晶体 | B. | 稀盐酸 | C. | 镁带 | D. | 碘化钾溶液 |
分析 增大氢离子的浓度、构成原电池且Zn作负极时,加快锌的溶解和放出H2的速率,以此来解答.
解答 解:A,加硫酸铜,构成Cu、Zn原电池,加快锌的溶解和放出H2的速率,故A选;
B.加少量稀盐酸,氢离子浓度变化不大,速率变化不明显,故B不选;
C.Mg比Zn活泼,不能加快锌的溶解,故C不选;
D.加入KI溶液,不参加反应,故D不选;
故选A.
点评 本题考查反应速率的影响因素,为高频考点,把握物质的性质、原电池对反应速率的影响为解答的关键,侧重分析与应用能力的考查,题目难度不大,选项C为易错点.

练习册系列答案
相关题目
4.CPMA是蜂胶的活性成分,其结构简式如图所示,下列有关CPMA的叙述正确的是( )

| A. | CPMA的分子式为C17H18O4 | |
| B. | 1 mol CPMA中含有7 mol双键 | |
| C. | 1 mol CPMA最多可与2molNaOH反应 | |
| D. | CPMA能使酸性高锰酸钾溶液、溴水褪色 |
17.在强酸性溶液中能大量共存的无色透明离子组是( )
| A. | Mg2+、Na+、Cl-、SO42- | B. | K+、Na+、NO3-、MnO4- | ||
| C. | K+、Na十、Cl-、Cu2+ | D. | Na十、Ba2+、OH-、SO42- |
4.下列有关晶体的叙述中,不正确的是( )
| A. | 氯化钠和氯化铯晶体中,阳离子的配位数均为6 | |
| B. | 金刚石为三维网状结构,由碳原子以sp3杂化轨道形成共价键 | |
| C. | 金属钠的晶体采用体心立方堆积,每个晶胞含2个原子,配位数为8 | |
| D. | 干冰晶体中,每个CO2分子周围紧邻12个CO2分子 |
14.已知:Ni+CuSO4→NiSO4+Cu;Cu+2AgNO3→Cu(NO3)2+2Ag,则下列判断正确的是( )
| A. | 还原性:Ni>Cu | B. | 氧化性:Cu2+>Ag+ | C. | 还原性:Ag>Cu | D. | 氧化性:Ni2+>Ag+ |
1.下列说法正确的是( )
| A. | 破坏生成物全部化学键所需要的能量大于破坏反应物全部化学键所需要的能量,该反应为吸热反应 | |
| B. | 任何酸与碱发生中和反应生成1 mol H2O的过程中,能量变化均相同 | |
| C. | 已知:①2H2(g)+O2(g)=2H2O(g)△H1,②2H2(g)+O2 (g)=2H2O(1)△H2,则△H1<△H2 | |
| D. | 已知:①C(s,石墨)+O2 (g)=CO2(g)△H=-393.5kJ•mol-1, ②C(s,金刚石)+O2(g)=CO2 (g)△H=-395.0 kJ•mol-1则C(s,石墨)=C(s,金刚石)△H=+1.5 kJ•mol-1 |
18.心理学研究发现一个人心理平衡才能把化学平衡的题做好.已知COCl2(g)?CO(g)+Cl2(g)△H>0,当反应达到平衡时,下列措施:
①升温
②恒容通入惰性气体
③增加CO的浓度
④扩大容积
⑤加催化剂
⑥恒压通入惰性气体,
能提高COCl2转化率的是( )
①升温
②恒容通入惰性气体
③增加CO的浓度
④扩大容积
⑤加催化剂
⑥恒压通入惰性气体,
能提高COCl2转化率的是( )
| A. | ①②④ | B. | ①④⑥ | C. | ②③⑥ | D. | ③⑤⑥ |
19.由A、B、C、D四种金属按表中装置进行实验.
根据实验现象回答下列问题:
(1)装置甲中负极的电极反应式是A-2e-═A2+.
(2)装置乙中正极的电极反应式是Cu2++2e-═Cu.
(3)装置丙中溶液的pH变大(填“变大”、“变小”或“不变”).
| 装置 | 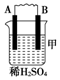 |  |  |
| 现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
(1)装置甲中负极的电极反应式是A-2e-═A2+.
(2)装置乙中正极的电极反应式是Cu2++2e-═Cu.
(3)装置丙中溶液的pH变大(填“变大”、“变小”或“不变”).