题目内容
相同物质的量的CO2和O2,其所含原子数目之比为________,所含氧原子数目之比为________,相同条件下的密度之比为________;质量相同的CO2和O2,其物质的量之比为________.
3:2 1:1 11:8 8:11
分析:根据物质的构成,利用物质的量与原子个数计算原子个数之比;因相同条件下,物质的量之比等于体积之比,则密度之比等于质量之比;利用n= 来计算物质的量及比值.
来计算物质的量及比值.
解答:设二者的物质的量都是1mol,
则的CO2和O2中所含原子数目之比为1mol×3:1mol×2=3:2,
所含氧原子数目之比为1mol×2:1mol×2=1:1,
又相同条件下,物质的量之比等于体积之比,则密度之比等于质量之比,
则CO2和O2的密度之比为1mol×44g/mol:1mol×32g/mol=11:8,
质量相同的CO2和O2,设质量都是mg,其物质的量之比为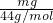 :
: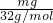 =8:11,
=8:11,
故答案为:3:2;1:1;11:8;8:11.
点评:本题考查物质的量的计算,较简单,注重了对基础知识的考查,明确质量、物质的量的关系及物质的构成是解答的关键.
分析:根据物质的构成,利用物质的量与原子个数计算原子个数之比;因相同条件下,物质的量之比等于体积之比,则密度之比等于质量之比;利用n=
 来计算物质的量及比值.
来计算物质的量及比值.解答:设二者的物质的量都是1mol,
则的CO2和O2中所含原子数目之比为1mol×3:1mol×2=3:2,
所含氧原子数目之比为1mol×2:1mol×2=1:1,
又相同条件下,物质的量之比等于体积之比,则密度之比等于质量之比,
则CO2和O2的密度之比为1mol×44g/mol:1mol×32g/mol=11:8,
质量相同的CO2和O2,设质量都是mg,其物质的量之比为
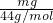 :
: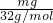 =8:11,
=8:11,故答案为:3:2;1:1;11:8;8:11.
点评:本题考查物质的量的计算,较简单,注重了对基础知识的考查,明确质量、物质的量的关系及物质的构成是解答的关键.

练习册系列答案
 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案
相关题目