题目内容
5.为了提纯下表所列物质(括号内为杂质),有关除杂试剂和分离方法的选择均正确的是( )| 选项 | 被提纯的物质 | 除杂试剂 | 分离方法 |
| A | 己烷(己烯) | 溴水 | 分液 |
| B | 淀粉溶液(NaCl) | 水 | 过滤 |
| C | CH3CH2OH (CH3COOH) | CaO | 蒸馏 |
| D | CH3COOC2H5 (CH3COOH) | NaOH溶液 | 分液 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.己烷与二溴己烷混溶;
B.淀粉可透过滤纸;
C.乙酸与CaO发生反应;
D.二者都与氢氧化钠溶液反应.
解答 解:A.己烷与二溴己烷混溶,不能得到纯净物,故A错误;
B.淀粉可透过滤纸,应用半透膜,用渗析的方法除杂,故B错误;
C.乙酸与CaO发生反应,生成盐和水,可用蒸馏的方法分离,故C正确;
D.二者都与氢氧化钠溶液反应,应用饱和碳酸钠溶液除杂,故D错误.
故选C.
点评 本题考查混合物分离、提纯方法的选择和应用,为高频考点,把握物质的性质及分离、提纯方法为解答的关键,侧重除杂的考查,注意除杂的原则,题目难度不大.

练习册系列答案
相关题目
2.化学是以实验为基础的科学,下列有关实验现象描述不正确的是( )
| A. | 钠块在氯气中燃烧,产生白烟 | |
| B. | 将氯水滴入紫色石蕊试液中,试液先变红后褪色 | |
| C. | 用pH试纸测得0.1mol•L-1硫酸铝溶液显中性 | |
| D. | 向新切土豆上滴加碘水,土豆片上显示蓝色 |
13.三氯化氧磷(POCl3)是一种重要的化工原料,常用作半导体掺杂剂,实验室制取POCl3并测定产品含量的实验过程如下:
I.制备POCl3
采用氧气氧化液态的PCl3法,实验装置(加热及夹持装置省略)及相关信息如下:
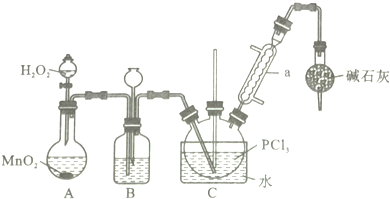
(1)仪器a的名称为冷凝管;
(2)装置C中生成POCl3的化学方程式为PCl3+H2O2=POCl3+H2O;
(3)实验中需控制通入O2的速率,对此采取的操作是控制分液漏斗中双氧水的加入量;
(4)装置B的作用除观察O2的流速之外,还有平衡气压、干燥氧气;
(5)反应温度应控制在60~65℃,原因是温度过低,反应速率小,温度过高,三氯化磷会挥发,影响产物纯度;
II.测定POCl3产品含量的实验步骤:
①实验I结束后,待三颈烧瓶中液体冷却到室温,准确称取16.725g POCl3产品,置于盛有60.00mL蒸馏水的水解瓶中摇动至完全水解,将水解液配成100.00mL溶液
②取10.00mL溶液于锥形瓶中,加入10.00mL 3.5mol/L AgNO3标准溶液(Ag++Cl-=AgCl↓)
③加入少量硝基苯(硝基苯密度比水大,且难溶于水)
④以硫酸铁溶液为指示剂,用0.2mol/L KSCN溶液滴定过量的AgNO3溶液(Ag++SCN-=AgSCN↓),到达终点时共用去10.00mL KSCN溶液.
(6)达到终点时的现象是溶液变红色;
(7)测得产品中n(POCl3)=0.11mol;
(8)已知Ksp(AgCl)>Ksp(AgSCN),据此判断,若取消步骤③,测定结果将偏低.(填偏高,偏低,或不变)
I.制备POCl3
采用氧气氧化液态的PCl3法,实验装置(加热及夹持装置省略)及相关信息如下:

| 物质 | 熔点/℃ | 沸点/℃ | 相对分子质量 | 其他 |
| PCl3 | -112.0 | 76.0 | 137.5 | 均为无色液体,遇水均剧烈水解为含氧酸和氯化氢,两者互溶 |
| POCl3 | 2.0 | 106.0 | 153.5 |
(2)装置C中生成POCl3的化学方程式为PCl3+H2O2=POCl3+H2O;
(3)实验中需控制通入O2的速率,对此采取的操作是控制分液漏斗中双氧水的加入量;
(4)装置B的作用除观察O2的流速之外,还有平衡气压、干燥氧气;
(5)反应温度应控制在60~65℃,原因是温度过低,反应速率小,温度过高,三氯化磷会挥发,影响产物纯度;
II.测定POCl3产品含量的实验步骤:
①实验I结束后,待三颈烧瓶中液体冷却到室温,准确称取16.725g POCl3产品,置于盛有60.00mL蒸馏水的水解瓶中摇动至完全水解,将水解液配成100.00mL溶液
②取10.00mL溶液于锥形瓶中,加入10.00mL 3.5mol/L AgNO3标准溶液(Ag++Cl-=AgCl↓)
③加入少量硝基苯(硝基苯密度比水大,且难溶于水)
④以硫酸铁溶液为指示剂,用0.2mol/L KSCN溶液滴定过量的AgNO3溶液(Ag++SCN-=AgSCN↓),到达终点时共用去10.00mL KSCN溶液.
(6)达到终点时的现象是溶液变红色;
(7)测得产品中n(POCl3)=0.11mol;
(8)已知Ksp(AgCl)>Ksp(AgSCN),据此判断,若取消步骤③,测定结果将偏低.(填偏高,偏低,或不变)
20.某同学用回收的镁铝合金制取氢气.现有10.8g镁铝合金,下列说法正确的是( )
| A. | 常温下与足量18mol/LH2SO4反应,最多可放出0.6molH2 | |
| B. | 常温下与足量2mol/LHNO3反应,最少可放出0.45molH2 | |
| C. | 常温下与足量2mol/LH2SO4反应,放出H2的量在0.45mol~0.6mol之间 | |
| D. | 常温下与足量2mol/LNaOH反应,放出H2的量在0.45mol~0.6mol之间 |
10.实现下列变化需加入氧化剂的是( )
| A. | I-→I2 | B. | MnO4-→Mn2+ | C. | S2-→HS- | D. | ClO3-→Cl2 |
17.在短周期元素中,属于金属元素的有( )
| A. | 13种 | B. | 9种 | C. | 5种 | D. | 3种 |