题目内容
相同质量的SO2和SO3,所含分子的数目之比为 ,所含原子数目之比为 ,所含氧原子物质的量之比为 .
考点:物质的量的相关计算
专题:计算题
分析:根据n=
可知,质量相等的SO2和SO3的物质的量之比与摩尔质量成反比,分子数目之比等于物质的量之比,结合分子含有原子总数、O原子数目解答.
| m |
| M |
解答:
解:根据n=
可知,质量相等的SO2和SO3的物质的量之比=80g/mol:64g/mol=5:4,故二者含有分子数目之比为5:4,二者原子数目之比=5×3:4×4=15:16,二者含有O原子数目之比=5×2:4×3=5:6,
故答案为:5:4;15:16;5:6.
| m |
| M |
故答案为:5:4;15:16;5:6.
点评:本题考查物质的量有关计算,比较基础,注意对公式的理解与灵活应用.

练习册系列答案
相关题目
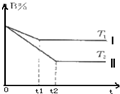 对于反应mA(g)+nB(g)?pC(g)+qD(g),当其他条件不变,温度分别为T1和T2时,反应物B的质量分数与反应时间(t)的关系分别可用图中曲线I和曲线Ⅱ表示.据此下列判断中,正确的是( )
对于反应mA(g)+nB(g)?pC(g)+qD(g),当其他条件不变,温度分别为T1和T2时,反应物B的质量分数与反应时间(t)的关系分别可用图中曲线I和曲线Ⅱ表示.据此下列判断中,正确的是( )| A、T1>T2 |
| B、T2>Tl |
| C、正反应是吸热反应 |
| D、Tl温度下转化率更高 |
设NA为阿伏加德罗常数,下列叙述正确的是( )
| A、7.1g氯气与足量的氢氧化钠溶液反应转移的电子数约为0.2×6.02×1023 |
| B、1 mol-CH3所含质子数为9NA |
| C、1L 0.1mol?L-1乙酸溶液中H+数为0.1NA |
| D、标准状况下,22.4L SO3中的分子数为NA |