题目内容
(6.02×1022个Na+ 的物质的量为: .
考点:物质的量的相关计算
专题:计算题
分析:根据n=
计算.
| N |
| NA |
解答:
解:n=
=
=0.1mol,故答案为:0.1mol.
| N |
| NA |
| 6.02×1022 |
| 6.02×1023mol-1 |
点评:本题考查了根据微粒数目计算物质的物质的量的计算公式,难度不大,注意基础知识的积累.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
如图装置中,通电后观察到Cu极溶解.下列说法中错误的是( )
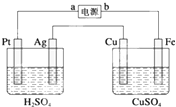

| A、a极是直流电源的正极 | ||
| B、Fe极是阳极 | ||
C、Pt极产生的气体体积是Ag极产生气体体积为
| ||
| D、硫酸铜溶液的浓度不变 |
解释下列物质性质的变化规律与物质结构间的因果关系时,与化学键强弱无关的变化规律是( )
| A、HF、HCI、HBr、HI的热稳定性依次减弱 |
| B、NaF、NaCl、NaBr、NaI的熔点依次降低 |
| C、F2、C12、Br2、I2的熔、沸点逐渐升高 |
| D、Li、Na、K、Rb 的熔点逐渐降低 |
下列说法中正确的是( )
| A、摩尔是国际单位制中把宏观物质的质量与微观粒子的数目联系起来的一个物理量 |
| B、摩尔是物质的量的单位,简称摩,符号为mol |
| C、摩尔质量就是该物质的相对分子质量或相对原子质量 |
| D、阿伏加德罗常数为6.02×1023 |
下列有关化学用语表示正确的是( )
| A、乙烯的结构简式:C2H4 | ||
B、中子数为146、质子数为92的铀(U)原子
| ||
C、氯原子的结构示意图: | ||
D、氢氧根离子的电子式: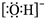 |
常温下,下列溶液中可能大量共存的离子组是( )
| A、加入金属镁能产生H2的溶液中:Na+、Fe2+、SO42-、NO3- |
| B、含有大量Fe2+的溶液中:K+、Mg2+、ClO-、SO42- |
| C、能使Al3+生成沉淀的溶液中:NH4+、Na+、SiO32-、HCO3- |
| D、水电离产生的c(OH-)=1×10-10mol/L的溶液中:Al3+、SO42-、NO3-、Cl- |