题目内容
16. 写出下列反应的热化学方程式
写出下列反应的热化学方程式(1)N2(g)与H2(g)反应生成1mol NH3(g),放出46.1KJ热量.
(2)0.5mol CH4完全燃烧生成CO2(g)和H2O(l)时,放出445kJ的热量.
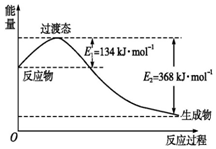
(3)如图所示是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:
(4)合金贮氢材料具有优异的吸收氢性能,贮氢合金可催化由CO、H2合成CH4的反应,温度为T时,该反应的热化学方程式为CO(g)+3H2(g)=CH4(g)+H2O(g)△H=-206kJ•mol-1.
已知温度为T时:
CH4(g)+2H2O═CO2(g)+4H2(g)△H=+165KJ•mol
CO(g)+H2O(g)═CO2(g)+H2(g)△H=-41KJ•mol.
分析 (1)根据N2(g)与H2(g)反应生成1mol NH3(g),放出46.1KJ热量,则1molN2(g)与3molH2(g)反应生成2mol NH3(g),放出46.1×2KJ热量,据此书写;
(2)根据0.5mol CH4完全燃烧生成CO2(g)和H2O(l)时,放出445kJ的热量,则1mol CH4完全燃烧生成CO2(g)和H2O(l)时,放出890kJ的热量,据此书写;
(3)由图可知,1mol NO2和1mol CO反应生成CO2和NO放出热量368-134=234kJ,根据热化学方程式书写原则进行书写;
(4)已知:①CH4(g)+2H2O(g)═CO2(g)+4H2(g)△H=+165kJ•mol-1
②CO(g)+H2O(g)═CO2(g)+H2(g)△H=-41kJ•mol-1,
根据盖斯定律,②-①可得.
解答 解:(1)因为N2(g)与H2(g)反应生成1mol NH3(g),放出46.1KJ热量,则1molN2(g)与3molH2(g)反应生成2mol NH3(g),放出46.1×2KJ热量,所以反应的热化学方程式为:N2(g)+3H2(g)?2NH3(g)△H=-92.2kJ•mol-1;故答案为:N2(g)+3H2(g)?2NH3(g)△H=-92.2kJ•mol-1;
(2)因为0.5mol CH4完全燃烧生成CO2(g)和H2O(l)时,放出445kJ的热量,则1mol CH4完全燃烧生成CO2(g)和H2O(l)时,放出890kJ的热量,所以反应的热化学方程式为:CH4(g)+2O2(g)═CO2(g)+2H2O(l)△=-890kJ•mol-1;故答案为:CH4(g)+2O2(g)═CO2(g)+2H2O(l)△=-890kJ•mol-1;
(3)由图可知,1mol NO2和1mol CO反应生成CO2和NO放出热量为:368-134=234kJ,
反应热化学方程式为:NO2(g)+CO(g)=NO(g)+CO2(g)△H=-234 kJ•mol-1 .
故答案为:NO2(g)+CO(g)=NO(g)+CO2(g)△H=-234 kJ•mol-1 ;
(4)已知:①CH4(g)+2H2O(g)═CO2(g)+4H2(g)△H=+165kJ•mol-1
②CO(g)+H2O(g)═CO2(g)+H2(g)△H=-41kJ•mol-1,
根据盖斯定律,②-①可得:CO(g)+3H2(g)=CH4(g)+H2O(g)△H=-206kJ•mol-1 ,
故答案为:CO(g)+3H2(g)=CH4(g)+H2O(g)△H=-206kJ•mol-1 .
点评 本题考查了热化学方程式的书写,题目难度中等,注意掌握盖斯定律的应用和热化学方程式的书写原则,试题培养了学生的分析能力及灵活应用能力.

 阅读快车系列答案
阅读快车系列答案| t℃ | 700 | 800 | 850 | 1000 | 1200 |
| K | 2.6 | 1.7 | 1.0 | 0.9 | 0.6 |
(2)该反应的正反应为放热反应(“吸热”或“放热”);原因是升高温度平衡常数减小,平衡逆向移动
(3)能判断该反应是否已经达到化学平衡状态的是:D
A.混合气体总的物质的量不变 B.容器中压强不变
C.混合体系中平均摩尔质量不变 D.混合气体中CO浓度不变
(4)在850℃时,可逆反应:CO2(g)+H2(g)?CO(g)+H2O(g),在该容器内各物质的浓度变化如下:
| 时间/min | CO2 (mol/L) | H2 (mol/L) | CO (mol/L) | H2O( mol/L) |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | c1 | c2 | c3 | c3 |
| 4 | c1 | c2 | c3 | c3 |
①前2min,CO2的平均反应速率;
②3min-4min达到平衡时CO的平衡浓度c3(c3精确到小数点后面三位数).
| A. | B的消耗速率与B的生成速率相等 | |
| B. | 单位时间内消耗3a mol C,同时生成a mol A | |
| C. | 容器内的压强不再变化 | |
| D. | 混合气体的密度不再变化 |
| A. | 硫酸溶液与氢氧化钡溶液:H++SO42-+Ba2++OH-═H2O+BaSO4↓ | |
| B. | 硫酸与氢氧化镁溶液:H++OH-═H2O | |
| C. | 碳酸钙与稀硝酸:CO32-+2H+═CO2↑+H2O | |
| D. | 铁与稀硫酸反应:Fe+2H+═Fe2++H2↑ |
| A. | 1molNa2O2晶体中共含有4NA个离子 | |
| B. | 0.1mol AlCl3完全水解转化为氢氧化铝胶体,生成0.1NA个胶粒 | |
| C. | 常温常压下16gO2和O3混合气体含有NA个氧原子 | |
| D. | 1mol/LNa2CO3溶液中含有NA个CO32- |