题目内容
下列反应最后能产生沉淀的是( )
| A、向AlCl3溶液中加过量的NaOH溶液 |
| B、向NaAlO2溶液中加过量的盐酸 |
| C、向AlCl3溶液中通入过量的CO2 |
| D、向NaAlO2溶液中通入过量的CO2 |
考点:钠的重要化合物,镁、铝的重要化合物
专题:
分析:A、氢氧化铝具有两性,能与强碱反应;
B、氢氧化铝具有两性,能与强酸反应;
C、碳酸的酸性比盐酸弱;
D、碳酸是弱酸.
B、氢氧化铝具有两性,能与强酸反应;
C、碳酸的酸性比盐酸弱;
D、碳酸是弱酸.
解答:
解:A、氢氧化铝具有两性,NaOH过量,生成NaAlO2,得不到氢氧化铝沉淀,故A错误;
B、氢氧化铝具有两性,盐酸过量,生成AlCl3,得不到氢氧化铝沉淀,故B错误;
C、碳酸的酸性比盐酸弱,故AlCl3溶液中通入过量的CO2不发生反应,故C错误;
D、碳酸是弱酸,能与NaAlO2反应生成氢氧化铝白色沉淀,氢氧化铝不能与弱酸反应,故D正确,
故选:D.
B、氢氧化铝具有两性,盐酸过量,生成AlCl3,得不到氢氧化铝沉淀,故B错误;
C、碳酸的酸性比盐酸弱,故AlCl3溶液中通入过量的CO2不发生反应,故C错误;
D、碳酸是弱酸,能与NaAlO2反应生成氢氧化铝白色沉淀,氢氧化铝不能与弱酸反应,故D正确,
故选:D.
点评:本题重点考查了氢氧化铝的两性,能溶于强酸、强碱,不溶于弱酸、弱碱,金属的重要化合物是高考热点题型,每年高考必考.

练习册系列答案
 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案
相关题目
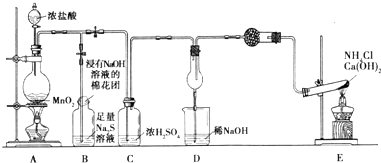
用下列实验装置完成对应的实验(部分仪器已省),能达到实验目的是( )
A、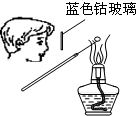 检验Na2CO3中的Na+ |
B、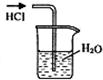 吸收HCl |
C、 石油的蒸馏 |
D、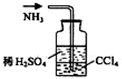 吸收NH3 |
工业上从含硒的废液中提取硒的方法之一是:用硫酸和硝酸处理废料,获得亚硒酸和少量硒酸,再与盐酸共热,硒酸转化为亚硒酸(2HCl+H2SeO4=H2SeO3+Cl2↑+H2O),通SO2于亚硒酸溶液中,有单质硒析出.据此,下列说法错误的是( )
| A、氧化性:H2SeO4>C12>H2SO3 |
| B、酸性:H2SO4>H2SeO4 |
| C、析出l mol硒需要消耗标准状况下22.4L SO2 |
| D、硒酸转化为亚硒酸的反应中氧化产物为Cl2 |
具有下列性质的有机化合物中同分异构体数目最多的是(不考虑立体异构)( )
| A、分子式为C7H8O且可与金属钠反应放出氢气的有机化合物 |
| B、分子式为C5H10O2且可与碳酸氢钠反应放出二氧化碳的有机化合物 |
| C、分子式为C5H10且能使溴的四氯化碳溶液褪色的有机化合物 |
| D、C6H12中沸点最高的烃与氯气反应后的一氯代有机化合物 |
下列有关物质应用的说法中,正确的是( )
| A、氢氧化铝具有弱碱性,可用于制胃酸中和剂 |
| B、用二氧化硫加工银耳,使之更白 |
| C、二氧化锰具有强氧化性,故能将双氧水氧化为氧气 |
| D、NH3极易溶于水,可用作制冷剂 |
设NA代表阿伏加德罗常数的值,下列有关叙述正确的是( )
| A、电解精炼铜时,若阳极质量减少6.4 g,则电路中转移电子数为0.2NA |
| B、标准状况下,44.8LNO与22.4LO2混合后气体中分子总数等于2NA |
| C、NO2和H2O反应每生成2molHNO3时转移的电子数目为2NA |
| D、lmolFe在氧气中充分燃烧失去3NA个电子 |
设NA为阿伏伽德罗常数的值,下列有关NA的说法正确的是( )
| A、标准状况下,0.1 mol Cl2溶于水,转移的电子数目为0.1NA |
| B、将含0.l mol FeCl3的饱和溶液制成胶体后,生成的Fe(OH)3胶粒数目为0.1NA |
| C、1 mol Fel2与足量氯气反应时转移的电子数为2NA |
| D、标准状况下,560ml的CH4和甲醛的混合气体,含有的共用电子对数为0.1NA |
关于硅的叙述不正确的是( )
| A、高纯硅是良好的半导体 |
| B、硅是制造太阳能电池的常用材料 |
| C、单质硅既不能与酸反应又不能与碱反应 |
| D、硅在地壳中含量居第二位,但在自然界中没有游离态的硅存在 |