题目内容
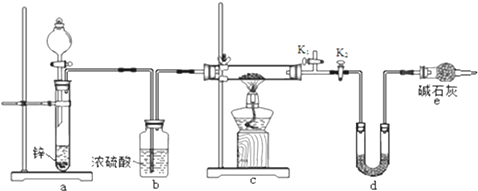
14.下列实验操作不正确的是( )| A. | 过滤时如果发现滤液是浑浊的,则滤液还要进行过滤 | |
| B. | 在进行蒸馏时,要加少量碎瓷片,防止液体暴沸 | |
| C. | 在进行分液操作时,分液漏斗内外气体相通,眼睛要注视烧杯中的溶液 | |
| D. | 在进行蒸馏时,温度计不要插入溶液中 |
分析 A.过滤时发现滤液浑浊,说明过滤不彻底;
B.碎瓷片有放暴沸作用;
C.分液时眼睛应注视分液漏斗里的液面;
D.蒸馏时,温度计测量馏分温度.
解答 解:A.过滤时如果发现滤液浑浊,说明过滤不彻底,滤液还要进行再次过滤,故A正确;
B.加入碎瓷片,可以通过孔隙凝聚水蒸汽,使成为气泡浮出,防止爆沸,故B正确;
C.分液时,使分液漏斗内外气体相通,便于液体顺利流下,眼睛应注视分液漏斗里的液面,下层液体从下口放出后立即关闭活塞,将上层液体从上口倒出,故C错误;
D.蒸馏时,温度计测量馏分温度,温度计水银球应在蒸馏烧瓶支管口处,不能插入溶液中,故D正确,
故答案为:C.
点评 本题以化学实验方案评价为载体考查实验基本操作,明确实验原理及基本操作规范性是解本题关键,注意从操作规范性、评价性进行分析解答,易错选项是D,注意温度计位置.

练习册系列答案
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案
相关题目
4.2SO2(g)+O2(g)═2SO3(g)的反应中,反应1分钟后,SO3的浓度增加了0.9mol/L,则O2表示的平均速率为( )
| A. | 0.45mol/(L•min) | B. | 0.55mol/(L•min) | C. | 0.60mol/(L•min) | D. | 0.90mol/(L•min) |
5.化学与材料、生活和环境密切相关.下列有关说法中错误的是( )
| A. | 煤炭经过干馏,石油经分馏、裂化、裂解化工处理,可获得清洁能源和重要的化工原料 | |
| B. | 比能量低而笨重的铅蓄电池使用时电压不稳定,所以有被其他新型电池取代的趋势 | |
| C. | 玛瑙饰品的主要成分与建筑材料砂子相同 | |
| D. | 神舟10号飞船所用太阳能电池板可将光能转换为电能,所用转换材料单晶硅也可以制备电脑芯片 |
9.电石制取乙炔产生大量废渣:电石渣(主要成分为Ca(OH)2,另外还含有Fe和Al化学物及SO2等杂质),可用下面工艺实现电石渣吸收氯碱工业废气中的氯气,综合治理废渣和废气,回答下列问题:
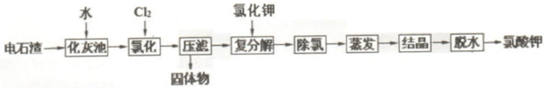
已知:①几种物质溶解度与温度的关系
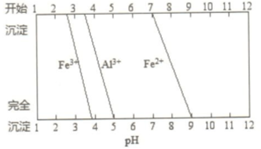
②几种离子开始和完全沉淀与pH的关系图
(1)某导电塑料是以乙炔为单体加聚合成,其化学为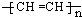 .
.
(2)化灰池中为加快水浸的速度,常采取的措施搅拌、加热.
(3)为除去Fe/Al 等杂质,氯化过程中需要控制溶液 pH为6-7.
(4)氯化过程的温度控制在 75~80℃,该过程主要反应的离子方程式为6Cl2+6Ca(OH)2=6Ca2++10Cl-+2ClO3-. 温度过低会发生副反应,产生的副产物为Ca(ClO)2(写化学式).
(5)复分解反应中,常控制温度为 20℃,加入KCl 发生的反应的方程式Ca(ClO3)2+2KCl=CaCl2+2KClO3+6H2O.
(6)通常用石墨电极电解 KClO 溶液制备 KClO3,则阳极的电极反应方程式为ClO--4e-+2H2O=ClO3-+4H+.
脱水过程实现固液分离,工业常用的设备是C
A.蒸馏塔 B.反应釜 C.离心机 D.交换器
(7)现代工艺氯化时通入O2做氧化剂提高效率,其氯化的化学方程式为2Ca(OH)2+2Cl2+5O2=2Ca(ClO3)2+2H2O.

已知:①几种物质溶解度与温度的关系
| 温度/ | 0 | 10 | 20 | 30 | 40 |
| S(CaCl2)/g | 59.5 | 64.7 | 74.5 | 100 | 128 |
| S[Ca(ClO3)2]/g | 209 | ||||
| S(KClO3)/g | 3.3 | 5.2 | 7.3 | 10.2 | 13.9 |

(1)某导电塑料是以乙炔为单体加聚合成,其化学为
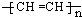 .
.(2)化灰池中为加快水浸的速度,常采取的措施搅拌、加热.
(3)为除去Fe/Al 等杂质,氯化过程中需要控制溶液 pH为6-7.
(4)氯化过程的温度控制在 75~80℃,该过程主要反应的离子方程式为6Cl2+6Ca(OH)2=6Ca2++10Cl-+2ClO3-. 温度过低会发生副反应,产生的副产物为Ca(ClO)2(写化学式).
(5)复分解反应中,常控制温度为 20℃,加入KCl 发生的反应的方程式Ca(ClO3)2+2KCl=CaCl2+2KClO3+6H2O.
(6)通常用石墨电极电解 KClO 溶液制备 KClO3,则阳极的电极反应方程式为ClO--4e-+2H2O=ClO3-+4H+.
脱水过程实现固液分离,工业常用的设备是C
A.蒸馏塔 B.反应釜 C.离心机 D.交换器
(7)现代工艺氯化时通入O2做氧化剂提高效率,其氯化的化学方程式为2Ca(OH)2+2Cl2+5O2=2Ca(ClO3)2+2H2O.
19.下列用电子式表示的形成过程正确的是( )
| A. | 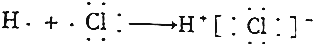 | |
| B. | 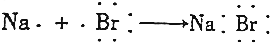 | |
| C. | 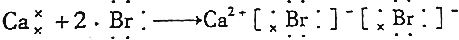 | |
| D. | 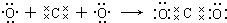 |
6.下列说法正确的是( )
| A. | 金属元素在不同的化合物中化合价均相同 | |
| B. | 所有合金都只含有金属元素 | |
| C. | 可利用铝热反应冶炼单质镁 | |
| D. | 镁合金的硬度和强度均高于纯镁 |
14.“美丽中国”是十八大提出的重大课题,她突出了生态文明,重点是社会发展与自然环境之间的和谐,下列行为中不符合这一主题的是( )
| A. | 推广“低碳经济”,减少温室气体的排放 | |
| B. | 开发太阳能、风能和氢能等能源代替化石燃料,有利于节约资源、保护环境 | |
| C. | 采用“绿色化学”工艺,使原料尽可能转化为所需要的物质 | |
| D. | 关停化工企业,消除污染源头 |
15.下列各组物质中比值为2:1的是( )
| A. | pH均为12的烧碱溶液与Ba(OH)2溶液的物质的量浓度之比 | |
| B. | (NH4)2SO4溶液中c(NH4+)与c(SO42-)之比 | |
| C. | 0.2mol/L的CH3COOH溶液与0.1mol/L和CH3COOH溶液中c(H+)之比 | |
| D. | 0.2mol/L的HCl与0.1mol/LHNO3溶液中n(H+)之比 |

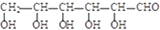 碱性条件下氧化为
碱性条件下氧化为 .
.