题目内容
下列说法中正确的是( )
| A、1 mol O2和1 mol N2所占的体积都约为22.4 L |
| B、H2的气体摩尔体积约为22.4 L |
| C、在标准状况下,1 mol H2和1 mol H2O所占的体积都约为22.4 L |
| D、在标准状况下,22.4 L由N2、N2O组成的混合气体中所含有的N的物质的量约2 mol |
考点:气体摩尔体积
专题:
分析:A、标况下的气体,Vm=22.4L/mol;
B、摩尔体积单位是L/mol;
C、标况下,水不是气体;
D、根据n=
求出混合气体的物质的量,然后根据N2和N2O均有2个N原子来分析.
B、摩尔体积单位是L/mol;
C、标况下,水不是气体;
D、根据n=
| V |
| Vm |
解答:
解:A、标况下,1 mol O2和1 mol N2所占的体积都约为22.4 L,故A错误;
B、H2的气体摩尔体积约为22.4 L/mol,故B错误;
C、在标准状况下,1 mol H2所占的体积都约为22.4 L,但是水在该状态下不是气体,体积不是22.4L,故C错误;
D、根据n=
可知混合气体的物质的量n=
=1mol,由于N2和N2O均有2个N原子,故1mol混合气体中含2mol氮原子,故D正确.
故选D.
B、H2的气体摩尔体积约为22.4 L/mol,故B错误;
C、在标准状况下,1 mol H2所占的体积都约为22.4 L,但是水在该状态下不是气体,体积不是22.4L,故C错误;
D、根据n=
| V |
| Vm |
| 22.4L |
| 22.4L/mol |
故选D.
点评:本题考查了阿伏伽德罗常数的有关计算,掌握公式的使用和物质的结构是关键,难度不大.

练习册系列答案
相关题目
取一质量为mg的铜丝在空气中加热后,插入下列液体中,铜丝的质量仍为mg的是( )
| A、盐酸 |
| B、NaOH溶液 |
| C、CH3CHO |
| D、CH3OH |
有M、N两溶液,各含有下列十四种离子中的七种离子:Al3+、Cl-、Na+、K+、NO3-、OH-、SO32-、MnO4-、Fe3+、NH4+、H+、SO42-、CO32-、AlO2-.已知两溶液所含离子各不相同,每组溶液中的阳离子至少有2种,则下列说法正确的是( )
| A、如果M溶液呈强酸性,则N溶液中可能含有的阴离子有:OH-、NO3-、CO32- |
| B、如果M溶液呈强碱性,则N溶液中可能含有的阴离子有:MnO4-、AlO2-、SO42- |
| C、如果M溶液具有强还原性,则N溶液中可能含有的阴离子有:MnO4-、NO3-、SO42- |
| D、如果M溶液具有强氧化性,则N溶液中可能含有的阳离子有:K+、Na+、NH4+ |
0.5L的Fe2(SO4)3溶液中Fe3+的浓度为0.2mol/L,与0.2L0.5mol/L的Na2SO4溶液中SO42-的浓度之比是( )
| A、3:2 | B、2:5 |
| C、3:5 | D、5:3 |
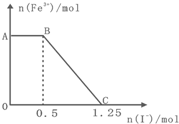 已知酸性高锰酸钾溶液可以将FeSO4氧化,化学反应方程式为:
已知酸性高锰酸钾溶液可以将FeSO4氧化,化学反应方程式为:2KMnO4+10FeSO4+8H2SO4═K2SO4+2MnSO4+5Fe2(SO4)3+8H2O,现将一定量的硫酸酸化的高锰酸钾溶液与硫酸亚铁溶液混合,充分反应后再向所得溶液中加入KI溶液(假设I-与KMnO4反应的氧化产物为I2),混合溶液中铁离子的物质的量随加入的KI的物质的量的变化关系如图所示,则下列有关说法不正确的是( )
| A、图中AB段主要是高锰酸钾和碘化钾溶液反应 | ||||
| B、图中BC段发生的反应为2Fe3++2I-═2Fe2++I2通电 | ||||
| C、根据OC段的数据可知开始加入的高锰酸钾的物质的量为0.25mol | ||||
D、以Pt为电极材料电解C点的溶液,总反应式为2H2O
|
如图示装置是化学实验室的常用装置,它有多种用途.以下各项用途的操作都正确的是( )


| A、洗气或干燥装置:瓶内放一定体积溶液,由a进气 |
| B、用于收集氢气:瓶内充满水,由b进气 |
| C、排空气收集H2:瓶内充满空气,由a进气 |
| D、病人输氧时用于观察输氧速度:瓶内装适量水,b接病人鼻腔 |
铜粉放入稀H2SO4中,加热后无明显现象,当加入一种盐后,铜粉质量减小,溶液变蓝,同时有气体逸出,此盐可能是( )
| A、FeSO4 |
| B、Na2CO3 |
| C、KNO3 |
| D、KCl |