题目内容
X、Y、Z、W均为中学化学中常见的单质或化合物,它们之间的转化关系如图1所示(水及部分产物已略去).
(1)若X为金属单质,W是某强酸的稀溶液.X与过量W反应生成Y的离子方程式为 向Z溶液中加入某种试剂 (填试剂名称或化学式),若出现蓝色沉淀,即可判断Z溶液中阳离子的存在.
(2)若X为非金属单质,W是空气的主要成分之一.它们之间转化的能量变化如图2中A所示,则X+W→Z的热化学方程式为 .
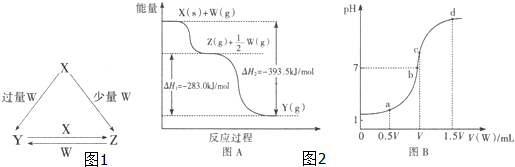
(3)若X、Y为正盐,X的水溶液显酸性,W为一元强碱(化学式为MOH),Z的电离方程式为 .室温下,若用0.1mol/L的W溶液滴定V mL 0.1mol/L HA溶液,滴定曲线如图2中B所示,则a、b、c、d四点溶液中水的电离程度最大的是 点;a点溶液中离子浓度的大小顺序为 ;取少量c点溶液于试管中,再滴加0.1mol/L盐酸至中性,此时溶液中除H+、OH-外,离子浓度的大小顺序为 .
(1)若X为金属单质,W是某强酸的稀溶液.X与过量W反应生成Y的离子方程式为
(2)若X为非金属单质,W是空气的主要成分之一.它们之间转化的能量变化如图2中A所示,则X+W→Z的热化学方程式为

(3)若X、Y为正盐,X的水溶液显酸性,W为一元强碱(化学式为MOH),Z的电离方程式为
考点:无机物的推断
专题:推断题
分析:(1)若X为金属单质,W是某强酸的稀溶液,由转化关系可知,X为变价金属为Fe,W为硝酸,Y是硝酸铁,Z是硝酸亚铁,依据亚铁离子的检验方法分析判断;
(2)若X为非金属单质,X和W反应生成物与W的量有关,则X是变价元素,W是空气的主要成分之一,则X为碳、W为氧气,Y是二氧化碳,Z是一氧化碳;
(3)若X、Y为正盐,X的水溶液显酸性,W为一元强碱(化学式为MOH),X为铝盐、Y为偏铝酸盐、Z为氢氧化铝.
(2)若X为非金属单质,X和W反应生成物与W的量有关,则X是变价元素,W是空气的主要成分之一,则X为碳、W为氧气,Y是二氧化碳,Z是一氧化碳;
(3)若X、Y为正盐,X的水溶液显酸性,W为一元强碱(化学式为MOH),X为铝盐、Y为偏铝酸盐、Z为氢氧化铝.
解答:
解:(1)若X为金属单质,W是某强酸的稀溶液,由转化关系可知,X为变价金属为Fe,W为硝酸,Y是硝酸铁,Z是硝酸亚铁,
铁和过量硝酸反应生成硝酸铁、一氧化氮和水,离子方程式为:Fe+4H++NO3-=Fe3++NO↑+2H2O,检验亚铁离子的试剂是,铁氰化钾或K3[Fe(CN)6],溶液若出现蓝色沉淀,即可判断硝酸亚铁溶液中阳离子的存在;
故答案为:Fe+4H++NO3-=Fe3++NO↑+2H2O;铁氰化钾或K3[Fe(CN)6];
(2)若X为非金属单质,X和W反应生成物与W的量有关,则X是变价元素,W是空气的主要成分之一,则X为碳、W为氧气,Y是二氧化碳,Z是一氧化碳,
碳和少量氧气反应生成一氧化碳,根据图知△H=-393.5kJ/mol-(-283.0kJ/mol)=-110.5kJ/mol,
所以该热化学反应方程式为C(s)+
O2(g)=CO(g)△H=-110.5kJ/mol,
故答案为:C(s)+
O2(g)=CO(g)△H=-110.5kJ/mol;
(3)若X、Y为正盐,X的水溶液显酸性,W为一元强碱(化学式为MOH),X为铝盐、Y为偏铝酸盐、Z为氢氧化铝,铝离子和过量强碱反应生成偏铝酸盐和水,氢氧化铝是两性氢氧化物存在酸式电离和碱式电离,电离方程式为:H++AlO2-+H2O?Al(OH)3?Al3++3OH-;酸或碱抑制水电离,含有弱根离子的盐促进水电离,根据图知,a、b点酸过量,d碱过量,c点二者恰好反应生成强碱弱酸盐,则水的电离程度最大,a点溶液中溶质是等物质的量浓度的HA和MA,溶液呈酸性,则c(H+)>c(OH-),根据电荷守恒得c(H+)+c(M+)=c(OH-)+c(A-),所以c(A-)>c(M+),酸的电离程度较小,所以c(M+)>c(H+),则离子浓度大小顺序是c(A-)>c(M+)>c(H+)>c(OH-),取少量c点溶液于试管中,再滴加0.1mol/L盐酸至中性,此时溶液中除H+、OH-外,离子浓度的大小顺序为c(M+)>c(A-)>c(Cl-);
故答案为:H++AlO2-+H2O?Al(OH)3?Al3++3OH-;c;c(A-)>c(M+)>c(H+)>c(OH-);c(M+)>c(A-)>c(Cl-).
铁和过量硝酸反应生成硝酸铁、一氧化氮和水,离子方程式为:Fe+4H++NO3-=Fe3++NO↑+2H2O,检验亚铁离子的试剂是,铁氰化钾或K3[Fe(CN)6],溶液若出现蓝色沉淀,即可判断硝酸亚铁溶液中阳离子的存在;
故答案为:Fe+4H++NO3-=Fe3++NO↑+2H2O;铁氰化钾或K3[Fe(CN)6];
(2)若X为非金属单质,X和W反应生成物与W的量有关,则X是变价元素,W是空气的主要成分之一,则X为碳、W为氧气,Y是二氧化碳,Z是一氧化碳,
碳和少量氧气反应生成一氧化碳,根据图知△H=-393.5kJ/mol-(-283.0kJ/mol)=-110.5kJ/mol,
所以该热化学反应方程式为C(s)+
| 1 |
| 2 |
故答案为:C(s)+
| 1 |
| 2 |
(3)若X、Y为正盐,X的水溶液显酸性,W为一元强碱(化学式为MOH),X为铝盐、Y为偏铝酸盐、Z为氢氧化铝,铝离子和过量强碱反应生成偏铝酸盐和水,氢氧化铝是两性氢氧化物存在酸式电离和碱式电离,电离方程式为:H++AlO2-+H2O?Al(OH)3?Al3++3OH-;酸或碱抑制水电离,含有弱根离子的盐促进水电离,根据图知,a、b点酸过量,d碱过量,c点二者恰好反应生成强碱弱酸盐,则水的电离程度最大,a点溶液中溶质是等物质的量浓度的HA和MA,溶液呈酸性,则c(H+)>c(OH-),根据电荷守恒得c(H+)+c(M+)=c(OH-)+c(A-),所以c(A-)>c(M+),酸的电离程度较小,所以c(M+)>c(H+),则离子浓度大小顺序是c(A-)>c(M+)>c(H+)>c(OH-),取少量c点溶液于试管中,再滴加0.1mol/L盐酸至中性,此时溶液中除H+、OH-外,离子浓度的大小顺序为c(M+)>c(A-)>c(Cl-);
故答案为:H++AlO2-+H2O?Al(OH)3?Al3++3OH-;c;c(A-)>c(M+)>c(H+)>c(OH-);c(M+)>c(A-)>c(Cl-).
点评:本题考查了物质的推断,明确物质的性质是解本题关键,根据物质间的特殊性质及转化关系进行推断,涉及盐类水解、酸碱中和反应、热化学反应等知识点,难点是离子浓度大小的比较,掌握基础是关键,难度中等.

练习册系列答案
相关题目
有机物X的结构如下,下列说法正确的是( )
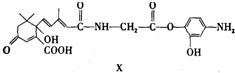

| A、X能发生氧化、取代、酯化、加聚、缩聚反应 |
| B、X与FeCl3溶液不能发生显色反应 |
| C、1mol X与足量NaOH溶液反应,最多消耗2mol NaOH |
| D、X的分子式为C23H26N2O7 |
下列说法正确的是( )
| A、共价化合物中可能含有离子键 | ||||||
| B、Ca2+、K+、Cl-、S2-四种粒子的离子半径依次减小 | ||||||
C、
| ||||||
| D、第ⅥA族元素氧、硫、硒对应的氢化物H2O、H2S、H2Se的稳定性依次减弱 |
 酚酞,别名非诺夫他林,是制药工业原料:适用于习惯性顽固便秘,有片剂、栓剂等多种剂型,其结构如右图所示,有关酚酞说法不正确的是( )
酚酞,别名非诺夫他林,是制药工业原料:适用于习惯性顽固便秘,有片剂、栓剂等多种剂型,其结构如右图所示,有关酚酞说法不正确的是( )| A、分子式为C20H14O4 |
| B、可以发生取代反应、加成反应、氧化反应 |
| C、含有的官能团有羟基、酯基 |
| D、1mol该物质可与H2和溴水发生反应,消耗H2和Br2的最大值为10mol和4mol |
用下列实验装置进行相应实验,设计正确且能达到实验目的是( )
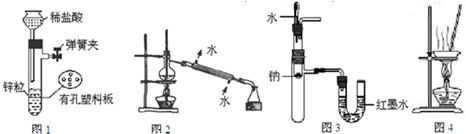

| A、用图1所示装置制取少量H2 |
| B、用图2所示装置分离Na2CO3溶液和CH3COOC2H5的混合物 |
| C、用图3所示装置验证Na和水反应的热效应 |
| D、用图4所示装置蒸干NH4Cl饱和溶液制备NH4Cl晶体 |
已知过氧化铬(CrO5)的结构式如下图所示,过氧化铬不稳定,溶于水生成过氧铬酸;溶于酸生成铬(Ⅲ)盐(绿色)并放出氧气,反应方程式为:4CrO5+12H+═4Cr3++7O2+6H2O,下列有关说法正确的是( )


| A、CrO5中Cr元素的化合价为+10 |
| B、过氧化铬中含有极性共价键、非极性共价键和离子键 |
| C、过氧化铬是酸性氧化物,具有较强的氧化性 |
| D、上述反应每转移0.2mol电子就能生成2.24L O2 |
下列关于物质应用和组成的说法正确的是( )
| A、P2O5可用于干燥Cl2和NH3 |
| B、“可燃冰”主要成分是甲烷和水 |
| C、CCl4可用于鉴别溴水和碘水 |
| D、Si和SiO2都用于制造光导纤维 |
