题目内容
20.在NaOH的环境中,Cl2与NaI反应,每1molNaI完全反应转移6mol电子,写出反应的化学方程式3Cl2+NaI+6NaOH=NaIO3+6NaCl+3H2O.分析 每1molNaI完全反应转移6mol电子,则I元素的化合价由-1价升高为+5价,生成NaIO3,结合电子守恒可知反应还生成NaCl,以此来解答.
解答 解:每1molNaI完全反应转移6mol电子,则I元素的化合价由-1价升高为+5价,生成NaIO3,结合电子守恒可知反应还生成NaCl,该反应为3Cl2+NaI+6NaOH=NaIO3+6NaCl+3H2O,故答案为:3Cl2+NaI+6NaOH=NaIO3+6NaCl+3H2O.
点评 本题考查化学反应方程式的书写,为高频考点,把握氧化还原反应的规律、化合价分析转移电子为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
相关题目
10.以下有机反应类型:①取代反应 ②加成反应 ③消去反应 ④酯化反应 ⑤加聚反应 ⑥还原反应,其中可能在有机分子中新产生羟基的反应类型是( )
| A. | ①②③ | B. | ①④⑥ | C. | ①②⑥ | D. | ②④⑤ |
11.下列图示与对应的叙述不相符的是( )
| A. | 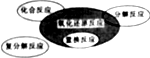 四种基本反应类型有氧化还原反应的关系 | |
| B. | 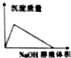 AlCl3溶液中滴加NaOH溶液生成沉淀的情况 | |
| C. | 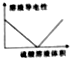 Ba(OH)2溶液中滴加硫酸溶液时的导电性情况 | |
| D. |  等体积、等浓度的稀硫酸分别与足量的铁和镁反应的情况 |
8.意大利科学家最近合成了一种新型的氧分子,其化学式为O4,下列关于O4的说法正确的是( )
| A. | 一个分子O4由两个分子O2构成 | |
| B. | O4是一种单质 | |
| C. | 等体积的O4和O2含有相同数目的分子 | |
| D. | 等质量的O4和O2含有相同数目的氧原子 |
15.能正确表示下列反应的离子方程式的为( )
| A. | 制备Fe(OH)3胶体:Fe3++3OH-=Fe(OH)3↓ | |
| B. | 稀硝酸中加入过量的铁粉:3Fe+2NO${\;}_{3}^{-}$+8H+=3Fe2++2NO↑+4H2O | |
| C. | 向Na2SiO3溶液中加入通入过量的H2S:SiO32-+H2SiO3↓+S2- | |
| D. | 向含amolFel2的水溶液中通入amol的Cl2反应为:2Fe2-+2l-+2Cl2=2Fe2++4Cl-+l2 |
9.下列烷烃的命名正确的是( )
| A. | 2,3-二乙基戊烷 | B. | 5-甲基-3-乙基已烷 | ||
| C. | 2-甲基-4-乙基戊烷 | D. | 2,3,3-三甲基戊烷 |
6.锂被誉为“金属味精”以LiCoO2为正极材料的锂离子电池已被广泛用作便携式电源.工业上常以β-锂辉矿(主要成分为LiAlSi2O6,还含有FeO、MgO、CaO等杂质)为原料来制取金属锂.其中一种工艺流程如下:

已知:①部分金属氢氧化物开始沉淀和完全沉淀时的pH:
②Li2CO3在不同温度下的溶解度如下表:
请回答下列问题:
(1)用氧化物形式表示LiAlSi2O6的组成:Li2O•Al2O3•4SiO2.
(2)反应Ⅱ加入碳酸钙的作用是除去反应Ⅰ中过量的H2SO4,控制pH,使Fe3+、Al3+完全沉淀.
(3)写出沉淀A的成分Mg(OH)2、CaCO3.
(4)反应Ⅳ生成Li2CO3沉淀,写出在实验室中得到Li2CO3沉淀的操作名称过滤,洗涤所得Li2CO3沉淀要使用热水 (选填“热水”或“冷水”),你选择的理由是Li2CO3在较高温度下溶解度小,用热水洗涤可减少Li2CO3的损耗.
(5)电解熔融氯化锂生产锂时,阳极产生的氯气中会混有少量氧气,原因是加热蒸干LiCl溶液时,LiCl有少量水解生成LiOH,受热分解生成Li2O,电解时产生O2.

已知:①部分金属氢氧化物开始沉淀和完全沉淀时的pH:
| 氢氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| 开始沉淀pH | 2.7 | 3.7 | 9.6 |
| 完全沉淀pH | 3.7 | 4.7 | 11 |
| 温度/℃ | 0 | 10 | 20 | 50 | 75 | 100 |
| Li2CO3的溶解度/g | 1.539 | 1.406 | 1.329 | 1.181 | 0.866 | 0.728 |
(1)用氧化物形式表示LiAlSi2O6的组成:Li2O•Al2O3•4SiO2.
(2)反应Ⅱ加入碳酸钙的作用是除去反应Ⅰ中过量的H2SO4,控制pH,使Fe3+、Al3+完全沉淀.
(3)写出沉淀A的成分Mg(OH)2、CaCO3.
(4)反应Ⅳ生成Li2CO3沉淀,写出在实验室中得到Li2CO3沉淀的操作名称过滤,洗涤所得Li2CO3沉淀要使用热水 (选填“热水”或“冷水”),你选择的理由是Li2CO3在较高温度下溶解度小,用热水洗涤可减少Li2CO3的损耗.
(5)电解熔融氯化锂生产锂时,阳极产生的氯气中会混有少量氧气,原因是加热蒸干LiCl溶液时,LiCl有少量水解生成LiOH,受热分解生成Li2O,电解时产生O2.
7.已知葡萄糖的燃烧热△H=-2804kJ/mol,当它氧化生成1g水时放出的热量是( )
| A. | 26.0kJ | B. | 155.8kJ | C. | 51.9kJ | D. | 467.3kJ |
