题目内容
 化学模型可以将微观分子宏观化,直观表现分子的结构特点.如图为某烃分子的一种模型,有关说法正确的是( )
化学模型可以将微观分子宏观化,直观表现分子的结构特点.如图为某烃分子的一种模型,有关说法正确的是( )| A、它是乙烯的球棍模型 | B、它是只有一种键角的非极性分子 | C、它的电子式为: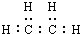 | D、半径较大原子核外电子排布的轨道表示式为: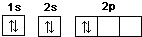 |
分析:A.根据图示的比例模型可知,该模型表示的为乙烯;
B.乙烯为平面三角形结构,键角为120°,且为非极性分子;
C.乙烯分子中存在碳碳双键,表示碳碳单键;
D.乙烯中半径较大原子为C,碳原子的2p轨道优先占据1个轨道,且自旋方向相同.
B.乙烯为平面三角形结构,键角为120°,且为非极性分子;
C.乙烯分子中存在碳碳双键,表示碳碳单键;
D.乙烯中半径较大原子为C,碳原子的2p轨道优先占据1个轨道,且自旋方向相同.
解答:解:A.该比例模型表示的分子含有2个C、4个H,且为平面结构,说明该有机物为乙烯,故A错误;
B.乙烯分子为平面三角形结构,键角都是120°,由于分子结构对称,乙烯为非极性分子,故B正确;
C.烯的分子式为C2H4,分子中碳原子与碳原子通过两对共用电子对相连接,碳原子与氢原子通过一对共用电子对相连接,所以乙烯的电子式为 ,故C错误;
,故C错误;
D.C原子的1s、2s、2p能量升高,2p轨道中电子优先单独占据1个轨道,且自旋方向相同,能量最低,正确的核外电子排布的轨道表示式为: ,故D错误;
,故D错误;
故选B.
B.乙烯分子为平面三角形结构,键角都是120°,由于分子结构对称,乙烯为非极性分子,故B正确;
C.烯的分子式为C2H4,分子中碳原子与碳原子通过两对共用电子对相连接,碳原子与氢原子通过一对共用电子对相连接,所以乙烯的电子式为
 ,故C错误;
,故C错误;D.C原子的1s、2s、2p能量升高,2p轨道中电子优先单独占据1个轨道,且自旋方向相同,能量最低,正确的核外电子排布的轨道表示式为:
 ,故D错误;
,故D错误;故选B.
点评:本题考查了电子式、比例模型、核外电子排布轨道的表示方法判断,题目难度中等,注意掌握常见化学用语的表示方法,明确比例模型的概念及表示方法是解答本题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列对有关化学用语的理解错误的是( )
A、电子式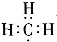 可以表示甲基,但是不可以表示C 可以表示甲基,但是不可以表示C
| ||
B、离子结构示意图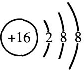 既可以表示32S2-,又可以表示34S2- 既可以表示32S2-,又可以表示34S2- | ||
C、比例模型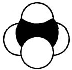 可以表示甲烷分子,也可以可以表示四氯化碳分子 可以表示甲烷分子,也可以可以表示四氯化碳分子 | ||
| D、分子式C3H8O既可以表示1-丙醇,又可以表示2-丙醇 |
对下列化学用语的理解和描述均正确的是( )
A、原子结构示意图 可以表示12C,也可以表示14C 可以表示12C,也可以表示14C | B、比例模型 可以表示二氧化碳分子,也可以表示水分子 可以表示二氧化碳分子,也可以表示水分子 | C、结构示意图为 的阴离子都不能破坏水的电离平衡 的阴离子都不能破坏水的电离平衡 | D、电子式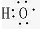 可以表示羟基,也可以表示氢氧根离子 可以表示羟基,也可以表示氢氧根离子 |