题目内容
4.氨是重要的氮肥,合成原理为:N2(g)+3H2(g) $?_{催化剂}^{高温、高压}$ 2NH3(g)△H=-92.4kJ/mol.回答下列问题:(1)写出平衡常数K的表达式$\frac{{c}^{2}(N{H}_{3})}{c({N}_{2}).{c}^{3}({H}_{2})}$,如果降低温度,该反应K值增大,化学反应速率减小,N2的转化率增大(填“增大”、“减小”或“不变”).
(2)在500℃、20MPa时,将N2、H2置于一个容积为2L的密闭容器中发生反应,反应过程中各种物质的量变化如图所示,回答下列问题:

①10min内以NH3表示的平均反应速率:0.005mol/(L.min).
②在10~20min内,NH3浓度变化的原因可能是B
A.加了催化剂 B.缩小容器体积
C.降低温度 D.增加NH3物质的量
③第1次达到平衡的时间为:10min,第2次达到平衡的时间为:20min;
④在反应进行至25min时,曲线发生变化的原因C
A.缩小容器体积 B.降低温度 C.分离了部分NH3
达第二次平衡时,新平衡的平衡常数K2等于K1,
(填“大于”、“小于”或“等于”).
分析 (1)化学平衡常数K等于生成物浓度幂之积与反应物浓度幂之积的比;该反应是一个反应前后气体体积减小的放热反应,降低温度平衡正向移动,化学反应速率减小;
(2)①10min内以v(NH3)=$\frac{\frac{△n}{V}}{△t}$;
②在10~20min内,根据图知,改变条件时各物质浓度不变且平衡正向移动;
③反应达到平衡状态时各物质的物质的量不变,相同时间内改变的物质的量增大,说明反应速率增大;
④在反应进行至25min时,氨气物质的量减小、氮气和氢气物质的量不变;
该反应中温度越高,化学平衡常数越小.
解答 解:(1)化学平衡常数K=$\frac{{c}^{2}(N{H}_{3})}{c({N}_{2}).{c}^{3}({H}_{2})}$;该反应是一个反应前后气体体积减小的放热反应,降低温度平衡正向移动,化学平衡常数增大,降低温度活化分子百分数减小导致化学反应速率减小,氮气转化率增大,
故答案为:$\frac{{c}^{2}(N{H}_{3})}{c({N}_{2}).{c}^{3}({H}_{2})}$;增大;减小;增大;
(2)①10min内以v(NH3)=$\frac{\frac{△n}{V}}{△t}$=$\frac{\frac{0.10-0}{2}}{10}$ mol/(L.min)=0.005mol/(L.min),
故答案为:0.005mol/(L.min);
②在10~20min内,根据图知,改变条件时各物质浓度不变且平衡正向移动,相同时间内改变的物质的量增大,说明反应速率增大,则改变的条件是缩小容器体积,故选B;
③反应达到平衡状态时各物质的物质的量不变,根据图知,第一次达到平衡时间为10min,第二次达到平衡时间为20min,
故答案为:10min;20min;
④在反应进行至25min时,氨气物质的量减小、氮气和氢气物质的量不变,所以改变条件是分离出部分氨气;
该反应中温度越高,化学平衡常数越小,温度相同则化学平衡常数相等,所以达第二次平衡时,新平衡的平衡常数K2等于K1,故答案为:C;等于.
点评 本题考查化学平衡计算、外界条件对化学平衡影响移动,侧重考查学生图象分析判断及计算能力,为高频考点,会根据曲线变化特点、变化趋势与外界条件关系判断改变条件,题目难度不大.

 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案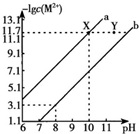 25℃时,Fe(OH)2和Cu(OH)2的饱和溶液中,金属阳离子的物质的量浓度的负对数[-lgC(M2+)]与溶液PH的变化关系如图所示,已知:该温度下,Ksp[Cu(OH)2]<Ksp[Fe(OH)2].下列说法正确的是( )
25℃时,Fe(OH)2和Cu(OH)2的饱和溶液中,金属阳离子的物质的量浓度的负对数[-lgC(M2+)]与溶液PH的变化关系如图所示,已知:该温度下,Ksp[Cu(OH)2]<Ksp[Fe(OH)2].下列说法正确的是( )| A. | b线表示Fe(OH)2饱和溶液中的变化关系,且Ksp[Fe(OH)2]=10-15.1 | |
| B. | 当Fe(OH)2和Cu(OH)2沉淀共存时,溶液中C(Fe2+):C(Cu2+)=1:104.6 | |
| C. | 向X点对应的饱和溶液中加入少量NaOH,可转化为Y点对应的溶液 | |
| D. | 除去CuSO4溶液中含有的少量Fe2+,可加入适量CuO |
| A. | 0.045 mol/L | B. | 1 mol/L | C. | 0.5 mol/L | D. | 2.24mol/L |
| A. | H2O(g)═H2(g)+O2(g)△H=+242 kJ•mol-1 | B. | 2H2(g)+O2(g)═2H2O(l)△H=-484 kJ•mol-1 | ||
| C. | H2(g)+O2(g)═H2O(g)△H=+242 kJ•mol-1 | D. | 2H2(g)+O2(g)═2H2O(g)△H=+484 kJ•mol-1 |
 25℃时,电离平衡常数:
25℃时,电离平衡常数:| 化学式 | CH3COOH | H2CO3 | HClO | |
| 电离平衡常数 | 1.8×10-5 | K1 4.3×10-7 K2 5.6×10-11 | 3.0×10-8 | |
(1)下列四种离子结合质子的能力由大到小的顺序是a>b>d>c;(填编号)
a.CO32- b.ClO- c.CH3COO- d.HCO3-
(2)下列反应不能发生的是:cd;
a.CO32-+CH3COOH=CH3COO-+CO2↑+H2O
b.ClO-+CH3COOH=CH3COO-+HClO
c.CO32-+HClO=CO2↑+H2O+ClO-
d.2ClO-+CO2+H2O=CO32-+2HClO
(3)用蒸馏水稀释0.10mol•L-1的醋酸,则下列各式表示的数值随水量的增加而增大的是B;
A.$\frac{c(C{H}_{3}COOH)}{c({H}^{+})}$ B.$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$ C.$\frac{c({H}^{+})}{{K}_{W}}$ D.$\frac{c({H}^{+})}{c(O{H}^{-})}$
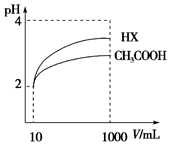
(4)体积为10mL pH=2的醋酸溶液与一元酸HX分别加水稀释至1000mL,稀释过程pH变化如图,则HX的电离平衡常数大于(填“大于”、“等于”或“小于”)醋酸的平衡常数,稀释后,HX溶液中水电离出来的c(H+)大于醋酸溶液中水电离出来的c(H+)(填“大于”、“等于”或“小于”)
(5)某温度下,纯水中c (H+)=2.0×10-7mol•L-1,0.9mol•L-1NaOH溶液与0.1mol•L-1HCl溶液等体积混合(不考虑溶液体积变化)后,溶液的pH=13.
| 选 项 | 操 作 | 现 象 | 结 论 |
| A | 向无水乙醇中滴入酸性KMnO4溶液,充分振荡 | 紫红色褪去 | 乙醇有氧化性 |
| B | 向某溶液中滴加BaCl2溶液 | 生成白色沉淀 | 原溶液中一定有SO42- |
| C | 向某无色溶液中滴加氯水和CCl4,振荡、静置 | 下层溶液显紫色 | 原溶液中有I- |
| D | 向某溶液中滴加稀NaOH溶液,将湿润红色石蕊试纸置于试管口 | 试纸不变蓝 | 原溶液中无NH4+ |
| A. | A | B. | B | C. | C | D. | D |
| 操作 | 现象 | 结论 | |
| A | 滴加稀盐酸 | 有气泡产生 | 原溶液中有CO32- |
| B | 滴加盐酸酸化的BaCl2溶液 | 生成白色沉淀 | 原溶液中有Ag+或SO42- |
| C | 用洁净铂丝蘸取溶液进行灼烧 | 火焰呈黄色 | 原溶液中有Na+、无K+ |
| D | 滴加稀NaOH溶液,将湿润红色石蕊试纸置于试管 | 试纸不变蓝 | 原溶液中无NH4+ |
| A. | A | B. | B | C. | C | D. | D |