题目内容
17.用0.1000mol•L-1NaOH溶液滴定未知浓度的盐酸,选用酚酞为指示剂,造成测定结果偏高的原因可能是( )| A. | 盛装待测液的锥形瓶用蒸馏水洗过,没用待测液润洗 | |
| B. | 酸式滴定管在使用前未用待测液盐酸润洗 | |
| C. | 滴定前碱式滴定管尖嘴中有气泡,滴定后气泡消失 | |
| D. | 滴定前读数平视,滴定终点读数时俯视碱式滴定管的刻度 |
分析 根据c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$分析不当操作对V(标准)的影响,以此判断浓度的误差.
解答 解:A、盛装待测液的锥形瓶用蒸馏水洗过,没用待测液润洗,待测液的物质的量不变,标准液的体积不变,结果不变,故A错误;
B、酸式滴定管在使用前未用待测液盐酸润洗,待测液盐酸被稀释,溶质的物质的量偏小,导致V(标准)偏小,根据c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$分析,则结果偏低,故B错误;
C、滴定前碱式滴定管尖嘴中有气泡,滴定后气泡消失,导致V(标准)偏大,根据c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$分析,则结果偏高,故C正确;
D、滴定前读数平视,滴定终点读数时俯视碱式滴定管的刻度,导致V(标准)偏小,根据c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$分析,则结果偏低,故D错误;
故选C.
点评 本题考查化学实验方案评价,为高频考点,侧重考查误差分析,明确实验原理是解本题关键,注意根据公式分析解答.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8.某工厂废水中含有毒的CrO42-和Cr2O72-,常见处理方法是使其转化为毒性较低的Cr3+或直接吸附除去.现有如下几种工艺:
(1)光催化法:在催化剂作用下,利用太阳光和人工光,使废水实现上述转化.
①该法的反应原理是2Cr2O72-+16H+→4Cr3++3O2+8H2O(将方程式补充完整)
②该法涉及的能量转化形式是.
③某小组通过实验研究催化剂中W(钨)和α-Fe2O3的比例对铬的去除率的影响(每次实验均采用:0.01mol/L 500mL酸化的K2Cr2O7溶液、总质量为0.2g的催化剂、光照10min),六价铬的去除率如下表所示.
上表中,b=15%;在去除率最高的催化剂实验组中,用Cr2O72-表示的该反应在10min内的平均化学反应速率v=mol/(L•min).
(2)电化学处理法:向废铁屑(铁碳合金)中加入含铬废水,一段时间后,废水中六价铬元素的去除率能达到90%.
①废铁屑在使用前酸洗除锈的离子方程式是Fe2O3+6H+=2Fe3++3H2O.
②结合电化学原理说明废铁屑在此过程中所起的作用是铁在原电池反应中做负极Fe-2e-=Fe2+,Fe2+做还原剂将六价铬还原.
(3)离子交换树脂(ROH)法:将CrO42-和Cr2O72-吸附至树脂上除去,原理如下:
2ROH+CrO42-→R2CrO4+2OH-、2ROH+Cr2O72-→R2Cr2O7+2OH-
(已知:废水中存在如下平衡:2CrO42-+2H+?Cr2O72-+H2O).
控制溶液酸性可以提高树脂对六价铬的去除率,其理由是由原理可知:2ROH~CrO42-~Cr,2ROH~Cr2O72-~2Cr,等量树脂去除Cr2O72-的效率高,因此控制酸性使上述平衡正向移动,使CrO42-转化为Cr2O72-.
(1)光催化法:在催化剂作用下,利用太阳光和人工光,使废水实现上述转化.
①该法的反应原理是2Cr2O72-+16H+→4Cr3++3O2+8H2O(将方程式补充完整)
②该法涉及的能量转化形式是.
③某小组通过实验研究催化剂中W(钨)和α-Fe2O3的比例对铬的去除率的影响(每次实验均采用:0.01mol/L 500mL酸化的K2Cr2O7溶液、总质量为0.2g的催化剂、光照10min),六价铬的去除率如下表所示.
| 催化剂组成 | 1 | 2 | 3 |
| WO3 W α-Fe2O3 | 65% 5% 30% | 65% 10% 25% | a b 20% |
| 六价铬去除率 | 60.2% | 80% | 72.9% |
(2)电化学处理法:向废铁屑(铁碳合金)中加入含铬废水,一段时间后,废水中六价铬元素的去除率能达到90%.
①废铁屑在使用前酸洗除锈的离子方程式是Fe2O3+6H+=2Fe3++3H2O.
②结合电化学原理说明废铁屑在此过程中所起的作用是铁在原电池反应中做负极Fe-2e-=Fe2+,Fe2+做还原剂将六价铬还原.
(3)离子交换树脂(ROH)法:将CrO42-和Cr2O72-吸附至树脂上除去,原理如下:
2ROH+CrO42-→R2CrO4+2OH-、2ROH+Cr2O72-→R2Cr2O7+2OH-
(已知:废水中存在如下平衡:2CrO42-+2H+?Cr2O72-+H2O).
控制溶液酸性可以提高树脂对六价铬的去除率,其理由是由原理可知:2ROH~CrO42-~Cr,2ROH~Cr2O72-~2Cr,等量树脂去除Cr2O72-的效率高,因此控制酸性使上述平衡正向移动,使CrO42-转化为Cr2O72-.
9.往氯水中滴入Na2SO3溶液的pH变化如图所示,下列说法正确的是( )
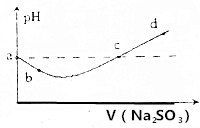

| A. | a点表示的溶液中存在3种分子,3种离子 | |
| B. | b点溶液中不存在SO2 | |
| C. | c点溶液中c(Na+)=2c(HSO3-)+2c(SO32-) | |
| D. | d点溶液中不存在HSO3- |
2.25℃时,Ksp(AgC1)=1.8×10-10,Ksp(AgI)=8.5×10-17,则下列说法正确的是( )
| A. | 向饱和AgCl水溶液中加入盐酸,Ksp(AgC1)变大 | |
| B. | AgNO3溶液与NaCl溶液混合后的溶液中,一定有c(Ag+)=c(Cl-) | |
| C. | 温度一定,当溶液中c(Ag+)c(Cl- )<Ksp(AgCl)时,此溶液中必有AgCl沉淀析出 | |
| D. | 向AgI的悬浊液中加NaCl浓溶液,可能有AgCl生成 |
9.原理Cr2O72-+CH3CH2OH+H++H2O→[Cr(H2O)6]3++CH3COOH(未配平)可用于检测司机是否酒后驾驶,下列说法正确的是( )
| A. | 消耗1 mol CH3CH2OH时转移电子的物质的量为4mol | |
| B. | 1mol/L CH3COOH溶液中含有σ键的数目为7NA个 | |
| C. | H2F+、NH2-、H2S、CH4均与H2O互为等电子体 | |
| D. | 在配合物[Cr(H2O)6]3+中,H、O原子与中心离子Cr3+形成配位键 |
6.S2Cl2是工业上常用的硫化剂,是一种金黄色液体.
已知:①S2Cl2不稳定,进一步氧化可得SCl2
②S2Cl2和SCl2 都与水反应,2S2Cl2+2H2O═3S↓+SO2↑+4HCl,3SCl2+4H2O═2S↓+H2SO4+64HCl
③几种物质的熔沸点如表:
如图是实验室中通过向熔融的单质硫中通入少量Cl2制取S2Cl2的装置(部分夹持、加热装置已略去)
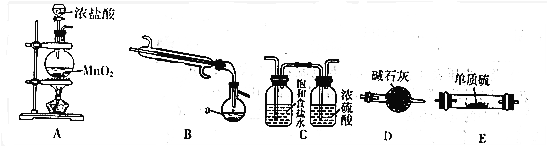
(1)B装置中仪器a的名称蒸馏烧瓶.
(2)装置的连接顺序是(每个装置只能使用一次)ACEBD.
(3)装置D的作用是防止空气中的水蒸气进入装置B,吸收多余的氯气.
(4)实验中先点燃A装置酒精灯制取Cl2时,当当E中充满黄绿色的气体时,说明排净空气,再点燃E处酒精灯.
(5)由实验粗产品获得纯净的S2Cl2,需要进行的操作是蒸馏,该操作的温度范围是59℃~137℃.
(6)请设计实验验证所得产品中是否含有杂质SCl2:取少量产品加入试管中,再加入适量蒸馏水,振荡、静置.取少量上层清夜,滴加氯化钡溶液,若有白色沉淀生成,证明有S2Cl2,否则无S2Cl2.
已知:①S2Cl2不稳定,进一步氧化可得SCl2
②S2Cl2和SCl2 都与水反应,2S2Cl2+2H2O═3S↓+SO2↑+4HCl,3SCl2+4H2O═2S↓+H2SO4+64HCl
③几种物质的熔沸点如表:
| 物质 | S | SCl2 | S2Cl2 |
| 沸点/℃ | 445 | 59 | 137 |
| 熔点/℃ | 113 | -122 | -77 |

(1)B装置中仪器a的名称蒸馏烧瓶.
(2)装置的连接顺序是(每个装置只能使用一次)ACEBD.
(3)装置D的作用是防止空气中的水蒸气进入装置B,吸收多余的氯气.
(4)实验中先点燃A装置酒精灯制取Cl2时,当当E中充满黄绿色的气体时,说明排净空气,再点燃E处酒精灯.
(5)由实验粗产品获得纯净的S2Cl2,需要进行的操作是蒸馏,该操作的温度范围是59℃~137℃.
(6)请设计实验验证所得产品中是否含有杂质SCl2:取少量产品加入试管中,再加入适量蒸馏水,振荡、静置.取少量上层清夜,滴加氯化钡溶液,若有白色沉淀生成,证明有S2Cl2,否则无S2Cl2.