题目内容
下列溶液中,c(Cl-)的大小顺序为 (用字母填写)
A.20mL 0.4mol/L AlCl3溶液
B.30mL 1.5mol/L KCl溶液
C.7.5mL 1mol/L MgCl2溶液
D.10mL 2mol/L NaCl溶液.
A.20mL 0.4mol/L AlCl3溶液
B.30mL 1.5mol/L KCl溶液
C.7.5mL 1mol/L MgCl2溶液
D.10mL 2mol/L NaCl溶液.
考点:物质的量浓度的相关计算
专题:
分析:离子的物质的量浓度与溶液的浓度和溶质的化学式有关,氯离子的浓度=溶液的浓度×化学式中氯离子个数,与溶液的体积无关.
解答:
解:A、20mL 0.4mol/L AlCl3溶液中氯离子的浓度为0.4mol/L×3=1.2mol/L;
B、30mL 1.5mol/L KCl溶液中氯离子的浓度为1.5mol/L×1=1.5mol/L;
C、7.5mL 1mol/L MgCl2溶液中氯离子的浓度为1mol/L×2=2mol/L;
D、10mL 2mol/L NaCl溶液中氯离子的浓度为2mol/L;
所以溶液中Cl-浓度由大到小的顺序是C=D>B>A,
故答案为:C=D>B>A.
B、30mL 1.5mol/L KCl溶液中氯离子的浓度为1.5mol/L×1=1.5mol/L;
C、7.5mL 1mol/L MgCl2溶液中氯离子的浓度为1mol/L×2=2mol/L;
D、10mL 2mol/L NaCl溶液中氯离子的浓度为2mol/L;
所以溶液中Cl-浓度由大到小的顺序是C=D>B>A,
故答案为:C=D>B>A.
点评:本题考查了溶液中离子浓度的计算,明确溶液中离子的浓度=溶液的浓度×化学式中离子个数是解本题的关键,难度不大.

练习册系列答案
 53天天练系列答案
53天天练系列答案
相关题目
下列溶液中各微粒的浓度关系不正确的是( )
| A、0.1 mol/LCH3COOH溶液中:c(CH3COO-)+c(CH3COOH)=0.1mol/L |
| B、CH3COONa溶液中:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
| C、Na2S溶液中:2 c(Na+)=c(S2-)+c(HS-)+c(H2S) |
| D、NaHCO3溶液中:c(OH-)=c(H+)+c(H2CO3)-c(CO32-) |
可逆反应A(g)+4B(g)?C(g)+D(g),在四种不同情况下的反应速率如下,其中表示反应进行得最快的是( )
| A、vA=0.15mol/(L?min) |
| B、vB=0.6 mol/(L?min) |
| C、vC=0.4 mol/(L?min) |
| D、vD=0.005 mol/(L?s) |
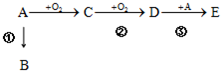
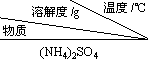
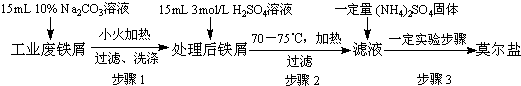

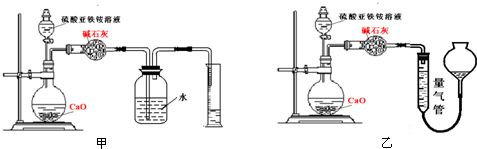
 阅读下表中的部分短周期主族元素的相关信息.
阅读下表中的部分短周期主族元素的相关信息.