题目内容
9.某研究小组进行Mg(OH)2沉淀溶解和生成的实验探究.实验如下: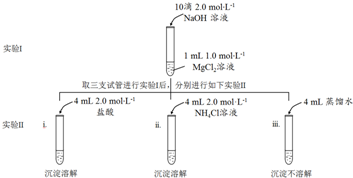
(1)实验I中发生反应的离子方程式是Mg2++2OH-═Mg(OH)2↓.
(2)比较2.0mol•L-1盐酸pH1和2.0mol•L-1 NH4Cl溶液pH2大小:pH1< pH2,原因是由于盐酸完全电离,NH4+部分水解:NH4++H2O?NH3•H2O+H+,导致同浓度两溶液中,盐酸中H+浓度大于NH4Cl溶液中H+浓度.
(3)用平衡移动原理解释i中沉淀溶解的原因:Mg(OH)2(s)?Mg2+(aq)+2OH-(aq),盐酸中的H+与OH-中和使得OH-浓度减小,
平衡右移,沉淀溶解.
(4)iii是i和ii的对比实验,目的是排除实验i、ii中溶剂水使沉淀溶解的可能性.
(5)推测ii中沉淀溶解的原因.
推测一,NH4Cl溶液显酸性,溶液中的H+可以结合OH-,进而使沉淀溶解;
推测二,溶液中c(NH4+)较大,NH4+结合OH-使沉淀溶解.
(6)为探究ii中沉淀溶解的原因,小组同学继续进行实验:
①取4mL2.0mol•L-1NH4Cl溶液,向其中滴加2滴浓氨水,得到pH为8的混合溶液,再向同样Mg(OH)2沉淀中加入该混合溶液,沉淀溶解.
②上述实验结果证明(5)中的推测二成立,理由是混合后溶液中c(H+)=10-8mol•L-1非常小,c(NH4+)=2.0mol•L-1较大,故能确定是NH4+结合OH-使沉淀溶解.
分析 (1)氢氧化钠与氯化镁反应生成氢氧化镁沉淀和氯化钠;
(2)氯化氢为强电解质完全电离,盐类水解是微弱的,据此分析解答;
(3)依据沉淀溶解平衡移动原理及影响因素解答;
(4)依据实验iii条件为加入蒸馏水判断解答;
(5)依据铵根离子能够水生成一水合氨和氢离子,铵根离子能够与氢氧根离子反应生成一水合氨的性质解答;
(6)向4mL 2mol•L-1 NH4Cl溶液中滴加2滴浓氨水,得到pH约为8的混合溶液,溶液呈碱性,如氢氧化镁能溶解,可说明NH4+结合OH-使沉淀溶解;
解答 解:(1)氢氧化钠与氯化镁反应生成氢氧化镁沉淀和氯化钠,离子方程式:Mg2++2OH-═Mg(OH)2↓;
故答案为:Mg2++2OH-═Mg(OH)2↓;
(2)由于盐酸中氯化氢为强电解质,完全电离,NH4+部分水解:NH4++H2O?NH3•H2O+H+,导致同浓度两溶液中,盐酸中H+浓度大于NH4Cl溶液中H+浓度,所以2.0mol•L-1盐酸pH1和2.0mol•L-1 NH4Cl溶液,盐酸中氢离子浓度大于氯化铵中氢离子浓度,所以pH1<pH2;
故答案为:<;由于盐酸完全电离,NH4+部分水解:NH4++H2O?NH3•H2O+H+,导致同浓度两溶液中,盐酸中H+浓度大于NH4Cl溶液中H+浓度
(3)氢氧化镁溶液中存储沉淀溶解平衡:Mg(OH)2(s)?Mg2+(aq)+2OH -(aq),加入盐酸后,盐酸中的H+与OH-中和使得OH-浓度减小,
平衡右移,沉淀溶解;
故答案为:Mg(OH)2(s)?Mg2+(aq)+2OH -(aq),盐酸中的H+与OH-中和使得OH-浓度减小,平衡右移,沉淀溶解;
(4)实验iii条件为只加蒸馏水,现象沉淀不溶解,可以排除实验i、ii中溶剂水使沉淀溶解的可能性;
故答案为:实验i、ii中溶剂水使沉淀溶解的可能性;
(5)铵根离子能够水生成一水合氨和氢离子,铵根离子能够与氢氧根离子反应生成一水合氨的性质,所以推测ii中沉淀溶解的原因:
推测一,NH4Cl溶液显酸性,溶液中的H+可以结合OH-,进而使沉淀溶解;推测二,溶液中c(NH4+)较大,NH4+结合OH-使沉淀溶解;
故答案为:溶液中c(NH4+)较大,NH4+结合OH-使沉淀溶解;
(6)向4mL 2mol•L-1 NH4Cl溶液中滴加2滴浓氨水,得到pH约为8的混合溶液,溶液呈碱性,如氢氧化镁能溶解,可说明NH4+结合OH-使沉淀溶解,配制理由:混合溶液显碱性,c(H+)非常小,c(NH4+)较大能确定是NH4+结合OH-使沉淀溶解,
故答案为:
①4 mL 2.0 mol•L-1 NH4Cl;
②二 理由:混合后溶液中c(H+)=10-8 mol•L-1非常小,c(NH4+)=2.0 mol•L-1较大,故能确定是NH4+结合OH-使沉淀溶解.
点评 本题考查较为综合,侧重于学生的分析能力和实验能力的考查,为高频考点,注意把握影响沉淀平衡,电离平衡和水解平衡的因素,综合把握相关基本理论知识,注重基础知识的学习,难度中等.

 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案| A. | 过滤时,玻璃棒的末端应轻轻靠在三层滤纸上 | |
| B. | 蒸馏时,应使温度计水银球靠近蒸馏烧瓶的支管口处 | |
| C. | 分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 | |
| D. | 称氢氧化钠时,不能直接称量,要放在纸片上称量 |
| A. | Fe(OH)3胶体区别于其他分散系的本质特征是分散质粒子的直径在10-9~10-7米之间 | |
| B. | 分别用一束光透过三种分散系,只有Fe(OH)3胶体具有丁达尔效应 | |
| C. | 往FeCl3溶液中加入NaOH溶液,并适当加热,可制得Fe(OH)3胶体 | |
| D. | 三种分散系中分散质均属于电解质 |
 某学生探究AgCl、Ag2S沉淀转化的原因.
某学生探究AgCl、Ag2S沉淀转化的原因.| 步 骤 | 现 象 |
| Ⅰ.将NaCl与AgNO3溶液混合 | 产生白色沉淀 |
| Ⅱ.向所得固液混合物中加Na2S溶液 | 沉淀变为黑色 |
| Ⅲ.滤出黑色沉淀,加入NaCl溶液 | 较长时间后,沉淀变为乳白色 |
(2)Ⅱ中能说明沉淀变黑的离子方程式是2AgCl(s)+S2-?Ag2S(s)+2Cl-,沉淀转化的主要原因是Ag2S比AgCl溶解度更小.
(3)滤出步骤Ⅲ中乳白色沉淀,推测含有AgCl.用浓HNO3溶解,产生红棕色气体,部分沉淀未溶解,过滤得到滤液X和白色沉淀Y.
ⅰ.向X中滴加Ba(NO3)2溶液,产生白色沉淀
ⅱ.向Y滴加KI溶液,产生黄色沉淀
①由ⅰ判断,滤液X中被检出的离子是SO42-.
②由ⅰ、ⅱ可确认步骤Ⅲ中乳白色沉淀含有AgCl和另一种沉淀S.
(4)该学生通过如下对照实验确认了步骤Ⅲ中乳白色沉淀产生的原因:在NaCl存在下,氧气将Ⅲ中黑色沉淀氧化.
| 现象 | B.一段时间后,出现白色沉淀 |
| C.一点时间后,无明显变化 |
②C中盛放的物质W是Ag2S的悬浊液.
③该同学认为B中产生沉淀的反应如下(请补充完整):
2Ag2S+1O2++4NaCl+2H2O?4AgCl+2S+4NaOH.
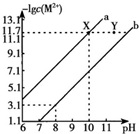 25℃时,Fe(OH)2和Cu(OH)2的饱和溶液中,金属阳离子的物质的量浓度的负对数[-lgC(M2+)]与溶液PH的变化关系如图所示,已知:该温度下,Ksp[Cu(OH)2]<Ksp[Fe(OH)2].下列说法正确的是( )
25℃时,Fe(OH)2和Cu(OH)2的饱和溶液中,金属阳离子的物质的量浓度的负对数[-lgC(M2+)]与溶液PH的变化关系如图所示,已知:该温度下,Ksp[Cu(OH)2]<Ksp[Fe(OH)2].下列说法正确的是( )| A. | b线表示Fe(OH)2饱和溶液中的变化关系,且Ksp[Fe(OH)2]=10-15.1 | |
| B. | 当Fe(OH)2和Cu(OH)2沉淀共存时,溶液中C(Fe2+):C(Cu2+)=1:104.6 | |
| C. | 向X点对应的饱和溶液中加入少量NaOH,可转化为Y点对应的溶液 | |
| D. | 除去CuSO4溶液中含有的少量Fe2+,可加入适量CuO |
(1)已知:H-H键能为436kJ•mol-1,N≡N键能为945kJ•mol-1,N-H键能为391kJ?mol-1.写出合成氨反应的热化学方程式N2(g)+3H2(g)?2NH3(g)△H=-93kJ•mol-1.
(2)恒温下,往一个2L的密闭容器中充入2.6mol H2和1mol N2,反应过程中对NH3的浓度进行检测,得到的数据如表所示:
| 时间/min | 5 | 10 | 15 | 20 | 25 | 30 |
| c(NH3)/mol•L-1 | 0.08 | 0.14 | 0.18 | 0.20 | 0.20 | 0.20 |
 (1)已知在2L的容器中进行下列可逆反应,各物质的有关数据如下:
(1)已知在2L的容器中进行下列可逆反应,各物质的有关数据如下:aA (g)+bB (g)?2C(g)
| 起始物质的量浓度(mol/L) | 1.5 | 1 | 0 |
| 2s末物质的量浓度(mol/L) | 0.9 | 0.8 | 0.4 |
②0到2s用物质B来表示的反应速率为0.1mol/(L•s);
③从反应开始到2s末,A的转化率为40%;
④下列事实能够说明上述反应在该条件下已经达到化学平衡状态的是BE.
A.vB(反应)=vC(生成) B.容器内气体的总压强保持不变
C.容器内气体的密度不变 D.vA:vB:vC=3:2:2
E.容器内气体C的物质的量分数保持不变
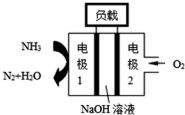
(2)①锌电池有望代替铅蓄电池,它的构成材料是锌、空气、某种电解质溶液,发生的总反应式是:2Zn+O2=2ZnO.则该电池的负极材料是锌;
②瑞典ASES公司设计的曾用于驱动潜艇的液氨-液氧燃料电池示意图如图,该燃料电池工作时,电池的总反应为4NH3+3O2=2N2+6H2O;负极的电极反应为2NH3-6e-+6OH-═N2+6H2O.