题目内容
16.关于金属钠单质及其化合物的说法中,不正确的是( )| A. | NaCl可用作食品调味剂 | |
| B. | 相同温度下NaHCO3溶解度大于Na2CO3 | |
| C. | Na2CO3的焰色反应呈黄色 | |
| D. | 工业上Na可用于制备钛、锆等金属 |
分析 A.NaCl具有咸味;
B.相同温度下,碳酸钠的溶解度大于碳酸氢钠;
C.钠元素的焰色反应呈现黄色;
D.钠性质活泼,具有较强的还原性.
解答 解:A.NaCl具有咸味,可用作食品调味剂,故A正确;
B.相同温度下,NaHCO3溶解度小于Na2CO3,故B错误;
C.钠元素的焰色反应呈现黄色,Na2CO3中含有钠元素,因此焰色反应呈黄色,故C正确;
D.钠性质活泼,具有较强的还原性,可用于冶炼金属钛、锆、铌等,故D正确;
故选B.
点评 本题考查了元素化合物知识,明确相关物质的性质及用途是解题关键,题目难度不大,有利于培养学生良好的科学素养,提高学习的积极性.

练习册系列答案
相关题目
6.将Na投入FeCl3溶液中,可观察到的现象是( )
| A. | 生成白色沉淀、有气泡产生 | B. | 生成红褐色沉淀、有气泡产生 | ||
| C. | 生成黑色沉淀,有气泡产生 | D. | 无明显现象 |
7.化学在生产和生活中有着重要的作用,下列有关说法正确的是( )
| A. | 汽车尾气污染物中含有氮的氧化物,是汽油不完全燃烧造成的 | |
| B. | 含磷污水是很好的肥料,可灌溉庄稼,能直接排放到自然界水体中 | |
| C. | 施用适量石灰乳可降低盐碱地(含较多NaCl、Na2CO3)的碱性 | |
| D. | 最理想的“原子经济”就是原子利用率为100% |
4.下列有关实验原理或操作正确的是( )
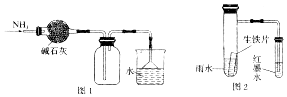

| A. | 图1所示的装置可用于干燥、收集并吸收多余的氨气 | |
| B. | 用广泛pH试纸测得0.1mol•L-1NaClO溶液的pH值约为12 | |
| C. | 用蒸发溶剂的方法将10%的Ca(HCO3)2溶液变为20%的Ca(HCO3)2溶液 | |
| D. | 用图2的装置可以验证生铁片在该雨水中是否会发生吸氧腐蚀 |
11.下列说法不正确的是( )
| A. | 煤和石油燃烧不完全时可排放出大量烟尘和CO | |
| B. | 化石燃料燃烧排出废气中含SO2,直接排到大气中会污染空气并形成酸雨 | |
| C. | 可通过物理方法把化石燃料转化为洁净燃料 | |
| D. | 氢能、核能、太阳能等都属于洁净、高效的新能源 |
1.设NA为阿伏加德罗常数的值,下列说法不正确的是( )
| A. | 10g质量分数为46%的乙醇水溶液中所含原子数目为0.6NA | |
| B. | 常温常压下,11.2L乙烯所含分子数目小于0.5NA | |
| C. | 常温常压下.4.4gN2O与CO2的混合气体中含的原子数目为0.3NA | |
| D. | 常温下,1molC5H12中含有共价键数为16NA |
8.下列关于有机化合物的说法正确的是( )
| A. | 乙醇的结构简式为C2H6O | |
| B. | C3H6Cl2有5种同分异构体 | |
| C. | 乙酸溶于水可以电离,属于离子化合物 | |
| D. | 由苯乙烯生成聚苯乙烯塑料属于加聚反应 |
5.钴及其化合物可应用与催化剂、电池、颜料与染料等.
(1)CoO是一种油漆添加剂,可通过反应①②制备.
①2Co(s)+O2(g)═2CoO(s)△H1=akJ•mol-1
②2CoCO3(s)═CoO(s)+CO2 (g)△H2=akJ•mol-1
则反应2Co(s)+O2(g)+2CO2(g)═2CoO3(s) 的△H=(a-2b)kJ•mol-1
(2)某锂电池的电解质可传导Li+,电池反应式为:LiC6+CoO2?C6+LiCoO2
①电池放电时,负极的电极反应式为,Li+向正极移动(填“正极”或“负极“).
②一种回收电极中Co元素的方法是:将LiCoO2与H2O2、H2SO4反应生成CoSO4.该反应的化学方程式为2LiCoO2+H2O2+3H2SO4═Li2SO4+2CoSO4+4H2O+O2↑
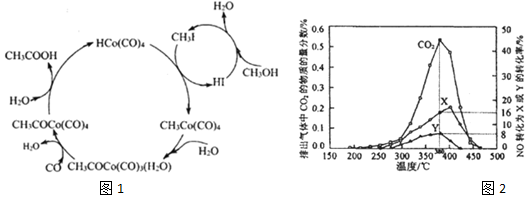
(3)BASF高压法制备醋酸采用钴碘催化循环过程如图1所示,该循环的总反应方程式为CO+CH3OH→CH3COOH(反应条件无需列出)
(4)某含钴催化剂可同时催化去除柴油车尾气中的碳烟(C)和NOx.不同温度下,将10mol模拟尾气(成分如图2所示)以相同的流速通过该催化剂,测得所有产物(CO2、N2、N2O)与NO的相关数据结果如表
①380℃时,测得排出的气体中含0.45 mol O2和0.0525 mol CO2,则Y的化学式为N2O.
②实验过程中采用NO模拟NOx,而不采用NO2的原因是NO较NO2稳定,NO2气体中存在N2O4,不便于定量测定.

(1)CoO是一种油漆添加剂,可通过反应①②制备.
①2Co(s)+O2(g)═2CoO(s)△H1=akJ•mol-1
②2CoCO3(s)═CoO(s)+CO2 (g)△H2=akJ•mol-1
则反应2Co(s)+O2(g)+2CO2(g)═2CoO3(s) 的△H=(a-2b)kJ•mol-1
(2)某锂电池的电解质可传导Li+,电池反应式为:LiC6+CoO2?C6+LiCoO2
①电池放电时,负极的电极反应式为,Li+向正极移动(填“正极”或“负极“).
②一种回收电极中Co元素的方法是:将LiCoO2与H2O2、H2SO4反应生成CoSO4.该反应的化学方程式为2LiCoO2+H2O2+3H2SO4═Li2SO4+2CoSO4+4H2O+O2↑
(3)BASF高压法制备醋酸采用钴碘催化循环过程如图1所示,该循环的总反应方程式为CO+CH3OH→CH3COOH(反应条件无需列出)
(4)某含钴催化剂可同时催化去除柴油车尾气中的碳烟(C)和NOx.不同温度下,将10mol模拟尾气(成分如图2所示)以相同的流速通过该催化剂,测得所有产物(CO2、N2、N2O)与NO的相关数据结果如表
| 模拟尾气 | 气体 | 碳烟 | ||
| NO | O2 | He | ||
| 物质的量分数或物质的量 | 0.25% | 5% | 94.75% | a mol |
②实验过程中采用NO模拟NOx,而不采用NO2的原因是NO较NO2稳定,NO2气体中存在N2O4,不便于定量测定.