题目内容
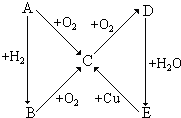 根据如图所示的A、B、C、D、E五种物质的相互转化关系,按如下要求填写相应的物质的化学式和有关反应的化学方程式.
根据如图所示的A、B、C、D、E五种物质的相互转化关系,按如下要求填写相应的物质的化学式和有关反应的化学方程式.当A是空气中含量最多的气体单质时,
A是
写出有关反应的化学方程式:
A→B:
A→C:
B→C:
C→D:
考点:无机物的推断,含氮物质的综合应用
专题:氮族元素
分析:当A是空气中含量最多的气体单质时,判断为N2,A能与氧气、氢气反应,且B能发生连续氧化反应,则证明A为N2,B为NH3,C为NO,D为NO2,E为HNO3;依据推断物质书写化学方程式;
解答:
解:当A是空气中含量最多的气体单质时,判断为N2,A能与氧气、氢气反应,且B能发生连续氧化反应,则证明A为N2,B为NH3,C为NO,D为NO2,E为HNO3;
(1)当A是空气中含量最多的气体单质时,判断为N2,A能与氧气、氢气反应,且B能发生连续氧化反应,则A为N2,B为NH3,C为NO,D为NO2,E为稀HNO3;
故答案为:N2,NH3,NO,NO2,HNO3;
(2)有关反应的化学方程式:
A-B是氮气和氢气 氨气反应的化学方程式为:N2+3H2
2NH3;
A-C是氮气和氧气反应生成无色气体一氧化氮,反应的化学方程式为:N2+O2
2NO;
B-C是氨气的催化氧化反应生成一氧化氮和水,反应的化学方程式为:4NH3+5O2
4NO+6H2O;
C-D是一氧化氮和氧气 反应生成红棕色气体二氧化氮,反应的化学方程式2NO+O2=2NO2;
故答案为:N2+3H2
2NH3;N2+O2
2NO;4NH3+5O2
4NO+6H2O;2NO+O2=2NO2;
(1)当A是空气中含量最多的气体单质时,判断为N2,A能与氧气、氢气反应,且B能发生连续氧化反应,则A为N2,B为NH3,C为NO,D为NO2,E为稀HNO3;
故答案为:N2,NH3,NO,NO2,HNO3;
(2)有关反应的化学方程式:
A-B是氮气和氢气 氨气反应的化学方程式为:N2+3H2
| ||
| 高温高压 |
A-C是氮气和氧气反应生成无色气体一氧化氮,反应的化学方程式为:N2+O2
| ||
B-C是氨气的催化氧化反应生成一氧化氮和水,反应的化学方程式为:4NH3+5O2
| ||
| △ |
C-D是一氧化氮和氧气 反应生成红棕色气体二氧化氮,反应的化学方程式2NO+O2=2NO2;
故答案为:N2+3H2
| ||
| 高温高压 |
| ||
| ||
| △ |
点评:本题考查无机物的推断,注意A是空气中含量最多的气体单质及B能发生连续氧化为解答本题的突破口,熟悉N的单质及化合物的性质是解答的关键,题目难度中等.

练习册系列答案
 智慧小复习系列答案
智慧小复习系列答案
相关题目
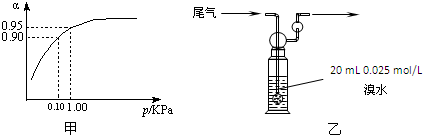
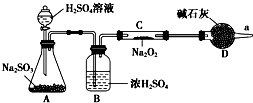 ①某学生根据SO2具有还原性判断SO2和Na2O2反应能生成硫酸钠,该同学无法断定反应中是否有氧气生成,拟使用如图所示装置进行实验(A为SO2的发生装置,图中铁架台等装置已略去).
①某学生根据SO2具有还原性判断SO2和Na2O2反应能生成硫酸钠,该同学无法断定反应中是否有氧气生成,拟使用如图所示装置进行实验(A为SO2的发生装置,图中铁架台等装置已略去).