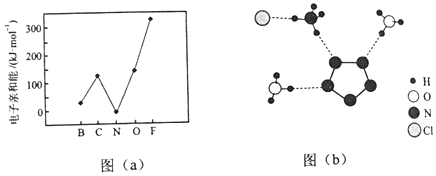
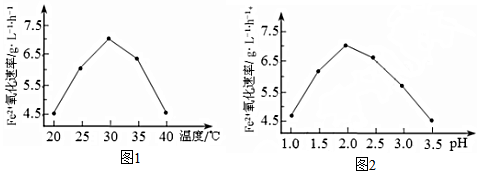
��Ŀ����
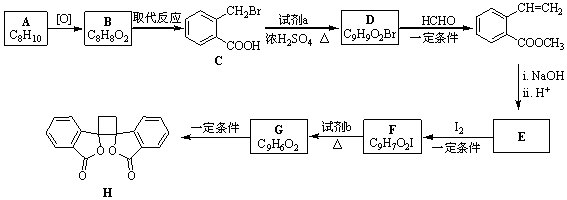
13��������H��һ���л��������м��壮ʵ�����ɷ��㻯����A�Ʊ�H��һ�ֺϳ�·�����£�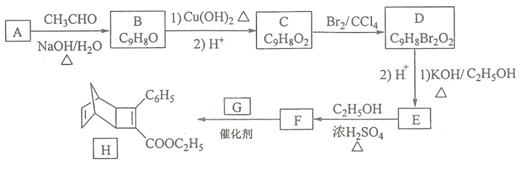
��֪����RCHO+CH3CHO$��_{��}^{NaOH/H_{2}O}$RCH=CHCHO+H2O
��
 +
+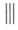 $\stackrel{����}{��}$
$\stackrel{����}{��}$
�ش��������⣺
��1��A�Ļ�ѧ����ΪΪ����ȩ��
��2����C����D��E����F�ķ�Ӧ���ͷֱ�Ϊ�ӳɷ�Ӧ��ȡ����Ӧ��
��3��E�Ľṹ��ʽΪ
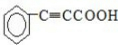 ��
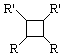
����4��GΪ�ױ���ͬ���칹�壬��F����H�Ļ�ѧ����ʽΪ
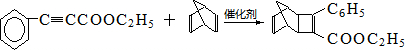 ��
����5�����㻯����X��F��ͬ���칹�壬X���뱥��̼��������Һ��Ӧ�ų�CO2����˴Ź���������ʾ��4�ֲ�ͬ��ѧ�������⣬�������Ϊ6��2��1��1��д��2�ַ���Ҫ���X�Ľṹ��ʽ
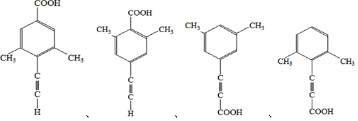 ��
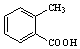
����6��д���û������2-��ȲΪԭ���Ʊ�������
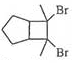 �ĺϳ�·��
�ĺϳ�·��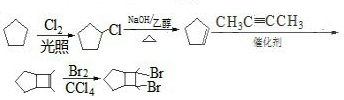 �������Լ���ѡ����
�������Լ���ѡ����
���� ����Ϣ�ٿ�֪AӦ����ȩ�����Һ���7��Cԭ�ӣ�ӦΪ ����BΪ
����BΪ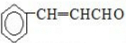 ����CΪ
����CΪ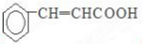 ��DΪ
��DΪ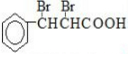 ��EΪ
��EΪ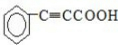 �����Ҵ�����������Ӧ����FΪ
�����Ҵ�����������Ӧ����FΪ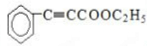 ���Ա�F��H�Ľṹ��ʽ��֪GΪ
���Ա�F��H�Ľṹ��ʽ��֪GΪ ���Դ˽��1������4����
���Դ˽��1������4����
��5��FΪ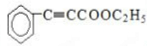 �����㻯����X��F��ͬ���칹�壬X���뱥��̼��������Һ��Ӧ�ų�CO2��˵�������Ȼ�����˴Ź���������ʾ��4�ֲ�ͬ��ѧ�������⣬�������Ϊ6��2��1��1���������Ӧ����2��������Ϊ�Գƽṹ��
�����㻯����X��F��ͬ���칹�壬X���뱥��̼��������Һ��Ӧ�ų�CO2��˵�������Ȼ�����˴Ź���������ʾ��4�ֲ�ͬ��ѧ�������⣬�������Ϊ6��2��1��1���������Ӧ����2��������Ϊ�Գƽṹ��
��6���������2-��ȲΪԭ���Ʊ������� ��������Ӧ�����ɻ���ϩ��Ȼ����2-��Ȳ�����ӳɷ�Ӧ����
��������Ӧ�����ɻ���ϩ��Ȼ����2-��Ȳ�����ӳɷ�Ӧ����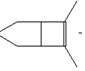 ��������巢���ӳɿ�����
��������巢���ӳɿ����� ���Դ˽����⣮
���Դ˽����⣮
��� �⣺��1�������Ϸ�����֪AΪ����ȩ���ʴ�Ϊ������ȩ��
��2��CΪ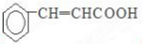 �������ӳɷ�Ӧ����
�������ӳɷ�Ӧ����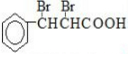 ��EΪ
��EΪ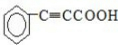 �����Ҵ�����������Ӧ����F��ҲΪȡ����Ӧ���ʴ�Ϊ���ӳɷ�Ӧ��ȡ����Ӧ��
�����Ҵ�����������Ӧ����F��ҲΪȡ����Ӧ���ʴ�Ϊ���ӳɷ�Ӧ��ȡ����Ӧ��
��3�������Ϸ�����֪EΪ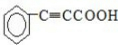 ���ʴ�Ϊ��
���ʴ�Ϊ��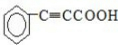 ��
��
��4��GΪ ��FΪ
��FΪ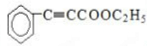 �����߷����ӳɷ�Ӧ����H����Ӧ�ķ���ʽΪ
�����߷����ӳɷ�Ӧ����H����Ӧ�ķ���ʽΪ ��
��
�ʴ�Ϊ�� ��
��
��5��FΪ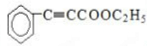 �����㻯����X��F��ͬ���칹�壬X���뱥��̼��������Һ��Ӧ�ų�CO2��˵�������Ȼ�����˴Ź���������ʾ��4�ֲ�ͬ��ѧ�������⣬�������Ϊ6��2��1��1���������Ӧ����2��������Ϊ�Գƽṹ�����ܽṹ��
�����㻯����X��F��ͬ���칹�壬X���뱥��̼��������Һ��Ӧ�ų�CO2��˵�������Ȼ�����˴Ź���������ʾ��4�ֲ�ͬ��ѧ�������⣬�������Ϊ6��2��1��1���������Ӧ����2��������Ϊ�Գƽṹ�����ܽṹ�� ��
��
�ʴ�Ϊ�� ��
��
��6���������2-��ȲΪԭ���Ʊ������� ��������Ӧ�����ɻ���ϩ��Ȼ����2-��Ȳ�����ӳɷ�Ӧ����
��������Ӧ�����ɻ���ϩ��Ȼ����2-��Ȳ�����ӳɷ�Ӧ���� ��������巢���ӳɿ�����
��������巢���ӳɿ����� ���ڷ�Ӧ������Ϊ
���ڷ�Ӧ������Ϊ ��
��
�ʴ�Ϊ�� ��
��
���� ����Ϊ2017�꿼�⣬�����л����ƶϺͺϳɣ�Ϊ��Ƶ���㣬���ؿ���ѧ�������ж���������ȷ�����ż������ʹ�ϵ��������Ӧ���ͼ���Ӧ�����ǽⱾ��ؼ���ע�������Ϣ��������ã���Ŀ�ѶȲ���

| A�� | 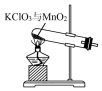 ��ȡ���� | B�� | 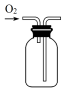 �ռ����� | C�� | 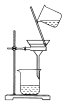 �����MnO2 | D�� |  �����ᾧ��KCl |

���ϣ�TiCl4�����������Ȼ��������
| ������ | SiCl4 | TiCl4 | AlCl3 | FeCl3 | MgCl2 |
| �е�/�� | 58 | 136 | 181�������� | 316 | 1412 |
| �۵�/�� | -69 | 25 | 193 | 304 | 714 |
| ��TiCl4�е��ܽ��� | ���� | - | �� | ���� | |
��֪��TiO2��s��+2Cl2��g��=TiCl4��g��+O2��g����H1=+175.4kJ•mol-1
2C��s��+O2��g��=2CO��g����H2=-220.9kJ•mol-1
�ٷ���¯�м�̼�Ȼ�����TiCl4��g����CO��g�����Ȼ�ѧ����ʽ��TiO2��s��+2Cl2��g��+2C��s��=TiCl4��g��+2CO��g����H=-45.5kJ•mol-1��
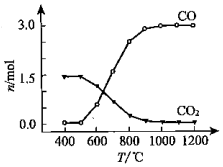
���Ȼ�������CO��CO2�����ת����������ͼ�жϣ�CO2����CO��Ӧ�ġ�H��0���������������=�������ж����ݣ��¶�Խ�ߣ�CO�����ʵ���Խ���CO2�����ʵ����٣�˵��CO2����CO�ķ�Ӧ�����ȷ�Ӧ��
���Ȼ���Ӧ��β���봦�����ŷţ�β���е�HCl��Cl2�����տɵô����ᡢFeCl3��Һ����β��������Һ�����DZ���ʳ��ˮ���Ȼ�������Һ��
���Ȼ�������ȴ�����£������˵õ���TiCl4���Һ���������к���TiO2��C��
��2�����ƹ��̣���TiCl4����������ô�TiCl4��ʾ��ͼ���£�
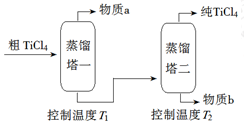
����a��SiCl4��T2Ӧ������136�����ң�
| A�� | ��ɫ������Һ�У�Fe3+��Mg2+��SCN -��Cl - | |
| B�� | c��H+��/c��OH-��=1��10 -12����Һ�У�K+��Na+��CO32-��NO3- | |
| C�� | c��Fe2+ ��=1 mol•L-1����Һ�У�K+��NH4+��MnO4-��SO42- | |
| D�� | ��ʹ���ȱ�����Һ�У�Na+��NH4+��SO42-��HCO3- |
| A | B | C | D |
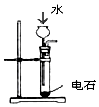 |  | 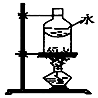 |  |
| ����Ȳ�ķ���װ�� | ����ʱ�Ľ���װ�� | ��������Ȼ��ƺ͵ⵥ�� | ȷ��ȡһ�����K2Cr2O7����Һ |
| A�� | A | B�� | B | C�� | C | D�� | D |
| A�� | ��ϩ������ͼ״� | B�� | �������ױ��ͺ������ˮ�� | ||
| C�� | ����غ��Ȼ��� | D�� | �Ȼ�狀�̼��� |
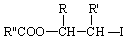
 ��
��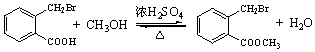 ��
�� ���˷�Ӧͬʱ��������һ���л�����������F��Ϊͬ���칹�壬���л�������Ľṹ��ʽ��
���˷�Ӧͬʱ��������һ���л�����������F��Ϊͬ���칹�壬���л�������Ľṹ��ʽ��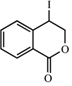 ��
��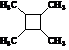 ·�ߣ��ýṹ��ʽ��ʾ�л���ü�ͷ��ʾת����ϵ����ͷ��ע���Լ��ͷ�Ӧ��������
·�ߣ��ýṹ��ʽ��ʾ�л���ü�ͷ��ʾת����ϵ����ͷ��ע���Լ��ͷ�Ӧ�������� ��
��