题目内容
3.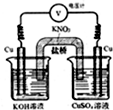 实验室利用如图所示装置.通过测电压求算Cu(OH)2的沉淀溶解平衡常数,工作一段时间后,两电极质量均增大.下列说法不正确的是( )
实验室利用如图所示装置.通过测电压求算Cu(OH)2的沉淀溶解平衡常数,工作一段时间后,两电极质量均增大.下列说法不正确的是( )| A. | 该装置工作时化学能转化为电能 | B. | 左池中的铜电极作正极 | ||
| C. | 总反应为Cu2+(aq)+2OH-(aq)?Cu(OH)2(s) | D. | 盐桥中的K+移向CuSO4溶液 |
分析 A、该装置是原电池;
B、左池铜失电子,生成铜离子;
C、左边的铜失电子生成铜离子,与电解质溶液中的氢氧根离子结合生成氢氧化铜,右边电解质溶液中的铜离子得电子生成单质铜;
D、电解池中的阳离子向正极移动.
解答 解:A、该装置是原电池,是将化学能转化为电能的装置,故A正确;
B、左池铜失电子,生成铜离子,发生氧化反应,所以左池中的铜电极作负极,故B错误;
C、左边的铜失电子生成铜离子,与电解质溶液中的氢氧根离子结合生成氢氧化铜,右边电解质溶液中的铜离子得电子生成单质铜,所以总反应为Cu2+(aq)+2OH-(aq)?Cu(OH)2(s),故C正确;
D、电解池中的阳离子向正极移动,所以盐桥中的K+向CuSO4溶液移动,故D正确;
故选B.
点评 本题考查了电化学中原电池的工作原理,明确正负极上发生的电极反应及离子的移动方向即可解答,比较容易.

练习册系列答案
相关题目
14.下列说法不正确的是( )
| A. | C5H12有三种不同的结构,其中一种同分异构体的名称是2,2-二甲基丙烷 | |
| B. | 聚乙烯(PE)和聚氯乙烯(PVC)的单体都是不饱和烃,均能使溴水褪色 | |
| C. | 用新制的Cu(OH)2悬浊液可以鉴别乙酸、乙醇和葡萄糖 | |
| D. | 不同条件下,乙稀可与氧气反应生成乙醛、乙酸、环氧乙烷(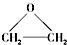 ),这些反应都属于氧化反应 ),这些反应都属于氧化反应 |
11.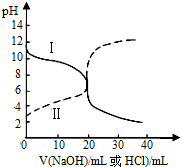 25℃时,取浓度均为0.1mol•L-1的醋酸溶液和氨水溶液各20mL,分别用0.1mol•L-1NaOH溶液、0.1mol•L-1盐酸进行中和滴定,滴定过程中pH随滴加溶液的体积变化关系如图所示.下列说法正确的是( )
25℃时,取浓度均为0.1mol•L-1的醋酸溶液和氨水溶液各20mL,分别用0.1mol•L-1NaOH溶液、0.1mol•L-1盐酸进行中和滴定,滴定过程中pH随滴加溶液的体积变化关系如图所示.下列说法正确的是( )
 25℃时,取浓度均为0.1mol•L-1的醋酸溶液和氨水溶液各20mL,分别用0.1mol•L-1NaOH溶液、0.1mol•L-1盐酸进行中和滴定,滴定过程中pH随滴加溶液的体积变化关系如图所示.下列说法正确的是( )
25℃时,取浓度均为0.1mol•L-1的醋酸溶液和氨水溶液各20mL,分别用0.1mol•L-1NaOH溶液、0.1mol•L-1盐酸进行中和滴定,滴定过程中pH随滴加溶液的体积变化关系如图所示.下列说法正确的是( )| A. | 曲线Ⅰ:滴加溶液到10 mL时:c(NH4+)>c(NH3•H2O)>c(Cl-)>c(OH-)>c(H+) | |
| B. | 曲线Ⅱ:滴加溶液到20 mL时:2c(CH3COO-)+c(CH3COOH)+c(OH-)═2c(Na+)+c(H+) | |
| C. | 根据滴定曲线,可得Kb(NH3•H2O)≈10-13 | |
| D. | 由曲线Ⅱ可知,选用酚酞和选用甲基橙作指示剂,消耗NaOH溶液的体积相同 |
18.将一定量的SO2通人BaCl2溶液中,无沉淀产生,若再通入a气体,则产生沉淀.下列所通a气体和产生沉淀的离子方程式正确的是( )
| A. | a为H2S,SO2+2H++S2-→3 S↓十2H2O | |
| B. | a为Cl2,Ba2++SO2+2 H2O+Cl2→BaSO3↓+4H++2Cl- | |
| C. | a为NO2,4Ba2++4SO2+5H2O+NO3-→4 BaSO4↓+NH4++6 H+ | |
| D. | a为NH3,Ba2++SO2+2 NH3+2H2O→BaSO4↓+2NH4++2H+ |
8.根据下列操作、现象,所得结论正确的是( )
| 选项 | 操作 | 现象 | 结论 |
| A | 向25mL冷水和沸水中分别滴入5滴FeCl3饱和溶液 | 前者为黄色. 后者为红褐色 | 温度升高,Fe3+的水解 程度增大 |
| B | NaOH的乙醇溶液与溴乙烷共热,产生的气体通入 酸性高锰酸钾溶液中 | 溶液褪色 | 产生的气体为乙烯 |
| C | 铜铝合金加入一定量稀硝酸中,有金属剩余,再加稀硫酸 | 剩余金属质量减小 | 铝与稀硫酸反应使 剩余金属质量减小 |
| D | 盛有NO2的集气瓶中加入一定量水 | 气体变为无色 | NO2是酸性氧化物 |
| A. | A | B. | B | C. | C | D. | D |
15.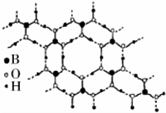 正硼酸(H3B03)是一种片层状结构的白色晶体,层内的H3BO3分子通过氢键相连(层状结构如图所示,图中“虚线”表示氢键).下列有关说法正确的是( )
正硼酸(H3B03)是一种片层状结构的白色晶体,层内的H3BO3分子通过氢键相连(层状结构如图所示,图中“虚线”表示氢键).下列有关说法正确的是( )
 正硼酸(H3B03)是一种片层状结构的白色晶体,层内的H3BO3分子通过氢键相连(层状结构如图所示,图中“虚线”表示氢键).下列有关说法正确的是( )
正硼酸(H3B03)是一种片层状结构的白色晶体,层内的H3BO3分子通过氢键相连(层状结构如图所示,图中“虚线”表示氢键).下列有关说法正确的是( )| A. | H3BO3分子的稳定性与氢键有关 | |
| B. | 含1mol H3BO3的晶体中有3mol氢键 | |
| C. | 分子中B、O最外层为8e-稳定结构 | |
| D. | 同层分子间的主要作用力是范德华力 |
12.PM2.5是指大气中直径小于或等于2.5微米的颗粒物,会导致雾霾天气.它主要来自化石燃料的燃烧.下列说法错误的是( )
| A. | 开发风能等洁净能源,减少使用化石燃料 | |
| B. | PM2.5表面积较大易吸附其他物质,对人体危害很大 | |
| C. | 雾霾严重时,中小学生应减少或停止户外活动 | |
| D. | 汽油标准由“国Ⅳ”提到“国 V”后,汽车不再排放氮氧化物 |
13.如图为立方烷的结构简式,其二氯代物有( )
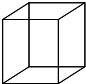

| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
 .
.