题目内容
10.某工厂的工业废水中含有大量的FeSO4、较多的Cu2+和少量的Na+.为了减少污染并变废为宝,工厂计划从该废水中回收硫酸亚铁和金属铜.简单的实验方案流程图如下,方框和括号内是所需用的物质A~F或操作方法Ⅰ~Ⅲ: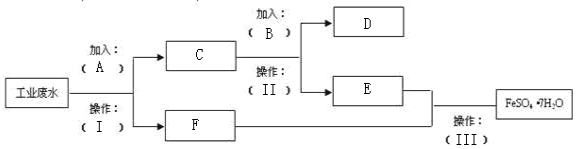
则物质A和操作Ⅱ分别为D
A.NaOH 过滤; B.Cu 蒸馏; C.Fe 萃取; D.Fe 过滤.
分析 某工厂的工业废水中含有大量的FeSO4、较多的Cu2+和少量的Na+,先加过量铁(A),过滤,得到F溶液为FeSO4,C为Cu和多余的铁,再向C中加过量稀硫酸,过滤得到的D为Cu,E为FeSO4,以此解答该题.
解答 解:某工厂的工业废水中含有大量的FeSO4、较多的Cu2+和少量的Na+,先加过量铁(A),过滤,得到F溶液为FeSO4,C为Cu和多余的铁,再向C中加过量稀硫酸,过滤得到的D为Cu,E为FeSO4,由此可知A为铁,操作Ⅱ为过滤,用于分离固体和溶液,
故答案为:D.
点评 本题考查了工艺流程图的分析判断,解答本题要充分理解各种物质的性质,从而得出正确的结论,应熟悉混合物的分离方法,掌握过滤和蒸发结晶分离方法的使用条件及实验操作,题目难度中等.

练习册系列答案
 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案
相关题目
20.下列各组离子中,在给定条件下能够大量共存的是( )
| A. | c(H+)/c(OH-)=1012的溶液中:NH4+、Al3+、NO3-、Cl- | |
| B. | 无色溶液中:Mg2+、MnO4-、SO42-、K+ | |
| C. | 酸性溶液中可能大量存在Na+、ClO?、SO42?、I? | |
| D. | 通入足量CO2后的溶液中:Na+、SiO32-、CH3COO-、CO32- |
1.下列事实中不能用平衡移动原理解释是( )
| A. | 密闭、低温是存放氨水的必要条件 | |
| B. | 实验室常用排饱和食盐水法收集氯气 | |
| C. | 打开汽水瓶时,有大量气泡冒出 | |
| D. | 已知合成氨的反应为N2(g)+3H2(g)?2NH3(g)△H=-92.4 kJ/mol,工业上采用较高温度和使用催化剂以提高氨气的产率 |
18.下列各组物质中,互为同分异构体的是( )
| A. | 葡萄糖和果糖 | B. | 淀粉和纤维素 | C. | 核糖和脱氧核糖 | D. | 丙氨酸、甘氨酸 |
5.下列叙述不正确的是( )
| A. | 雾是气溶胶,在阳光下可观察到丁达尔效应 | |
| B. | 预制备Fe(OH)3胶体,向盛有沸水的烧杯中加入FeCl3饱和溶液煮沸得红褐色沉淀 | |
| C. | 用石膏或卤水点制豆腐利用了胶体的性质 | |
| D. | 用鸡蛋壳膜和蒸馏水除去淀粉胶体中的食盐 |
15.下列实验操作和数据记录都正确的是( )
| A. | 用25mL碱式滴定管量取高锰酸钾溶液,体积为16.60mL | |
| B. | 用标准NaOH溶液滴定未知浓度盐酸,用去NaOH溶液20.50mL | |
| C. | 用10mL量筒量取8.25mL盐酸 | |
| D. | 用普通pH试纸测得某溶液pH为3.2 |
2.在溶液中能大量共存,加入OH-有沉淀产生,加入H+有气体放出的是( )
| A. | Na+、Cu2+、Cl-、SO42- | B. | Fe3+、K+、SO42-、NO3- | ||
| C. | H+、Mg2+、OH-、NO3- | D. | Na+、Ca2+、Cl-、HCO3- |
7.氨是生产硝酸、尿素等物质的重要原料,工业合成氨是最重要的化工生产之一.
(1)氨催化氧化法是工业制硝酸的主要方法.已知:2NO(g)+3H2(g)?2NH3(g)+O2(g)△H1=-272.9 kJ•mol-1,2H2(g)+O2(g)═2H2O(g)△H2=-483.6kJ•mol-1,则4NH3(g)+5O2(g)=4NO(g)+6H2O(g)△H3=-905.0 kJ/mol.
(2)恒容密闭容器中进行合成氨反应N2(g)+3H2(g)?2NH3(g)△H4=-92.4 kJ•mol-1,其化学平衡常数(K)与温度的关系如表:
K1> (填“>”或“<”)K2,其判断理由是反应是放热反应,温度升高,平衡逆向进行,平衡常数减小.
(3)向氨合成塔中充入10molN2和40mol H2进行氨的合成,一定温度(T)下平衡混合物中氨气的体积分数与压强(p)的关系如图1所示.下列说法正确的是AB(填字母).
A.由图1可知增大体系压强(p),有利于增大氨气在混合气体中的体积分数
B.若图1中T=500℃,则温度为450℃时对应的曲线是b
C.工业上采用500℃温度可有效提高氮气的转化率
D.当3v正(H2)=2v逆(NH3)时,反应达到平衡状态
当温度为T、氨气的体积分数为25%时,N2的转化率为50%.
(4)电化学法是合成氨的一种新方法,其原理如图2所示,通入H2的一极为阳极(填“阴极”或“阳极”),阴极得电极反应式是N2+6H++6e-=2NH3.
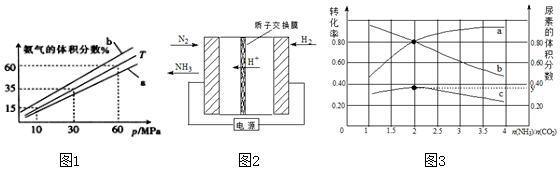
(5)氨碳比[$\frac{n(N{H}_{3})}{C{O}_{2}}$]对合成尿素的反应:2NH3(g)+CO2(g)?CO(NH2)2(g)+H2O(g)有影响,T℃时,在一体积为2L地 恒容密闭容器中,将物质的量之和为3mol的NH3和CO2以不同的氨碳比进行反应,结果如图3所示,a,b分别表示CO2或NH3的转化率,c表示平衡体系中尿素的体积分数,$\frac{n(N{H}_{3})}{C{O}_{2}}$=2时,尿素的产量最大;该条件下反应的平衡常数K=40.
(1)氨催化氧化法是工业制硝酸的主要方法.已知:2NO(g)+3H2(g)?2NH3(g)+O2(g)△H1=-272.9 kJ•mol-1,2H2(g)+O2(g)═2H2O(g)△H2=-483.6kJ•mol-1,则4NH3(g)+5O2(g)=4NO(g)+6H2O(g)△H3=-905.0 kJ/mol.
(2)恒容密闭容器中进行合成氨反应N2(g)+3H2(g)?2NH3(g)△H4=-92.4 kJ•mol-1,其化学平衡常数(K)与温度的关系如表:
温度/K | 298 | 398 | 498 | … |
| 平衡常数(K) | 4.1×105 | K1 | K2 | … |
(3)向氨合成塔中充入10molN2和40mol H2进行氨的合成,一定温度(T)下平衡混合物中氨气的体积分数与压强(p)的关系如图1所示.下列说法正确的是AB(填字母).
A.由图1可知增大体系压强(p),有利于增大氨气在混合气体中的体积分数
B.若图1中T=500℃,则温度为450℃时对应的曲线是b
C.工业上采用500℃温度可有效提高氮气的转化率
D.当3v正(H2)=2v逆(NH3)时,反应达到平衡状态
当温度为T、氨气的体积分数为25%时,N2的转化率为50%.
(4)电化学法是合成氨的一种新方法,其原理如图2所示,通入H2的一极为阳极(填“阴极”或“阳极”),阴极得电极反应式是N2+6H++6e-=2NH3.

(5)氨碳比[$\frac{n(N{H}_{3})}{C{O}_{2}}$]对合成尿素的反应:2NH3(g)+CO2(g)?CO(NH2)2(g)+H2O(g)有影响,T℃时,在一体积为2L地 恒容密闭容器中,将物质的量之和为3mol的NH3和CO2以不同的氨碳比进行反应,结果如图3所示,a,b分别表示CO2或NH3的转化率,c表示平衡体系中尿素的体积分数,$\frac{n(N{H}_{3})}{C{O}_{2}}$=2时,尿素的产量最大;该条件下反应的平衡常数K=40.
8.二甲醚(DME)被誉为“21世纪的清洁燃料”.由合成气制备二甲醚的主要原理如下:
反应Ⅰ:CO(g)+2H2(g)?CH3OH(g)△H1
反应Ⅱ:2CH3OH(g)?CH3OCH3(g)+H2O(g)、△H2
反应Ⅲ:2CO(g)+4H2(g)?CH3OCH3(g)+H2O(g)△H3
相关反应在不同温度时的平衡常数及其大小关系如表所示
回答下列问题:
(1)反应Ⅰ的自发性可能自发(填“一定自发”、“可能自发”或“一定不自发”);反应Ⅱ的平衡常数表达式为$\frac{c({H}_{2}O)•c(C{H}_{3}OC{H}_{3})}{{c}^{2}(C{H}_{3}OH)}$,反应Ⅲ的△H3和△H1、△H2的关系△H3=2×△H1+△H2反应.
(2)在合成过程中,因为有CO(g)+H2O(g)?CO2(g)+H2(g)反应发生,所以能提高CH3OCH3的产率,原因是此反应消耗了H2O(g)有利于反应II、III正向移动;同时此反应生成了H2,有利于反应I、III正向移动.
(3)如图1两条曲线分别表示反应I(按物质的量比:n(CO):n(H2)=1:2)中压强为0.1MPa和5.0MPa下CO转化率随温度的变化关系,计算压强为5.0MPa、温度为200℃时,平衡混合气中甲醇的物质的量分数是43.75%.

(4)反应Ⅲ逆反应速率与时间的关系如图2所示:
①试判断t2时改变的条件是增大生成物C浓度或升高温度.
②若t4扩大容器体积,t5达到平衡,t6时增大反应物浓度,请在上图中画出t4-t6的变化曲线.
反应Ⅰ:CO(g)+2H2(g)?CH3OH(g)△H1
反应Ⅱ:2CH3OH(g)?CH3OCH3(g)+H2O(g)、△H2
反应Ⅲ:2CO(g)+4H2(g)?CH3OCH3(g)+H2O(g)△H3
相关反应在不同温度时的平衡常数及其大小关系如表所示
| 温度/K | 反应I | 反应Ⅱ | 已知: K1>K2>K1′>K2′ |
| 298 | K1 | K2 | |
| 328 | K1′ | K2′ |
(1)反应Ⅰ的自发性可能自发(填“一定自发”、“可能自发”或“一定不自发”);反应Ⅱ的平衡常数表达式为$\frac{c({H}_{2}O)•c(C{H}_{3}OC{H}_{3})}{{c}^{2}(C{H}_{3}OH)}$,反应Ⅲ的△H3和△H1、△H2的关系△H3=2×△H1+△H2反应.
(2)在合成过程中,因为有CO(g)+H2O(g)?CO2(g)+H2(g)反应发生,所以能提高CH3OCH3的产率,原因是此反应消耗了H2O(g)有利于反应II、III正向移动;同时此反应生成了H2,有利于反应I、III正向移动.
(3)如图1两条曲线分别表示反应I(按物质的量比:n(CO):n(H2)=1:2)中压强为0.1MPa和5.0MPa下CO转化率随温度的变化关系,计算压强为5.0MPa、温度为200℃时,平衡混合气中甲醇的物质的量分数是43.75%.

(4)反应Ⅲ逆反应速率与时间的关系如图2所示:
①试判断t2时改变的条件是增大生成物C浓度或升高温度.
②若t4扩大容器体积,t5达到平衡,t6时增大反应物浓度,请在上图中画出t4-t6的变化曲线.