题目内容
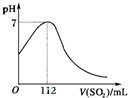 在标准状况下,向100mL氢硫酸溶液中通入二氧化硫气体,溶液pH的变化如图所示,则原氢硫酸溶液的物质的量浓度为:( )
在标准状况下,向100mL氢硫酸溶液中通入二氧化硫气体,溶液pH的变化如图所示,则原氢硫酸溶液的物质的量浓度为:( )分析:标准状况下,向100mL氢硫酸溶液中通入二氧化硫,发生反应2H2S+SO2=3S↓+2H2O,溶液pH=7时,二氧化硫越硫化氢恰好反应,此时消耗二氧化硫112mL,根据n=
计算二氧化硫的物质的量,再根据方程式计算硫化氢的物质的量,根据c=
计算.
| V |
| Vm |
| n |
| V |
解答:解:标准状况下,向100mL氢硫酸溶液中通入二氧化硫,发生反应2H2S+SO2=3S↓+2H2O,溶液pH=7时,二氧化硫越硫化氢恰好反应,此时消耗二氧化硫112mL,二氧化硫的物质的量=
=0.005mol,根据方程式可知硫化氢的物质的量为0.005mol×2=0.01mol,则原氢硫酸溶液的物质的量浓度为
=0.1mol/L,
故选D.
| 0.112L |
| 22.4L/mol |
| 0.01mol |
| 0.1L |
故选D.
点评:本题考查根据方程式进行的计算,难度不大,判断pH=7时二氧化硫与硫化氢恰好反应是关键,注意对基础知识的理解掌握.

练习册系列答案
 优质课堂快乐成长系列答案
优质课堂快乐成长系列答案
相关题目
|
下列离子方程式正确的是 | |
| [ ] | |
A. |
氯化铵溶液呈酸性 NH |
B. |
氢硫酸电离 H2S |
C. |
向小苏打溶液中加入醋酸溶液 HCO |
D. |
在标准状况下,向10 mL 0.1 mol·L-1 FeBr2溶液中通入22.4 mL Cl2 2Fe2++2Br-+2Cl2 |
 NH3+H+
NH3+H+ 2H++S2-
2H++S2- CO2+H2O
CO2+H2O 2Fe3++Br2+4Cl-
2Fe3++Br2+4Cl-