题目内容
8.在硫酸铜溶液中加入一定量的铁片,充分反应后铁片的质量增加了0.4g,求析出铜的质量是多少克?分析 铁与硫酸铜反应生成铜和硫酸亚铁,生成的铜附着铁片上,而消耗铁的质量小于生成铜的质量,因此铁片质量增加;利用反应的化学方程式,根据铁片质量增加量可计算出生成铜的质量.
解答 解:设析出铜的质量为x,
Fe+CuSO4=FeSO4+Cu 铁片质量增加
56 64 64-56=8
x 0.4g
则:$\frac{64}{x}$=$\frac{8}{0.4g}$,解得:x=3.2g
答:析出铜的质量是3.2g.
点评 本题考查了混合物反应的计算,题目难度不大,明确反应前后质量不会的原因为解答关键,注意掌握差量法在化学计算中的应用方法,试题培养了学生的化学计算能力.

练习册系列答案
相关题目
18.下列说法错误的是( )
| A. | 摩尔是国际科学界建议采用的一种物理量 | |
| B. | 摩尔是物质的量的单位,简称摩,符号为mol | |
| C. | 1mol氧气约含6.02×1023个O2 | |
| D. | 0.5molH2O含有的原子数目为1.5NA |
16.海洋是地球生命的摇篮,她为地球生命提供了水循环,为地球储存能量,吸收、分解地球生命排出的各种物质,使地球适合生命的存在,下列说法中不正确的是( )
| A. | 海水蒸发→云→降水,这是地球水循环的过程,该过程主要是物理变化 | |
| B. | 海水中所含的常量元素大部分以盐的形式存在,其中含量最高的盐是氯化钠 | |
| C. | 海洋是化学元素的集散地,元素周期表所有的元素在海水中都能找到 | |
| D. | 由海水制备镁、氯、溴、碘等单质均需要涉及氧化还原反应 |
3.设NA表示阿伏伽德罗常数的值,下列说法正确的是( )
| A. | a mol Na2O2中含有的离子数为4aNA | |
| B. | 100mL 1mol/L NaHCO3溶液中含有0.1NA个HCO3- | |
| C. | 标准状况下,2.24L氟化氢,其分子数为0.1NA | |
| D. | 28g N2和N4的混合气体中含有原子个数为2NA |
20.W、X、Y、Z为原子序数依次增大的短周期元素,W原子与X原子最外层电子数之和与Z原子最外层电子数相等.Z原子最外层电子数是Y原子最外层电子数的2倍,XW3气体能使酚酞溶液变红.下列说怯正确的是( )
| A. | 单质沸点:X>Y | B. | 阳离子的氧化性:W>Y | ||
| C. | 氧化物对应水化物的酸性:Z>X | D. | Y、Z离子均能抑制水的电离 |
11.化学试剂不变质和实验方法科学是化学实验成功的保障.下列试剂保存方法或实验方法中,不正确的是( )
| A. | 保存FeCl2溶液时,通常在溶液中加少量的单质铁 | |
| B. | 常温下,浓硝酸可以用铁罐车贮运 | |
| C. | 可用湿润的蓝色石蕊试纸检验氨气 | |
| D. | 除去CO2中混有的HCl,可通过盛有饱和NaHCO3溶液的洗瓶 |
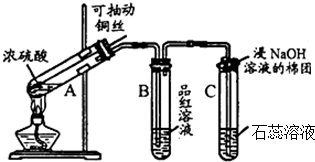
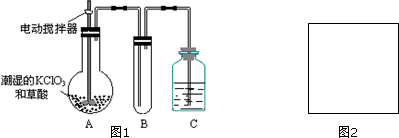 X+5H2O,则X的化学式NaCl.
X+5H2O,则X的化学式NaCl.