题目内容
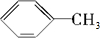
3.“瘦肉精”对人体健康会产生危害,已知某种“瘦肉精”含有克伦特罗,其结构如下图所示.下列有关克伦特罗的叙述不正确的是( )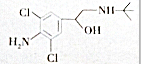
| A. | 该物质含有苯环,属于芳香族化合团 | |
| B. | 该物质只含有-OH,-NH2两种官能团 | |
| C. | 该物质含有-OH,就具有-OH的性质 | |
| D. | 该物质能发生氧化反应 |
分析 A、含苯环,叫属于芳香族化合物;
B、该物质只含有-OH,-NH2、-Cl三种官能团;
C、官能团是决定物质化学性质的原子团;
D、与羟基相连碳上有氢,所以可能发生催化氧化反应.
解答 解:A、含苯环,该物质属于芳香族化合物,故A正确;
B、该物质只含有-OH,-NH2、-Cl三种官能团,而不是两种,故B错误;
C、官能团是决定物质化学性质的原子团,所以该物质含有-OH,就具有-OH的性质,故C正确;
D、与羟基相连碳上有氢,所以可能发生催化氧化反应,生成羰基化合物,所以该物质能发生氧化反应,故D正确;
故选B.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重有机物性质及分析与应用能力的考查,题目难度不大.

练习册系列答案
相关题目
13.下列有关金属腐蚀与防护的说法不正确的是( )
| A. | 金属腐蚀就是金属原子失去电子被氧化的过程 | |
| B. | 钢铁吸氧腐蚀时,正极反应式为:2H20+O2+4e-═4OH- | |
| C. | 在轮船底镶嵌锌块以保护船体,利用的是牺牲阳极保护法 | |
| D. | 纯银器表面在空气中因电化学腐蚀渐渐变暗 |
14.下列有关说法正确的是( )
| A. | 2014年西非国家爆发埃博拉病毒,双氧水、高锰酸钾溶液可以完全杀灭该病毒感染,其消毒原理和漂白粉消毒饮用水相同 | |
| B. | PM2.5表示每立方米空气中直径小于或等于2.5微米的颗粒物的含量,2015年初公益调查《柴静雾霾调查:穹顶之下》发布,引起社会强烈反响,PM2.5引起的雾霾一定属于气溶胶. | |
| C. | 陶瓷、玻璃和光导纤维都是硅酸盐材料 | |
| D. | 原子结构模型的演变经历了: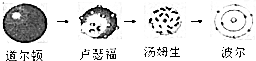 |
5.乙醛能与银氨溶液反应析出银,如果条件控制适当,析出的银会均匀分布在试管上,形成光亮的银镜,这个反应叫银镜反应.银镜的光亮程度与反应条件有关,某课外活动小组同学在课外活动中对乙醛的银镜反应进行了探究.
Ⅰ.探究银镜反应的最佳实验条件的部分实验数据如下表:
请回答下列问题:
(1)若只进行实验1和实验3,其探究目的是比较乙醛用量不同,生成银镜的时间(速度或质量均可).
(2)推理当银氨溶液的量为1mL,乙醛的量为3滴,水浴温度为40℃,反应混合液pH为11时,出现银镜的时间范围是在6.5~9min之间.
(3)进一步实验还可探索银氨溶液的用量不同或pH不同对出现银镜快慢的影响.
Ⅱ.探究对废液的回收处理:银氨溶液放久后会变成氮化银而引起爆炸,直接排放会污染环
境,且造成银资源的浪费.通过查找资料,已知从银氨溶液中提取银的一种实验流程如下:
$→_{①}^{(NH_{4})_{2}S}$$→_{②}^{过滤、洗涤}$$→_{③}^{烘干}$Ag2S$→_{④}^{铁粉还原}$银粉
(4)操作④的方法是把Ag2S和铁粉放到烧杯中加浓盐酸搅拌煮沸,使Ag2S变成银粉,反应的化学方程式为Ag2S+Fe+2HCl$\frac{\underline{\;\;△\;\;}}{\;}$2Ag+FeCl2+H2S↑.过滤需要用到的玻璃仪器有bef(填编号).要得到纯净的Ag2S沉淀,需要洗涤沉淀,实验室过滤器中洗涤沉淀的操作是:沿着玻璃棒向过滤器注入蒸馏水浸没沉淀,水自然流下,重复2~3次.
(5)根据电化原理也可Ag2S转变为Ag,方法是:在铝质容器中加入食盐溶液,再将表面生成Ag2S的银器浸入该溶液中,一段时间后发现黑色会褪去.
①该装置中银器为正极.
②该装置总反应的化学方程式为2Al+3Ag2 S+3H2O=2Al(OH)3+6Ag+3H2S↑.
Ⅰ.探究银镜反应的最佳实验条件的部分实验数据如下表:
| 实验序号 | 银氨溶液 | 乙醛的量/滴 | 水浴温度/℃ | 反应混合液的pH | 出现银镜时间 |
| 1 | 1 | 3 | 65 | 11 | 5 |
| 2 | 1 | 3 | 45 | 11 | 6.5 |
| 3 | 1 | 5 | 65 | 11 | 4 |
| 4 | 1 | 3 | 30 | 11 | 9 |
| 5 | 1 | 3 | 50 | 11 | 6 |
| 6 | 1 | 5 | 80 | 11 | 3 |
(1)若只进行实验1和实验3,其探究目的是比较乙醛用量不同,生成银镜的时间(速度或质量均可).
(2)推理当银氨溶液的量为1mL,乙醛的量为3滴,水浴温度为40℃,反应混合液pH为11时,出现银镜的时间范围是在6.5~9min之间.
(3)进一步实验还可探索银氨溶液的用量不同或pH不同对出现银镜快慢的影响.
Ⅱ.探究对废液的回收处理:银氨溶液放久后会变成氮化银而引起爆炸,直接排放会污染环
境,且造成银资源的浪费.通过查找资料,已知从银氨溶液中提取银的一种实验流程如下:
$→_{①}^{(NH_{4})_{2}S}$$→_{②}^{过滤、洗涤}$$→_{③}^{烘干}$Ag2S$→_{④}^{铁粉还原}$银粉
(4)操作④的方法是把Ag2S和铁粉放到烧杯中加浓盐酸搅拌煮沸,使Ag2S变成银粉,反应的化学方程式为Ag2S+Fe+2HCl$\frac{\underline{\;\;△\;\;}}{\;}$2Ag+FeCl2+H2S↑.过滤需要用到的玻璃仪器有bef(填编号).要得到纯净的Ag2S沉淀,需要洗涤沉淀,实验室过滤器中洗涤沉淀的操作是:沿着玻璃棒向过滤器注入蒸馏水浸没沉淀,水自然流下,重复2~3次.

(5)根据电化原理也可Ag2S转变为Ag,方法是:在铝质容器中加入食盐溶液,再将表面生成Ag2S的银器浸入该溶液中,一段时间后发现黑色会褪去.
①该装置中银器为正极.
②该装置总反应的化学方程式为2Al+3Ag2 S+3H2O=2Al(OH)3+6Ag+3H2S↑.
12.某小组探究Na2CO3和NaHCO3的性质,实验步骤及记录如下:
Ⅰ.分别向盛有0.5g Na2CO3固体、0.5g NaHCO3固体的烧杯中加入10mL水(20℃),搅拌,测量温度为T1;
Ⅱ.静置恒温后测量温度为T2;
Ⅲ.分别加入10mL 密度约为1.1g/mL 20%的盐酸(20℃),搅拌,测量温度T3.
得到表1的数据:
温度试剂
表1
回答下列问题:
(1)Na2CO3溶于水显碱性,其原因是CO32-+H2O?HCO3-+OH-、HCO3-+H2O?H2CO3+OH-(用离子方程式表示).
(2)根据试题后的附表判断:
步骤Ⅰ中Na2CO3、NaHCO3固体分别是全部溶解还是部分溶解Na2CO3、NaHCO3固体都是全部溶解.
(3)分析表1的数据得出:Na2CO3固体溶于水放热,NaHCO3固体溶于水吸热
(填“放热”或“吸热”).
(4)甲同学分析上述数据得出:Na2CO3和NaHCO3与盐酸反应都是放热反应.
乙同学认为应该增加一个实验,并补做如下实验:向 盛 有10 mL水(20℃)的烧杯中
加入10mL密度约为1.1g/mL20%的盐酸,搅拌,测量温度为22.2℃.
(5)结合上述探究,下列说法正确的是AC.
A.NaHCO3与盐酸的反应是吸热反应
B.不能用稀盐酸鉴别Na2CO3和NaHCO3固体
C.Na2CO3、NaHCO3固体与稀盐酸反应的能量变化还与物质的溶解等因素有关
(6)丙同学为测定一份NaHCO3和Na2CO3混合固体中NaHCO3的纯度,称取m1 g混合物,加热至质量不变时,称其质量为m2 g,则原混合物中NaHCO3的质量分数为$\frac{84(m_{1}-m_{2})}{31m_{1}}$×100%(用代数式表示).
附表:溶解度表
Ⅰ.分别向盛有0.5g Na2CO3固体、0.5g NaHCO3固体的烧杯中加入10mL水(20℃),搅拌,测量温度为T1;
Ⅱ.静置恒温后测量温度为T2;
Ⅲ.分别加入10mL 密度约为1.1g/mL 20%的盐酸(20℃),搅拌,测量温度T3.
得到表1的数据:
温度试剂
表1
| 试剂 温度 | T1/℃ | T2/℃ | T3/℃ |
| Na2CO3 | 23.3 | 20.0 | 23.7 |
| NaHCO3 | 18.5 | 20.0 | 20.8 |
(1)Na2CO3溶于水显碱性,其原因是CO32-+H2O?HCO3-+OH-、HCO3-+H2O?H2CO3+OH-(用离子方程式表示).
(2)根据试题后的附表判断:
步骤Ⅰ中Na2CO3、NaHCO3固体分别是全部溶解还是部分溶解Na2CO3、NaHCO3固体都是全部溶解.
(3)分析表1的数据得出:Na2CO3固体溶于水放热,NaHCO3固体溶于水吸热
(填“放热”或“吸热”).
(4)甲同学分析上述数据得出:Na2CO3和NaHCO3与盐酸反应都是放热反应.
乙同学认为应该增加一个实验,并补做如下实验:向 盛 有10 mL水(20℃)的烧杯中
加入10mL密度约为1.1g/mL20%的盐酸,搅拌,测量温度为22.2℃.
(5)结合上述探究,下列说法正确的是AC.
A.NaHCO3与盐酸的反应是吸热反应
B.不能用稀盐酸鉴别Na2CO3和NaHCO3固体
C.Na2CO3、NaHCO3固体与稀盐酸反应的能量变化还与物质的溶解等因素有关
(6)丙同学为测定一份NaHCO3和Na2CO3混合固体中NaHCO3的纯度,称取m1 g混合物,加热至质量不变时,称其质量为m2 g,则原混合物中NaHCO3的质量分数为$\frac{84(m_{1}-m_{2})}{31m_{1}}$×100%(用代数式表示).
附表:溶解度表
温度 溶解度 | 10℃ | 20℃ | 30℃ | 40℃ |
| Na2CO3 | 12.5g | 21.5g | 39.7g | 40.0g |
| NaHCO3 | 8.1g | 9.6g | 11.1g | 12.7g |