题目内容
1.某化学小组以苯甲酸为原料制取苯甲酸甲酯.已知有关物质的沸点和相对分子质量如表:| 物质 | 甲醇 | 苯甲酸 | 苯甲酸甲酯 |
| 沸点/℃ | 64.7 | 249 | 199.6 |
| 相对分子质量 | 32 | 122 | 136 |

(提示:苯甲酸甲酯粗产品往往含有少量甲醇、硫酸、苯甲酸和水等)
(1)简述第一步混合液体时,最后加入浓硫酸的理由是浓硫酸密度较大,且易于苯甲酸、甲醇混合放出大量热量,甲醇易挥发.若反应产物水分子中有同位素18O,写出能表示反应前后18O位置的化学方程式
 .
.(2)反应物CH3OH应过量,理由是该反应是可逆反应,增加甲醇的量,使平衡向右移动,有利于提高苯甲酸的转化率.
(3)分液时上层液体从分液漏斗的上口出来,接受馏分时温度控制在199.6℃左右.
(4)以上流程图中加入Na2CO3的作用是通过反应消耗硫酸、苯甲酸,降低苯甲酸甲酯的溶解度.
(5)通过计算,苯甲酸甲酯的产率为65%.
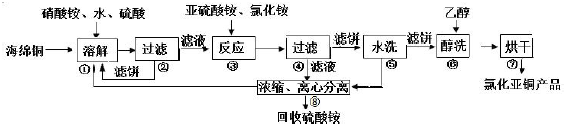
分析 在浓硫酸作催化剂、加热条件下,甲醇和苯甲酸发生酯化反应生成苯甲酸甲酯,冷却后向烧瓶中加入水,将得到的混合溶液移置到分液漏斗中,然后进行分液,将得到的上层液体倒入锥形瓶中,锥形瓶中加入饱和的碳酸钠溶液,饱和的碳酸钠溶液能抑制苯甲酸甲酯的溶解,能和苯甲酸、硫酸反应生成钠盐,然后过滤,最后蒸馏得到粗产品;
(1)混合溶液时,先加入密度小的液体,后加入密度大的液体,且甲醇都易挥发;
二者在浓硫酸作催化剂、加热条件下发生酯化反应生成苯甲酸甲酯;
(2)该反应是可逆反应,反应物CH3OH过量,促进平衡正向移动;
(3)分液时上层液体从上口倒出,温度计的温度应该大于苯甲酸甲酯的熔点而小于苯甲酸的熔点;
(4)Na2CO3溶液能消耗硫酸和苯甲酸,降低酯的溶解度;
(5)苯甲酸甲酯的产率=$\frac{实际质量}{理论质量}×100%$.
解答 解:在浓硫酸作催化剂、加热条件下,甲醇和苯甲酸发生酯化反应生成苯甲酸甲酯,冷却后向烧瓶中加入水,将得到的混合溶液移置到分液漏斗中,然后进行分液,将得到的上层液体倒入锥形瓶中,锥形瓶中加入饱和的碳酸钠溶液,饱和的碳酸钠溶液能抑制苯甲酸甲酯的溶解,能和苯甲酸、硫酸反应生成钠盐,然后过滤,最后蒸馏得到粗产品;
(1)混合溶液时,先加入密度小的液体,后加入密度大的液体,苯甲酸、甲醇混合时放出大量热量,甲醇易挥发,所以应该最后加入浓硫酸;
二者在浓硫酸作催化剂、加热条件下发生酯化反应生成苯甲酸甲酯,反应方程式为 ,
,
故答案为:浓硫酸密度较大,且易于苯甲酸、甲醇混合放出大量热量,甲醇易挥发; ;
;
(2)该反应是可逆反应,反应物CH3OH过量,促进平衡正向移动,从而提高苯甲酸的转化率,
故答案为:该反应是可逆反应,增加甲醇的量,使平衡向右移动,有利于提高苯甲酸的转化率;
(3)分液时上层液体从分液漏斗的上口倒出,温度计的温度应该大于苯甲酸甲酯的熔点而小于苯甲酸的熔点,所以温度控制在199.6℃左右,故答案为:分液漏斗的上口;199.6℃左右;
(4)Na2CO3溶液能消耗硫酸和苯甲酸,降低酯的溶解度,
故答案为:通过反应消耗硫酸、苯甲酸,降低苯甲酸甲酯的溶解度;
(5)苯甲酸的物质的量=$\frac{12.2g}{122g/mol}$=0.1mol,甲醇的物质的量=$\frac{0.79g/mL×20mL}{32g/mol}$=0.5mol,根据方程式知,甲醇过量,应该以苯甲酸为标准进行计算,n(苯甲酸甲酯)=n(苯甲酸)=0.1mol,则苯甲酸甲酯的质量=0.1mol×136g/mol=13.6g,苯甲酸甲酯的产率=$\frac{实际质量}{理论质量}×100%$=$\frac{8.84g}{13.6g}×100%$=65%,
故答案为:65%.
点评 本题考查物质制备,为高频考点,涉及实验基本操作、基本计算、反应条件的判断、物质分离和提纯等知识点,明确实验原理及物质性质、物质分离提纯方法是解本题关键,注意冷凝管中水流方向,为易错点.

 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案| 编号 | ① | ② | ③ | ④ |
| 装置 | 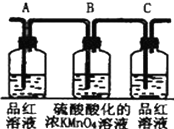 |  |  |  |
④→②→①→③.
(2)实验时可观察到:装置①中A瓶的溶液褪色,C瓶的溶液不褪色.B瓶溶液的作用是将多余的SO2全部氧化吸收,C瓶溶液的作用是确证产物中SO2已被B瓶溶液全部氧化.
(3)装置②中所加的固体药品是无水CuSO4,可确证的产物是水蒸气,确定装置②在整套装置中位置的理由是由于产物气流通过①、③时会带出水蒸气,所以②必须在①、③之前.
(4)盛放浓硫酸的试剂瓶标签上应印有下列警示标记中的D

| A. | 以Mg、Al为电极,NaOH溶液为电解质溶液的原电池中,导线上流过NA个电子,则正极放出H2的体积为11.2 L | |
| B. | 常温常压下,2.8g的乙烯和丙烯的混合气体中含碳碳双键的数目为0.1NA | |
| C. | 常温下1 L 0.5mol/L NH4Cl溶液与2L 0.25mol/L NH4Cl溶液所含NH4+的数目均为0.5NA | |
| D. | 高温下,16.8 g Fe与足量水蒸气完全反应失去0.8NA个电子 |
常见高铁酸钾的制备方法如下:
| 制备方法 | 具体内容 |
| 干法 | Fe2O3、KNO3、KOH混合加热共熔生成紫红色高铁酸钾和KNO2等产物 |
| 湿法 | 强碱性介质中,Fe(NO3)3与KClO反应生成紫红色高铁酸钾溶液 |
| 电解法 | 电解浓NaOH溶液制备Na2FeO4 |
(2)某湿法制备高铁酸钾的基本流程及步骤如下:
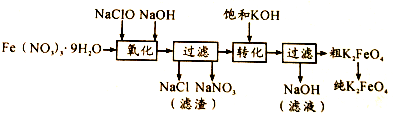
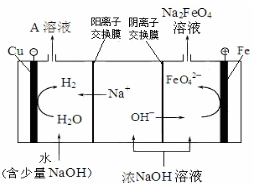
①控制反应温度为25℃,搅拌1.5h,经氧化等过程溶液变为紫红色,该反应的离子方程式为3ClO-+2Fe3++10OH-═2FeO42-+3Cl-+5H2O.
②在紫红色溶液中加入饱和KOH溶液,析出紫黑色晶体,过滤,得到K2FeO4粗产品.沉淀过程中加入饱和KOH溶液得到晶体的原因是该温度下高铁酸钾的溶解度比高铁酸钠的溶解度小.
③K2FeO4粗产品含有Fe(OH)3、KCl等杂质,用重结晶方法进行分离提纯.其提纯步骤为:将一定量的K2FeO4粗产品溶于冷的3mol/LKOH溶液中,过滤,将滤液置于冰水浴中,向滤液中加入饱和KOH溶液,搅拌、静置、过滤,用乙醇洗涤2~3次,在真空干燥箱中干燥.
④若以FeCl3 代替Fe(NO3)3作铁源,K2FeO4的产率和纯度都会降低.一个原因是在反应温度和强碱环境下NaCl的溶解度比NaNO3大,使得NaCl结晶去除率较低;另一个原因是Cl-被FeO42-氧化,消耗产品使产率降低.
(3)工业上还可用通过电解浓NaOH溶液制备Na2FeO4,其工作原理如下图所示:阳极的电极反应为Fe-6e-+8OH-=FeO42-+4H2O;其中可循环使用的物质的电子式是
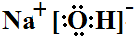 .
.
(4)已知25℃时,Ksp[Fe(OH)3]=4.0×10-38、Ksp[Cu(OH)2]=2.2×10-20,向该温度下含有Fe3+、Cu2+浓度均为0.01mol/L的溶液中,滴加浓NaOH溶液,当溶液pH=10时,溶液中c(Cu2+):c(Fe3+)=5.5×1013:1.
| A. | 石灰石在高温下的分解反应 | B. | 金属钠和水的反应 | ||
| C. | 盐酸与氢氧化钠溶液的反应 | D. | 铝热反应 |

| A. | 铜中含有大量的有机物,可采用灼烧的方法除去有机物 | |
| B. | 灼烧后含有少量铜的可能原因是该条件下铜无法被氧气氧化 | |
| C. | 通过途径Ⅱ实现用粗制氧化铜制取胆矾,必须进行的实验操作步骤:酸溶、加热通氧气、过滤、蒸发、冷却结晶、过滤、自然干燥 | |
| D. | 与途径II相比,产生等量的胆矾途径I消耗硫酸少,途径I不会产生污染大气的气体 |
 非血红素铁是食物中铁存在的形式之一,主要是三价铁与蛋白质和羧酸结合成络合物.
非血红素铁是食物中铁存在的形式之一,主要是三价铁与蛋白质和羧酸结合成络合物.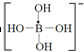 .
.