题目内容
8.下列说法中错误的是( )| A. | 弱电解质的电离是一个吸热过程,升温其电离度增大 | |
| B. | 某些盐类的水解是一个吸热过程,升温水解程度增大 | |
| C. | 溶液的酸碱性取决于溶液中氢离子浓度的大小 | |
| D. | 酸性溶液不一定是酸溶液,碱性溶液不一定是碱溶液 |
分析 A.弱电解质电离时要吸收能量;B、盐类的水解是一个吸热过程;C、溶液的酸碱性取决于溶液中氢离子和氢氧根离子浓度的相对大小;D、有的盐水解显示酸性,有的盐水解显示碱性.
解答 解:A.弱电解质电离时要吸收能量,即弱电解质的电离是一个吸热的过程,故A正确;B、盐类的水解是一个吸热过程,升温促进水解,所以水解程度增大,故B正确;C、溶液的酸碱性取决于溶液中氢离子和氢氧根离子浓度的相对大小,故C错误;D、酸性溶液不一定是酸溶液,有的盐水解显示酸性,碱性溶液不一定是碱溶液,有的盐水解显示碱性,故D正确.故选C.
点评 本题考查学生盐的水解原理以及应用、溶液酸碱性的判断等方面的知识,属于综合知识的考查,难度中等.

练习册系列答案
相关题目
20.黑火药爆炸时反应如下:S+2KNO3+3C═K2S+X+3CO2.其中X的化学式为( )
| A. | N2 | B. | NO2 | C. | NO | D. | N2O |
20.设NA为阿伏加德罗常数的数值.下列说法正确的是( )
| A. | 80mL 10mol•L-1 盐酸与足量MnO2加热反应,产生Cl2分子数为0.2NA | |
| B. | 2 L0.5 mol•L-1硫酸钾溶液中阴离子所带电荷数为NA | |
| C. | 标况下,11.2 L氯气完全溶于1 L水中,所得溶液中Cl-和ClO-两种粒子数之和为NA | |
| D. | 标准状况下,11.2LSO3所含的分子数大于0.5NA |
17.下列反应中符合图象的是( )
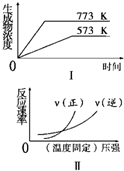

| A. | N2(g)+3H2(g)?2NH3(g)△H<0 | B. | 2SO3(g)?2SO2 (g)+O2(g)△H>0 | ||
| C. | 4NH3(g)+5O2 (g)?4NO(g)+6H2O(g)△H<0 | D. | H2(g)+CO(g)?C(s)+H2O(g)△H>0 |
18.下列有关说法正确的是( )
| A. | 铁碳合金发生电化腐蚀时,电子由碳流向铁 | |
| B. | 6NO(g)+4NH3(g)═5N2(g)+6H2O(l)常温下能自发进行,则该反应△H>0 | |
| C. | 常温下,用水稀释0.1mol•L-1NH4Cl溶液,则$\frac{c(N{H}_{3}•{H}_{2}O)}{c(N{H}_{4}^{+})•(O{H}^{-})}$的值不变 | |
| D. | 对于溴乙烷的水解反应(△H>0),加入NaOH 并加热,该反应的反应速率和平衡常数均增大 |




 B.
B. C.
C. D.CH3CH2C≡CH与CH2═CH-CH═CH2E.
D.CH3CH2C≡CH与CH2═CH-CH═CH2E. F.戊烯和戊烷
F.戊烯和戊烷 表示的分子式C6H14结构简式CH3CH(CH3)CH2CH2CH3,名称是2-甲基戊烷.
表示的分子式C6H14结构简式CH3CH(CH3)CH2CH2CH3,名称是2-甲基戊烷.