题目内容
9.Na2O2是强氧化剂,也是航天航空、水下作业的供氧剂.(1)Na2O2作供氧剂时,主要与人呼出的CO2反应,写出该反应的化学方程式,并用双线桥标明电子转移的方向和数目
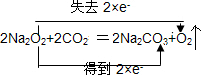 .
.(2)航空和水下作业有时也会产生污染性气体,某学习小组欲探究Na2o2能否完全吸收氮氧化物、硫氧化物等污染性气体,设计了如下装置(未画完):
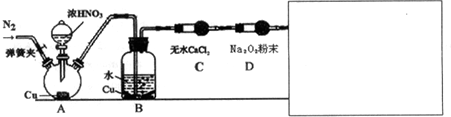
【资料信息】①酸性条件下,NO和NO2都能与MnO4-(H+)反应生成NO3-和Mn2+
②稀硝酸与Cu反应缓慢 ③2NO+Na2O2=2NaNO2
请在答题卷方框内补充完整装置示意图,并做必要标注.补充装置的作用是检验污染气体是否完全被Na2O2吸收,同时可防止污染气体排放到空气中.
(3)该学习小组中甲、乙、丙三位同学设计实验如下,完成表中空格(乙和丙同学对装置和试剂上进行了优化):
| 实验学生 | 实验操作 | 现象与结论 |
| 甲 | 滴入浓硝酸前,需先打开弹簧夹,通入一段时间N2,目的是将装置中的空气排出.关闭弹簧夹,打开分液漏斗活塞,加入适量浓硝酸后关闭活塞. | 酸性高锰酸钾溶液不褪色,说明Na2O2能完全吸收NO, |
| 乙 | 去掉装置B,直接将A、C装置相连.打开分液漏斗活塞,加入适量浓硝酸后关闭活塞. | 与甲同学现象相似,说明Na2O2能完全吸收NO2 |
| 丙 | 在乙同学装置的基础上,将A装置中浓硝酸换成浓硫酸,并进行加热,(或将分液漏斗中的试剂换为浓硫酸,将铜换为亚硫酸钠粉末),打开分液漏斗活塞,加入适量试剂后关闭活塞. | 与甲同学现象相似,说明Na2O2能完全吸收NO2 |
分析 (1)Na2O2中O元素化合价为-1价,在反应2Na2O2+2CO2=2Na2CO3+O2中,只有O元素化合价发生变化,O元素化合价分别由-1价降低到-2价、升高到0价,反应中Na2O2既是氧化剂又是还原剂,O2为氧化产物,Na2CO3为还原产物,该反应中转移2e-;
(2)探究Na2o2能否完全吸收氮氧化物、硫氧化物等污染性气体,A装置:铜和浓硝酸反应,和稀硝酸反应,由于一氧化氮在空气中容易被氧化为二氧化氮,故需先通入氮气,将装置中的空气排出,B装置:铜和、稀硝酸反应,C干燥一氧化氮,D装置:NO与Na2O2反应,需补充的装置应为检验氮氧化物是否被反应完全的装置,同时可防止污染气体排放到空气中;
(3)甲:一氧化氮在空气中容易被氧化为二氧化氮,需排出装置中的空气,乙:去掉装置B,直接将A、C装置相连,丙,铜和浓硫酸反应可制取二氧化硫,或浓硫酸和亚硫酸钠反应制取二氧化硫,乙同学实验中D装置发生的反应可根据2NO+Na2O2=2NaNO2书写.
解答 解:(1)在 2Na2O2+2CO2═2Na2CO3+O2反应中,只有Na2O2中O元素的化合价发生变化,分别由-1价变化为0价和-2价,用双线桥法可表示为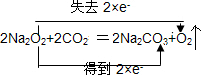 ,
,
故答案为: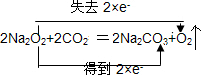 ;
;
(2)根据本次实验的目的探究Na2o2能否完全吸收氮氧化物可知,方框中需补充的装置应为检验氮氧化物是否被反应完全的装置,根据所给的信息酸性条件下,NO和NO2都能与MnO4-(H+)反应生成NO3-和Mn2+可知,一氧化氮、二氧化氮均可与酸性高锰酸钾溶液反应,使溶液褪色,故此处可添加盛有酸性高锰酸钾的溶液的试管,将反应后的尾气通入其中,若溶液褪色则可知污染气体未被过氧化钠吸收,由于一氧化氮、二氧化氮均为污染性的气体,该装置在检验污染气体是否被过氧化钠吸收也能起到防止污染性气体排放到空气中的作用,补充的装置为: ,
,
故答案为: ;
;
(3)甲:通入D装置的气体为一氧化氮,由于一氧化氮在空气中容易被氧化为二氧化氮,故需先通入氮气,将装置中的空气排出,一氧化氮可与酸性高锰酸钾溶液反应,使溶液褪色,若一氧化氮被过氧化钠完全吸收,则无一氧化氮通入高锰酸钾溶液中,溶液不褪色,
乙:根据该同学给出的结论可知通入D装置的为二氧化氮,因此可将B装置去掉,将A、C直接相连,D装置中发生的反应为过氧化钠和二氧化氮的反应,反应方程式可参照2NO+Na2O2=2NaNO2,乙同学实验中D装置发生2NO2+Na2O2=2NaNO3,
丙:结合实验目的以及上述实验可知,丙同学的实验探究过氧化钠能否完全吸收硫氧化物污染气体,故可在乙同学装置的基础上将分液漏斗中的试剂改为浓硫酸,并进行加热,(或将分液漏斗中的试剂换为浓硫酸,将铜换为亚硫酸钠粉末),
故答案为:
| 实验学生 | 实验操作 | 现象与结论 |
| 甲 | 将装置中的空气排出 | 酸性高锰酸钾溶液不褪色 |
| 乙 | 去掉装置B,直接将A、C装置相连 | |
| 丙 | 将A装置中浓硝酸换成浓硫酸,并进行加热,(或将分液漏斗中的试剂换为浓硫酸,将铜换为亚硫酸钠粉末) |
点评 本题考查氮氧化物、硫氧化物与过氧化钠的探究实验,掌握氮硫及其化合物的性质、把握习题中的信息及知识迁移应用为解答的关键,侧重学生综合应用能力及信息抽取和分析能力的考查,题目难度中等.

 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案 高效智能课时作业系列答案
高效智能课时作业系列答案| A. | 1molFe与过量稀HNO3反应,电子转移数为2NA | |
| B. | 120g由NaHSO4和KHSO3组成的混合物含硫原子数为NA | |
| C. | 标准状况下,22.4LCH2Cl2含氯原子数为2 NA | |
| D. | 0.3mol/LAl(NO3)3溶液中含A13+数小于0.3 NA |
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向沸水中滴入几滴FeCl3饱和溶液,继续煮沸,并用激光笔照射 | 溶液变红褐色,出现 丁达尔效应 | 产生了 Fe(OH)3胶体 |
| B | 向FeCl3溶液中滴加少量KI溶液,再滴加几滴淀粉溶液 | 溶液变蓝 | 氧化性:Fe3+>I2 |
| C | 将溴乙烷和NaOH的乙醇溶液混合加热,产生气体通入酸性KMnO4溶液 | 酸性KMnO4溶液褪色 | 产生了乙烯 |
| D | 向滴有酚酞的Na2CO3溶液中,逐滴加入BaCl2溶液 | 溶液红色逐渐褪去 | BaCl2溶液呈酸性 |
| A. | A | B. | B | C. | C | D. | D |
C(金刚石,s)+O2(g)═CO2(g)△H1 ①
C(石墨,s)+O2(g)═CO2(g)△H2 ②
C(石墨,s)═C(金刚石,s)△H3=+1.9kJ•mol-1③
下列说法正确的是( )
| A. | 金刚石比石墨稳定 | |
| B. | 石墨转化成金刚石的反应是吸热反应 | |
| C. | △H3=△H1-△H2 | |
| D. | △H1>△H2 |
| A. |  | B. |  | C. |  | D. |  |
| A. | 浓度均为0.1 mol•L-1的①(NH4)2CO3②(NH4)2SO4③(NH4)2Fe(SO4)2溶液中,c(NH4+)的大小顺序为:③<②<① | |
| B. | 工业上常用Na2SO3溶液作为吸收液脱除烟气中的SO2,随着SO2的吸收,吸收液的pH不断变化.当吸收液呈酸性时:c (Na+)=c (SO32-)+c (HSO3-)+c (H2SO3) | |
| C. | 常温下,将0.1 mol•L-1 CH3COOH溶液加水稀释,当溶液的pH从3.0升到5.0时,溶液中$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$的值增大到原来的100倍 | |
| D. | 向0.2 mol/LNaHCO3溶液中加入等体积0.1 mol/L NaOH溶液:c(CO32-)>c(HCO3-)>c(OH-)>c(H+) |
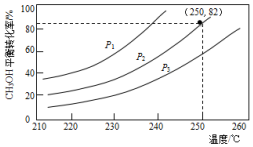 2016年9月.“乔歌里1号”中国首台静默移动发电站MFC30正式问世,MFC30是基于甲醇重整制氢燃料电池发电技术.
2016年9月.“乔歌里1号”中国首台静默移动发电站MFC30正式问世,MFC30是基于甲醇重整制氢燃料电池发电技术.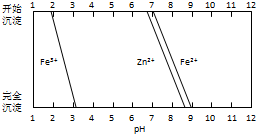 铁酸锌(ZnFe2O4)是对可见光敏感的半导体催化剂,其实验室制备原理为:
铁酸锌(ZnFe2O4)是对可见光敏感的半导体催化剂,其实验室制备原理为: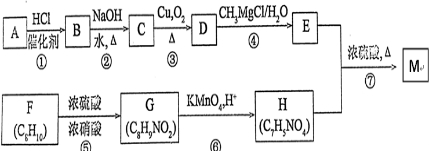
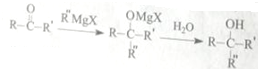
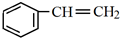 ,H中官能团的名称为羧基、硝基.
,H中官能团的名称为羧基、硝基.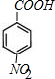 +
+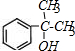 $?_{△}^{浓硫酸}$
$?_{△}^{浓硫酸}$ +H2O.
+H2O. 、
、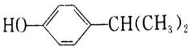 .(任写一种)
.(任写一种)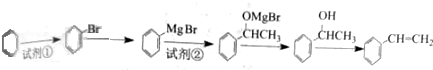
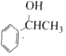 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$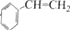 +H2O.
+H2O.