题目内容
某课外小组同学拟用乙醇分解法制乙烯,并对该反应进行探究.
(1)浓硫酸在反应中的作用是 .
实验过程中,可观察到混合液变黑,产生有刺激性气味的气体.某研究小组同学经分析、讨论后认定:此现象是在该反应条件下,浓硫酸与乙醇发生氧化还原反应所致.
(2)为证明产物中混有SO2、CO2气体,甲同学设计了如图1实验装置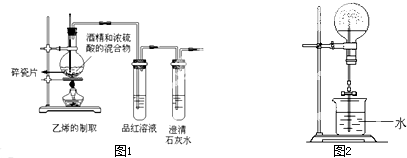
他认为,只要观察到品红褪色,澄清石灰水变浑浊,就可确证混合气体中一定存在有SO2、CO2.甲同学的观点是错误的,理由是 .
(3)为探究乙烯与Br2的反应,乙同学将制取的乙烯气体分别通过:①NaOH溶液,②Ba(OH)2溶液,后用排水法收集于1000mL的圆底烧瓶中(塞好橡皮塞),然后打开橡皮塞,向烧瓶中一次性加入1.5mL液溴,塞上配有带乳胶管(用止水夹夹紧)的尖嘴玻璃管,摇荡,可观察到瓶内红棕色逐渐消失.然后按图2装好装置,
打开止水夹,可观察到有喷泉形成,静置一段时间后,在溶液下部,有一层无色油状液体(约1.5mL).
①将乙烯气体通过Ba(OH)2溶液的目的是 ;
②用化学方程式和简单的文字表述说明产生喷泉的原因 ;
③请利用上述喷泉实验反应的产物设计一个简单实验,证明乙烯与Br2发生的是加成反应而不是取代反应 .
(1)浓硫酸在反应中的作用是
实验过程中,可观察到混合液变黑,产生有刺激性气味的气体.某研究小组同学经分析、讨论后认定:此现象是在该反应条件下,浓硫酸与乙醇发生氧化还原反应所致.
(2)为证明产物中混有SO2、CO2气体,甲同学设计了如图1实验装置

他认为,只要观察到品红褪色,澄清石灰水变浑浊,就可确证混合气体中一定存在有SO2、CO2.甲同学的观点是错误的,理由是
(3)为探究乙烯与Br2的反应,乙同学将制取的乙烯气体分别通过:①NaOH溶液,②Ba(OH)2溶液,后用排水法收集于1000mL的圆底烧瓶中(塞好橡皮塞),然后打开橡皮塞,向烧瓶中一次性加入1.5mL液溴,塞上配有带乳胶管(用止水夹夹紧)的尖嘴玻璃管,摇荡,可观察到瓶内红棕色逐渐消失.然后按图2装好装置,
打开止水夹,可观察到有喷泉形成,静置一段时间后,在溶液下部,有一层无色油状液体(约1.5mL).
①将乙烯气体通过Ba(OH)2溶液的目的是
②用化学方程式和简单的文字表述说明产生喷泉的原因
③请利用上述喷泉实验反应的产物设计一个简单实验,证明乙烯与Br2发生的是加成反应而不是取代反应
考点:乙醇的消去反应,性质实验方案的设计
专题:实验设计题
分析:(1)实验室制备乙烯所用的原料为乙醇,浓硫酸作催化剂、脱水剂,反应条件是加热到170℃;
(2)CO2、SO2气体都能使澄清石灰水变浑浊;
(3)①乙烯气体中可能含有SO2、CO2,而SO2、CO2都可以与Ba(OH)2溶液反应生成沉淀;
②乙烯和溴发生反应,导致烧瓶内压强减小,大气压将水压入烧瓶形成喷泉;
③乙烯若与溴水发生取代,则有HBr生成从而使溶液显酸性,若发生加成反应则生成CH2BrCH2Br溶液不显酸性.
(2)CO2、SO2气体都能使澄清石灰水变浑浊;
(3)①乙烯气体中可能含有SO2、CO2,而SO2、CO2都可以与Ba(OH)2溶液反应生成沉淀;
②乙烯和溴发生反应,导致烧瓶内压强减小,大气压将水压入烧瓶形成喷泉;
③乙烯若与溴水发生取代,则有HBr生成从而使溶液显酸性,若发生加成反应则生成CH2BrCH2Br溶液不显酸性.
解答:
解:(1)利用乙醇在浓硫酸的催化作用下发生分子内脱水制取乙烯,乙醇发生了消去反应,反应方程式为:CH3CH2OH
CH2=CH2↑+H2O,浓硫酸具有吸水性,所以该反应中浓硫酸具有催化性和脱水性,
故答案为:催化剂、脱水剂;
(2)品红溶液褪色说明混合气体中存在SO2,但SO2气体也能使澄清石灰水变浑浊,SO2不一定被品红溶液完全吸收,无法判断CO2是否存在,
故答案为:品红溶液能够检验SO2,但SO2气体也能使澄清石灰水变浑浊,SO2不一定被品红溶液完全吸收,难以判断CO2是否存在;
(3)①乙烯气体中可能含有SO2、CO2,而SO2、CO2都可以与Ba(OH)2溶液反应生成沉淀,将乙烯气体通过Ba(OH)2溶液,可判断SO2、CO2是否已被除尽,
故答案为:确认其中的SO2、CO2均已被除尽;
②乙烯与溴发生加成反应生成液态的1,2-溴乙烷,化学方程式为CH2=CH2+Br2→Br-CH2-CH2-Br,烧瓶内的气体物质的量减少,导致烧瓶内压强减小,大气压将水压入烧瓶形成喷泉,
故答案为:CH2=CH2+Br2→Br-CH2-CH2-Br,溴跟乙烯气体发生加成反应,生成液态的1,2-溴乙烷,导致烧瓶内压强减小,大气压将水压入烧瓶形成喷泉;
③乙烯若与溴水发生取代,则有HBr生成从而使溶液显酸性,若发生加成反应则生成CH2BrCH2Br溶液不显酸性,所以检验方法为:取少量烧瓶中的水层液体,用pH 试纸测定,发现不呈酸性,说明无取代反应产物HBr生成,故发生的是加成反应,
故答案为:取少量烧瓶中的水层液体,用pH 试纸测定,发现不呈酸性,说明无取代反应产物HBr生成,故发生的是加成反应.
| 浓硫酸 |
| 170℃ |
故答案为:催化剂、脱水剂;
(2)品红溶液褪色说明混合气体中存在SO2,但SO2气体也能使澄清石灰水变浑浊,SO2不一定被品红溶液完全吸收,无法判断CO2是否存在,
故答案为:品红溶液能够检验SO2,但SO2气体也能使澄清石灰水变浑浊,SO2不一定被品红溶液完全吸收,难以判断CO2是否存在;
(3)①乙烯气体中可能含有SO2、CO2,而SO2、CO2都可以与Ba(OH)2溶液反应生成沉淀,将乙烯气体通过Ba(OH)2溶液,可判断SO2、CO2是否已被除尽,
故答案为:确认其中的SO2、CO2均已被除尽;
②乙烯与溴发生加成反应生成液态的1,2-溴乙烷,化学方程式为CH2=CH2+Br2→Br-CH2-CH2-Br,烧瓶内的气体物质的量减少,导致烧瓶内压强减小,大气压将水压入烧瓶形成喷泉,
故答案为:CH2=CH2+Br2→Br-CH2-CH2-Br,溴跟乙烯气体发生加成反应,生成液态的1,2-溴乙烷,导致烧瓶内压强减小,大气压将水压入烧瓶形成喷泉;
③乙烯若与溴水发生取代,则有HBr生成从而使溶液显酸性,若发生加成反应则生成CH2BrCH2Br溶液不显酸性,所以检验方法为:取少量烧瓶中的水层液体,用pH 试纸测定,发现不呈酸性,说明无取代反应产物HBr生成,故发生的是加成反应,
故答案为:取少量烧瓶中的水层液体,用pH 试纸测定,发现不呈酸性,说明无取代反应产物HBr生成,故发生的是加成反应.
点评:本题主要考查乙烯的制备和性质实验、物质的分离与除杂,题目难度中等,注意掌握乙烯的制备原理及具有的化学性质,明确物质的分离与除杂方法,试题充分考查了学生的分析、理解能力及化学实验能力.

练习册系列答案
相关题目
用如图所示装置进行下列实验,能达到实验目的是( )
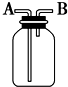

| A、瓶中盛有适量浓H2SO4,从A口进气来干燥NH3 |
| B、从B口进气,用排空气法收集CO2 |
| C、瓶中盛满水,从B口进气,用排水法收集NO2 |
| D、瓶中装满水,A口连接导管并伸入量筒中,从B口进气,用排水法测量生成H2的体积 |
某同学量取50ml 0.5mol/LNaOH溶液和30ml 0.5mol/L H2SO4溶液做中和热实验,测得中和热数据比57.3kJ?mol-1大,其原因可能是( )
| A、实验装置保温、隔热效果差 |
| B、量取NaOH溶液的体积时仰视读数 |
| C、分多次把NaOH溶液倒入盛有硫酸的小烧杯中 |
| D、用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度 |
下列可逆反应达平衡状态后,降温可以使混和气体平均相对分子质量减小的是( )
| A、H2(气)+Br2(气)?2HBr(气) (正反应为放热反应) |
| B、N2(气)+3H2(气)?2NH3(气) (正反应为放热反应) |
| C、2SO3(气)?2SO2(气)+O2(气) (正反应为吸热反应) |
| D、4NH3(气)+5O2(气)?4NO(气)+6H2O(气) (正反应为放热反应) |

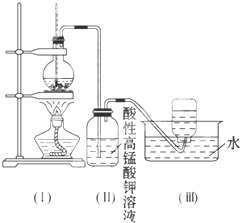 如图所示,在实验室里,通常利用浓硫酸与乙醇混合加热制乙烯:CH3CH2OH
如图所示,在实验室里,通常利用浓硫酸与乙醇混合加热制乙烯:CH3CH2OH