题目内容
16.二氯化二硫(S2C12)可用作橡胶工业的硫化剂,常温下它是橙黄色有恶臭的液体,它的分子结构与H2O2相似,熔点为l93K,沸点为41lK,遇水很容易水解,产生的气体能使品红褪色,S2C12可由干燥的氯气通入熔融的硫中制得.下列有关说法正确的是( )| A. | S2C12晶体中存在离子键和非极性共价键 | |
| B. | S2C12分子中各原子均达到8电子稳定结构 | |
| C. | S2C12在熔融状态下能导电 | |
| D. | S2C12与水反应后生成的气体难溶于水 |
分析 S2Cl2的分子结构与H2O2相似,熔点为193K,沸点为411K,熔沸点较低,则存在分子,应为共价化合物,对应晶体为分子晶体,S2Cl2的电子式为 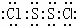 ,根据反应物和生成物写出水解方程式,以此解答该题.
,根据反应物和生成物写出水解方程式,以此解答该题.
解答 解:A.S2Cl2晶体熔沸点较低,应为分子晶体,则一定不存在离子键,故A错误;
B.S2Cl2的电子式为 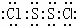 ,分子中各原子均达到8电子稳定结构,故B正确;
,分子中各原子均达到8电子稳定结构,故B正确;
C.S2Cl2为分子晶体,在液态下不能电离出自由移动的离子,则不能导电,故C错误;
D.S2Cl2溶于水H2O反应产生的气体能使品红褪色,则水解方程式为:2S2Cl2+2H2O=SO2↑+3S↓+4HCl,水解生成的气体易溶于水,故D错误.
故选B.
点评 本题以S2Cl2的结构为载体,为高频考点,侧重考查学生的分析能力,考查分子结构、化学键、水解反应等,难度不大,是对基础知识的综合运用与学生能力的考查,注意基础知识的全面掌握.

练习册系列答案
相关题目
6.下列几种气体(括号内为溶剂或反应物溶液)按如图所示装置进行实验,不能看到喷泉现象的是( ) 

| A. | HCl(H2O) | B. | CO2(H2O) | C. | SO2(NaOH溶液) | D. | NH3(KCl溶液) |
7.对于反应IBr+H2O=HBr+HIO的说法正确的是( )
| A. | IBr只作氧化剂 | B. | IBr只作还原剂 | ||
| C. | IBr既不是氧化剂,又不是还原剂 | D. | IBr既是氧化剂,又是还原剂 |
11.已知二氯化二硫(S2Cl2)的结构式为Cl-S-S-Cl,它易与水反应:2S2Cl2+2H2O═4HCl+SO2↑+3S↓ 对该反应的说法正确的是( )
| A. | 还原剂与氧化剂的物质的量之比为3:1 | |
| B. | H2O既不作氧化剂又不作还原剂 | |
| C. | 每生成1 mol SO2转移4 mol电子 | |
| D. | S2Cl2只作氧化剂 |
1.用惰性电极电解下列溶液一段时间后再加入一定量的某种纯净物(括号内的物质),能使溶液恢复到原来的成分和浓度的是( )
| A. | AgNO3(AgNO3) | B. | NaOH(NaOH) | C. | NaCl(NaCl) | D. | CuCl2(CuCl2) |
8.A元素原子的L层比B元素原子的L层少3个电子,B元素原子核外电子数比A元素总电子数多5个,则A、B可形成( )
| A. | 共价化合物B2A3 | B. | 离子化合物B2A3 | C. | 共价化合物B3A2 | D. | 离子化合物B3A2 |
5.在bXm-和aYn+两种微粒,它们的电子层结构相同,则a,m,n,b的关系是( )
| A. | a=b-m-n | B. | b+m+n=a | C. | a=b-m+n | D. | m-n+b=a |
5.下列各原子构成的单质中,肯定能与稀盐酸反应放出H2的是( )
| A. | 形成化合物种类最多的原子 | |
| B. | M层有5个电子的原子 | |
| C. | N层上电子数与K层电子数相等,次外层有8个电子的原子 | |
| D. | 原子核外最外层电子数等于电子层数的原子 |
