题目内容
7.填写如表中各溶液的PH与氢离子,氢氧根浓度(25℃)| C(H+)mol•L-1 | C(OH-)mol•L-1 | PH | |
| 溶液1 | 1×10-4 | 1×10-10 | 4 |
| 溶液2 | 1×10-7 | 1×10-7 | 7 |
| 溶液3 | 1×10-9 | 1×10-5 | 9 |
分析 25℃时水的离子积为Kw=c(H+)•c(OH-)=10-14,然后根据c(H+)=$\frac{{K}_{w}}{c(O{H}^{-})}$、c(OH-)=$\frac{{K}_{w}}{c({H}^{+})}$、pH=-lgc(H+)对各溶液进行计算.
解答 解:25℃时水的离子积为Kw=c(H+)•c(OH-)=10-14,
溶液1中,c(H+)=1×10-4mol/L,则c(OH-)=$\frac{{K}_{w}}{c({H}^{+})}$=$\frac{1×1{0}^{-14}}{1{0}^{-4}}$mol/L=1×10-10mol/L,该溶液的pH=-lgc(H+)=-lg1×10-4=4;
溶液2中,c(OH-)=1×10-7mol/L,则c(H+)=$\frac{{K}_{w}}{c(O{H}^{-})}$=$\frac{1×1{0}^{-14}}{1×1{0}^{-7}}$mol/L=1×10-7mol/L,该溶液的pH=-lgc(H+)=-lg1×10-7=7;
溶液3中,pH=9,根据pH=-lgc(H+)可知:c(H+)=10-pH=1×10-9mol/L,c(OH-)=$\frac{{K}_{w}}{c({H}^{+})}$=$\frac{1×1{0}^{-14}}{1×1{0}^{-9}}$mol/L=1×10-5mol/L,
故答案为:
| C(H+)mol•L-1 | C(OH-)mol•L-1 | PH | |
| 溶液1 | 1×10-10 | ||
| 溶液2 | 1×10-7 | 7 | |
| 溶液3 | 1×10-9 | 1×10-5 |
点评 本题考查了溶液pH的简单计算,题目难度不大,明确溶液水的离子积的表达式为解答关键,注意掌握溶液pH的概念及计算方法,试题培养了学生的化学计算能力.

练习册系列答案
 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案
相关题目
18.向盛有10mL 1mol•L-1 NH4Al(SO4)2溶液的烧杯中滴加20mL 1.2mol•L-1 Ba(OH)2溶液,充分反应后,溶液中产生沉淀的质量为( )
| A. | 4.816g | B. | 0.78g | C. | 4.66g | D. | 5.44g |
2.固体混和物,可能含有氯化钙、碳酸铵、烧碱、硫酸铵,将它溶解于水得到无色澄清的溶液,无其它明显现象,向溶液中加入硝酸钡溶液,产生白色沉淀,再加入硝酸沉淀部分溶解,则原混合物肯定有( )
| A. | CaCl2和(NH4)2SO4 | B. | (NH4)2SO4和(NH4)2CO3 | ||
| C. | NaOH和CaCl2 | D. | NaOH和(NH4)2SO4 |
6.2010年8月7日,甘肃甘南藏族自治州舟曲县发生特大泥石流,造成大量人员伤亡,其中饮用水安全在灾后重建中占有极为重要的地位,某研究小组提取三处被污染的水源进行了如下分析:并给出了如下实验信息:其中一处被污染的水源含有A、B两种物质,一处含有C、D两种物质,一处含有E物质,A、B、C、D、E五种常见化合物都是由如表中的离子形成的:
为了鉴别上述化合物,分别完成以下实验,其结果是:
①将它们溶于水后,D为蓝色溶液,其他均为无色溶液.
②将E溶液滴入到C溶液中,出现白色沉淀,继续滴加沉淀溶解.
③进行焰色反应,只有B、C为紫色(透过蓝色钴玻璃).
④在各溶液中加入Ba(NO3)2溶液,再加入过量稀硝酸,A中放出无色气体,C、D中产生白色沉淀.
⑤将B、D两溶液混合,未见沉淀或气体生成.
根据上述实验现象填写下列空白:
(1)写出化学式:ANaHCO3、BKNO3、CKAl(SO4)2、DCuSO4.
(2)将含1mol A的溶液与含1mol E的溶液反应后蒸干,仅得到一种化合物,该化合物为Na2CO3.
(3)写出实验②发生反应的离子方程式Al3++3OH-═Al(OH)3↓、Al(OH)3+OH-═AlO2-+2H2O.
(4)C常用作净水剂,用离子方程式表示其净水原理Al3++3H2O═Al(OH)3(胶体)+3H+.
| 阳离子 | K+、Na+、Cu2+、Al3+ |
| 阴离子 | SO${\;}_{4}^{2-}$、HCO${\;}_{3}^{-}$、NO${\;}_{3}^{-}$、OH- |
①将它们溶于水后,D为蓝色溶液,其他均为无色溶液.
②将E溶液滴入到C溶液中,出现白色沉淀,继续滴加沉淀溶解.
③进行焰色反应,只有B、C为紫色(透过蓝色钴玻璃).
④在各溶液中加入Ba(NO3)2溶液,再加入过量稀硝酸,A中放出无色气体,C、D中产生白色沉淀.
⑤将B、D两溶液混合,未见沉淀或气体生成.
根据上述实验现象填写下列空白:
(1)写出化学式:ANaHCO3、BKNO3、CKAl(SO4)2、DCuSO4.
(2)将含1mol A的溶液与含1mol E的溶液反应后蒸干,仅得到一种化合物,该化合物为Na2CO3.
(3)写出实验②发生反应的离子方程式Al3++3OH-═Al(OH)3↓、Al(OH)3+OH-═AlO2-+2H2O.
(4)C常用作净水剂,用离子方程式表示其净水原理Al3++3H2O═Al(OH)3(胶体)+3H+.
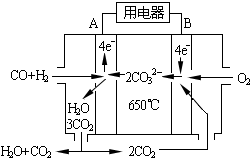 (6)工业上可回收CO作燃料.如图是MCFC燃料电池,它是以水煤气(CO、H2)为燃料,一定比例Li2CO3和Na2CO3低熔混合物为电解质.A为电池的负(填“正”或“负”)极,写出B极电极反应式:2CO2+O2+4e-=2CO32-.
(6)工业上可回收CO作燃料.如图是MCFC燃料电池,它是以水煤气(CO、H2)为燃料,一定比例Li2CO3和Na2CO3低熔混合物为电解质.A为电池的负(填“正”或“负”)极,写出B极电极反应式:2CO2+O2+4e-=2CO32-.