题目内容
17.已知:R-CH=CH-O-R′$\stackrel{H_{2}O/H+}{→}$ R-CH2CHO+R′OH(烃基烯基醚)烃基烯基醚A的相对分子质量为176,分子中碳氢原子数目比为3:4.与A相关的反应如图:
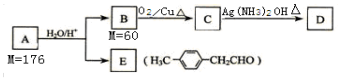
请回答下列问题:
(1)A的分子式为C12H16O,B的名称是1-丙醇(或正丙醇).
(2)写出C→D反应的化学方程式:CH3CH2CHO+2Ag(NH3)2OH$\stackrel{△}{→}$CH3CH2COONH4+2Ag↓+3NH3↑+H2O.
(3)链烃M的相对分子质量比B多24,分子中所有碳原子均在同一平面上,其结构简式是(CH3)2C=C(CH3)2.
分析 利用信息可知A的分子式可写为(C3H4)nO,则:40n+16=176,n=4,所以A的分子式为C12H16O,由信息可知,A反应生成B为醇,E为醛,B的相对分子质量为60,则B为CH3CH2CH2OH,B→C发生催化氧化反应,所以C为CH3CH2CHO,C→D为银镜反应,则D为CH3CH2COONH4,由B、E结构及信息可知,A为 ,以此解答该题.
,以此解答该题.
解答 解:(1)由上述分析可知,A的分子式为C12H16O,B为CH3CH2CH2OH,名称为1-丙醇(或正丙醇),
故答案为:C12H16O;1-丙醇(或正丙醇);
(2)C→D反应的化学方程式为:CH3CH2CHO+2Ag(NH3)2OH$\stackrel{△}{→}$CH3CH2COONH4+2Ag↓+3NH3↑+H2O,
故答案为:CH3CH2CHO+2Ag(NH3)2OH$\stackrel{△}{→}$CH3CH2COONH4+2Ag↓+3NH3↑+H2O;
(3)链烃M的相对分子质量比B多24,则M相对分子质量为84,分子中C原子最大数目=$\frac{84}{12}$=7,故M为C6H12,分子中所有碳原子均在同一平面上,则分子中含有C=C双键,且不饱和碳原子连接4个甲基,所以M结构简式为(CH3)2C=C(CH3)2,
故答案为:(CH3)2C=C(CH3)2.
点评 本题为有机推断,为高考常见题型,侧重考查考生的阅读、自学能力和思维能力,注意把握有机物的官能团的转化,难度不大.

练习册系列答案
 培优三好生系列答案
培优三好生系列答案 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案
相关题目
8.${\;}_{16}^{35}$S可用于治疗软骨肉瘤,下列关于${\;}_{16}^{35}$S的说法错误的是( )
| A. | 质量数35 | B. | 中子数19 | C. | 核电荷数35 | D. | 质子数16 |
12.设NA为阿伏加德罗常数的值.下列说法不正确的是( )
| A. | 常温常压下,35.5g的氯气与足量的氢氧化钙溶液完全反应,转移的电子数为0.5NA | |
| B. | 60g甲酸甲酯和葡萄糖的混合物含有的碳原子数目为2NA | |
| C. | 标准状况下,2.24L PH3与3.4gH2S气体分子所含电子数目均为1.8NA | |
| D. | 已知合成氨反应N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol,当该反应生成NA个NH3分子时,反应放出的热量小于46.2kJ |
2.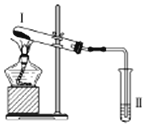 按如图装置进行实验,下列推断正确的是( )
按如图装置进行实验,下列推断正确的是( )
 按如图装置进行实验,下列推断正确的是( )
按如图装置进行实验,下列推断正确的是( )| 选项 | I中试剂 | II中试剂及现象 | 推 断 |
| A | 铁粉与湿棉花 | 肥皂水冒泡 | 铁粉与水蒸气发生了反应 |
| B | 硫酸亚铁 | 品红溶液褪色 | FeSO4分解生成FeO和SO2 |
| C | 涂有石蜡油的碎瓷片 | 酸性高锰酸钾溶液褪色 | 石蜡油分解产物中含有不饱和烃 |
| D | 氯化铵 | 酚酞溶液不变红色 | 氯化铵稳定 |
| A. | A | B. | B | C. | C | D. | D |
9.下列说法不正确的是( )
| A. | 聚乙烯是无毒高分子化合物,可用作食品包装 | |
| B. | 醋和蔗糖的主要成分均为有机物 | |
| C. | 蜜蜂蜇人将蚁酸注入人体可涂抹肥皂缓解 | |
| D. | 人造纤维、合成纤维和光导纤维都是有机高分子化合物 |
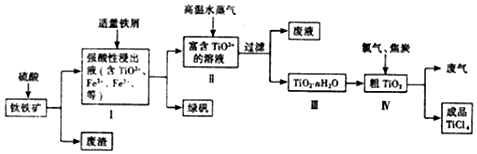
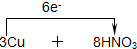 =3Cu(NO3)2+2NO↑+4H2O
=3Cu(NO3)2+2NO↑+4H2O