题目内容
现有如下各说法:
①在水分子中氢、氧原子间以共价键相结合;
②活泼金属和活泼非金属化合时一般形成离子键;
③非金属元素间形成的化合物一定是共价化合物;
④根据电离方程式HCl=H++Cl-,判断HCl分子里存在离子键.上述各种说法正确的是( )
①在水分子中氢、氧原子间以共价键相结合;
②活泼金属和活泼非金属化合时一般形成离子键;
③非金属元素间形成的化合物一定是共价化合物;
④根据电离方程式HCl=H++Cl-,判断HCl分子里存在离子键.上述各种说法正确的是( )
| A、①② | B、①②④ |
| C、①②③④ | D、①③④ |
考点:共价键的形成及共价键的主要类型,离子化合物的结构特征与性质
专题:化学键与晶体结构
分析:①氢、氧原子间以共用电子对成键;
②活泼金属和活泼非金属化合时,一般金属失去电子,非金属得到电子;
③非金属元素间形成的化合物,可能为离子化合物;
④HCl分子中只有共价键.
②活泼金属和活泼非金属化合时,一般金属失去电子,非金属得到电子;
③非金属元素间形成的化合物,可能为离子化合物;
④HCl分子中只有共价键.
解答:
解:①氢、氧原子间以共用电子对成键,则水中存在H-O共价键,故正确;
②活泼金属和活泼非金属化合时,一般金属失去电子,非金属得到电子,则一般形成离子键,可能形成共价键,如氯化铝,故正确;
③非金属元素间形成的化合物,可能为离子化合物,如铵盐为离子化合物,不存在金属元素,故错误;
④HCl分子中只有共价键,HCl溶于水发生电离方程式为HCl=H++Cl-,故错误;
故选A.
②活泼金属和活泼非金属化合时,一般金属失去电子,非金属得到电子,则一般形成离子键,可能形成共价键,如氯化铝,故正确;
③非金属元素间形成的化合物,可能为离子化合物,如铵盐为离子化合物,不存在金属元素,故错误;
④HCl分子中只有共价键,HCl溶于水发生电离方程式为HCl=H++Cl-,故错误;
故选A.
点评:本题考查共价键及物质的分类,为高频考点,把握共价键的形成及物质的化学家、电离等为解答的关键,注重基础知识的考查,题目难度不大.

练习册系列答案
相关题目
下列装置能够组成原电池并发生原电池反应的是( )
A、 稀硫酸 |
B、 稀硫酸 |
C、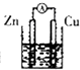 硫酸铜 |
D、 乙醇 |
已知短周期元素X的最外层电子数是电子层数的2倍,则X元素族序数不可能的是( )
| A、0 | B、ⅡA | C、ⅣA | D、ⅥA |
下列说法正确的是( )
| A、“是药三分毒”必须按医嘱或药物说明书使用药物,防范药物不良反应 |
| B、使用青霉素时,有些人可以不进行皮肤敏感试验 |
| C、长期大量使用阿司匹林可预防疾病,没有副作用 |
| D、对于标记“OTC“的药物,必需在医生指导下使用 |
下列物质的化学用语正确的是( )
A、甲烷分子的球棍模型 |
B、CO2的电子式: |
| C、乙酸的最简式:CH2O |
D、S2-的结构示意图: |
甲烷与氯气在光照条件下反应生成的产物最多的是( )
| A、氯化氢 | B、二氯甲烷 |
| C、三氯甲烷 | D、四氯化碳 |
设NA为阿伏加德罗常数的值,下列叙述中正确的是( )
| A、标准状态下,22.4L水中含分子的数目为NA |
| B、11.2L NH3中所含的质子数为5NA |
| C、常温常压下,48g O3含有的氧原子数为3NA |
| D、2.4g金属镁变为镁离子时失去的电子数为0.1NA |
下列说法不正确的是( )
| A、乙醇和乙酸都可以与钠反应生成氢气 |
| B、苯的硝化反应需要水浴加热 |
| C、用溴水鉴别苯和环己烷 |
| D、乙烯和甲烷可用酸性高锰酸钾溶液鉴别 |



