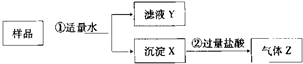
题目内容
A、B、C、D、E、F六种短周期主族元素,它们的原子序数依次增大.已知:A元素的原子半径最小,B元素原子的最外层电子数是内层电子数的2倍,C元素的最高价氧化物对应的水化物与其氢化物反应能生成盐,D与E同主族,E元素原子的最外层电子数比次外层电子数少2.请回答:
(1)元素B的原子结构示意图为 .
(2)元素D的单质与金属钠反应生成的化合物X可作潜水面具中的供氧剂.化合物X的电子式为 ,X中含有的化学键类型有 .
(3)原子数相同,电子数也相同的微粒互为等电子体.互为等电子体的分子,结构相似,物理性质相近.元素B与D能形成两种常见分子,其中一种有毒,根据等电子体原理写出它的结构式 ,另一种是 分子(填“极性”或“非极性”)
(4)D和E两种元素相比较,其原子得电子能力较强的是 (写名称).以下说法中,可以证明上述结论的是 (填写编号).
a.比较这两种元素的常见单质的沸点
b.二者形成的化合物中,D元素显负价
c.比较这两种元素的气态氢化物的稳定性
d.比较这两种元素氢化物的水溶液的酸性
(5)元素A、D、E与钠元素可形成两种酸式盐(均含有这四种元素),这两种酸式盐在水溶液中反应的离子方程式是 .
(6)元素C的氢化物易液化,极易溶于水.试用物质结构理论解释之: .
(1)元素B的原子结构示意图为
(2)元素D的单质与金属钠反应生成的化合物X可作潜水面具中的供氧剂.化合物X的电子式为
(3)原子数相同,电子数也相同的微粒互为等电子体.互为等电子体的分子,结构相似,物理性质相近.元素B与D能形成两种常见分子,其中一种有毒,根据等电子体原理写出它的结构式
(4)D和E两种元素相比较,其原子得电子能力较强的是
a.比较这两种元素的常见单质的沸点
b.二者形成的化合物中,D元素显负价
c.比较这两种元素的气态氢化物的稳定性
d.比较这两种元素氢化物的水溶液的酸性
(5)元素A、D、E与钠元素可形成两种酸式盐(均含有这四种元素),这两种酸式盐在水溶液中反应的离子方程式是
(6)元素C的氢化物易液化,极易溶于水.试用物质结构理论解释之:
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:A、B、C、D、E、F六种短周期主族元素,它们的原子序数依次增大,A元素的原子半径最小,则A为H元素;
B元素原子的最外层电子数是内层电子数的2倍,则B为C元素;
C元素的最高价氧化物对应的水化物与其氢化物反应能生成盐,则C为N元素;
D与E同主族,E元素原子的最外层电子数比次外层电子数少2,则D为O元素,E为S元素;
因为F为短周期元素,原子序数大于S,所以F为Cl元素,
根据以上分析可知:A为H元素、B为C元素、C为N元素、D为O元素、E为S元素、F为Cl元素,据此完成各题.
B元素原子的最外层电子数是内层电子数的2倍,则B为C元素;
C元素的最高价氧化物对应的水化物与其氢化物反应能生成盐,则C为N元素;
D与E同主族,E元素原子的最外层电子数比次外层电子数少2,则D为O元素,E为S元素;
因为F为短周期元素,原子序数大于S,所以F为Cl元素,
根据以上分析可知:A为H元素、B为C元素、C为N元素、D为O元素、E为S元素、F为Cl元素,据此完成各题.
解答:
解:A、B、C、D、E、F六种短周期主族元素,它们的原子序数依次增大,A元素的原子半径最小,则A为氢元素,B元素原子的最外层电子数是内层电子数的2倍,则B为碳元素,C元素的最高价氧化物对应的水化物与其氢化物反应能生成盐,则C为氮元素,D与E同主族,E元素原子的最外层电子数比次外层电子数少2,则D为氧元素,E为硫元素,因为F为短周期元素,原子序数大于硫,所以F为氯元素,
根据以上分析可知:A为H元素、B为C元素、C为N元素、D为O元素、E为S元素、F为Cl元素,
(1)B为C元素,核电荷数为6,最外层含有4个电子,其原子结构示意图为: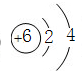 ,
,
故答案为: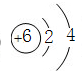 ;
;
(2)元素D的单质与金属钠反应生成的化合物X可作潜水面具中的供氧剂,则化合物X为Na2O2,过氧化钠中含有离子键和非极性共价键,
故答案为:Na2O2;离子键、非极性共价键;
(3)B为C元素、D为O元素,C和O形成的两种化合物为CO和二氧化碳,其中CO有毒,CO分子中含有两个原子、14个电子,与氮气互为等电子体,氮气分子中存在氮氮三键,则CO中存在碳氧三键,一氧化碳的结构式为:C≡O;
二氧化碳为直线型结构,是由极性键构成的非极性分子,
故答案为:C≡O;非极性;
(4)D为O元素、E为S元素,O和S两种元素相比较,其原子得电子能力较强的是氧,要证明这一结论,
a.单质的沸点与得电子能力无关,故a错误;
b.二者形成的化合物中,O元素的原子显负价,说明氧得电子能力强,故b正确;
c.得电子能力越强,气态氢化物越稳定,故c正确;
d.氢化物的水溶液的酸性不能说明得电子能力强弱,故d错误;
故答案为:氧;bc;
(5)A为H元素、B为C元素、D为O元素,元素A、D、E与钠元素可形成两种酸式盐为硫酸氢钠和亚硫酸氢钠,这两种酸式盐在水溶液中反应生成硫酸钠、二氧化硫气体和水,反应的离子方程式是:H++HSO3-═SO2↑+H2O,
故答案为:H++HSO3-═SO2↑+H2O;
(6)元素C为N,元素C的氢化物为氨气,氨气易液化是因为氨气分子间存在氢键,中心原子(N)半径较小,对H原子吸引能力强,可以吸引其它氨气分子的H原子;
氨气易溶于水是基于相似相容原理,氨气和水都是极性分子,而且都可以形成氢键,故而加大的溶解度,
故答案为:氨气易液化是由于氨气分子中存在氢键,易溶于水是氨气为极性分子,极性分子易溶于极性溶剂水,且可以形成氢键.
根据以上分析可知:A为H元素、B为C元素、C为N元素、D为O元素、E为S元素、F为Cl元素,
(1)B为C元素,核电荷数为6,最外层含有4个电子,其原子结构示意图为:
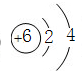 ,
,故答案为:
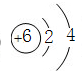 ;
; (2)元素D的单质与金属钠反应生成的化合物X可作潜水面具中的供氧剂,则化合物X为Na2O2,过氧化钠中含有离子键和非极性共价键,
故答案为:Na2O2;离子键、非极性共价键;
(3)B为C元素、D为O元素,C和O形成的两种化合物为CO和二氧化碳,其中CO有毒,CO分子中含有两个原子、14个电子,与氮气互为等电子体,氮气分子中存在氮氮三键,则CO中存在碳氧三键,一氧化碳的结构式为:C≡O;
二氧化碳为直线型结构,是由极性键构成的非极性分子,
故答案为:C≡O;非极性;
(4)D为O元素、E为S元素,O和S两种元素相比较,其原子得电子能力较强的是氧,要证明这一结论,
a.单质的沸点与得电子能力无关,故a错误;
b.二者形成的化合物中,O元素的原子显负价,说明氧得电子能力强,故b正确;
c.得电子能力越强,气态氢化物越稳定,故c正确;
d.氢化物的水溶液的酸性不能说明得电子能力强弱,故d错误;
故答案为:氧;bc;
(5)A为H元素、B为C元素、D为O元素,元素A、D、E与钠元素可形成两种酸式盐为硫酸氢钠和亚硫酸氢钠,这两种酸式盐在水溶液中反应生成硫酸钠、二氧化硫气体和水,反应的离子方程式是:H++HSO3-═SO2↑+H2O,
故答案为:H++HSO3-═SO2↑+H2O;
(6)元素C为N,元素C的氢化物为氨气,氨气易液化是因为氨气分子间存在氢键,中心原子(N)半径较小,对H原子吸引能力强,可以吸引其它氨气分子的H原子;
氨气易溶于水是基于相似相容原理,氨气和水都是极性分子,而且都可以形成氢键,故而加大的溶解度,
故答案为:氨气易液化是由于氨气分子中存在氢键,易溶于水是氨气为极性分子,极性分子易溶于极性溶剂水,且可以形成氢键.
点评:本题主要考查了位置、结构与性质的关系,题目难度中等,试题涉及原子结构示意图、离子方程式、元素周期律等知识,内容较多、综合性较强,元素推断是解题关键,解题要注意基础知识的灵活运用.

练习册系列答案
相关题目
已知3.01×1023个X气体分子的质量为32g,则X气体的摩尔质量是( )
| A、16g |
| B、32g |
| C、64g/mol |
| D、32g/mol |
将某Mg-Al合金放入足量的盐酸中,生成H2 的体积在标况下是2240ml;同质量的Mg-Al合金放入足量的NaOH溶液中生成H2 的体积在标况下是2016ml,则Mg、Al的质量之比是( )
| A、1:1 | B、6:1 |
| C、1:6 | D、4:27 |
某条件下锌与稀硝酸反应时其物质的量之比为5:12,则此时硝酸的还原物是( )
| A、NO2 |
| B、NO |
| C、N2O |
| D、N2 |
X、Y、Z、W均为常见的烃的含氧衍生物且物质类别不同,存在如图所示的转化关系,则以下判断正确的是( )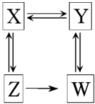

| A、X是羧酸,Y是酯 |
| B、Z是醛,W是羧酸 |
| C、Y是醛,W是醇 |
| D、X是醇,Z是酯 |