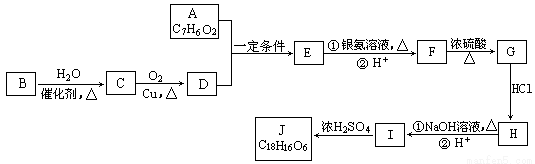
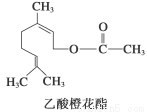
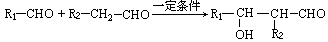题目内容
4.6g铜镁合金完全溶解于100mL密度为1.40g·mL-1、质量分数为63%的浓硝酸中,得到4480mLNO2和336 mLN2O4 的混合气体(标准状况),向反应后的溶液中加入1.0mol·L-1NaOH溶液至离子恰好全部沉淀时,下列说法不正确的是
A.该合金中铜与镁的物质的量之比是46:69
B.该浓硝酸中HNO3的物质的量浓度是14.0mol·L-1
C.产生沉淀8.51 g
D.离子恰好完全沉淀时,加入NaOH溶液的体积是230mL
D
【解析】
试题分析:A.4480mL NO2的物质的量=4.48L÷22.4L/mol=0.2mol,336mLN2O4的物质的量=0.336L÷22.4L/mol=0.015mol,令Cu、Mg的物质的量分别为xmol、ymol,根据二者质量与电子转移守恒,可得:64x+24y=4.6, 2x+2y=0.2+0.015×2,解得x=0.046、y=0.069,故该合金中铜与镁的物质的量之比=0.046mol:0.069mol=46:69,正确;B、密度为1.40g/mL、质量分数为63%的浓硝酸.其物质的量浓度=1000×1.4×63%/63 mol/L=14mol/L,正确;C、铜镁合金完全溶解于浓硝酸中,向反应后的溶液中加入NaOH溶液至离子恰好全部沉淀,生成沉淀为Cu(OH)2、Mg(OH)2,由化学式可知n(OH-)2=n(Cu)+2n(Mg)=2×(0.046mol+0.069mol)=0.23mol,故沉淀质量=m(Cu)+m(Mg)+m(OH-)=4.6g+0.23mol×17g/mol=8.51g,正确;D、离子恰好完全沉淀时,此时溶液中溶质为NaNO3,根据N元素守恒可知n原(HNO3)=n(NaNO3)+n(NO2)+2n(N2O4),故n(NaNO3)=0.1L×14mol/L-0.2mol-2×0.015mol=1.17mol,根据钠离子守恒有n(NaOH)=n(NaNO3)=1.17mol,故需要氢氧化钠溶液的体积=1.17mol÷1mol/L=1.17L=1170mL,错误。
考点:本题考查化合物的有关计算。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案(10分)信息时代产生的大量电子垃圾对环境构成严重威胁。某研究性学习小组将一批废弃的线路板简单处理后,得到含Cu、Fe及少量Au、Pt等金属的混合物,并用如下流程制备胆矾晶体(CuSO4?5H2O):
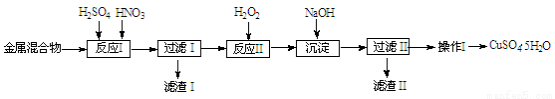
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
阳离子 | Fe3+ | Fe2+ | Cu2+ |
开始沉淀 | 1.5 | 6.4 | 4.2 |
完全沉淀 | 3.2 | 8.9 | 6.7 |
(1)滤渣Ⅰ的主要成份是(写化学式)__________。
(2)反应Ⅱ中加入H2O2的作用是___________________。
(3)生成沉淀反应的离子方程式有______________________。
(4)操作Ⅰ的步骤是 、过滤、洗涤、干燥。
(5)测定胆矾晶体纯度的实验步骤如下:
A. 准确称取3.125g胆矾晶体样品配成100mL溶液;
B. 取10.00 mL溶液于带塞锥形瓶中,加适量水稀释,加入过量KI固体,发生反应:2Cu2+ +4Iˉ= 2CuI↓ + I2
C. 继续向上述混合物中,逐滴加入0.1000 mol·L-1Na2S2O3溶液至恰好完全反应,共消耗12. 00mL Na2S2O3溶液:I2+2S2O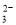 = 2Iˉ+S4O
= 2Iˉ+S4O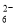 , 则样品中胆矾晶体的质量分数______。
, 则样品中胆矾晶体的质量分数______。
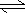 H++HA-,HA-
H++HA-,HA- 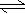 H++A2-
H++A2-