题目内容
3.25℃时,pH=9的NaHA溶液中各微粒的物质的量浓度关系正确的是( )| A. | c(A2-)>c(H2A) | B. | c(Na+)+c(H+)=c(OH-)+c(HA-)+2c(A2-) | ||
| C. | c(Na+)=c( HA-)+c(H2A) | D. | c(H+)=c(A2-)+c(OH-) |
分析 NaHA溶液中即存在HA-的电离又存在其水解,pH=9说明其水解程度大于电离程度,据此分析.
解答 解:A、HA-的水解程度大于电离程度,所以c(A2-)<c(H2A),故A错误;
B、据电荷守恒c(Na+)+c(H+)=c(OH-)+c(HA-)+2c(A2-),故B正确;
C、据物料守恒c(Na+)=c(H2A)+c(HA-)+c(A2-),故C错误;
D、据电荷守恒和物料守恒有c(H2A)+c(H+)=c(OH-)+c(A2-),故D错误;
故选B.
点评 本题考查了盐类水解、弱电解质电离平衡影响因素、电解质溶液中电荷守恒和物料守恒分析判断、溶液酸碱性等,掌握基础是解题关键,题目难度中等.

练习册系列答案
相关题目
14.下列变化中,一定要加入适当的还原剂才能实现的是( )
| A. | KMnO4→MnO2 | B. | HCl→Cl2 | C. | Fe2O3→Fe | D. | CaO→CaCO3 |
11.已知在苯分子中,不存在单、双键交替的结构.下列可以作为证据的实验事实是( )
①苯不能使酸性KMnO4溶液褪色
②苯中6个碳碳键完全相同
③苯能在一定条件下与氢气加成生成环己烷
④实验室测得二甲苯只有三种结构
⑤苯分子具有平面正六边形结构( )
①苯不能使酸性KMnO4溶液褪色
②苯中6个碳碳键完全相同
③苯能在一定条件下与氢气加成生成环己烷
④实验室测得二甲苯只有三种结构
⑤苯分子具有平面正六边形结构( )
| A. | ②③④⑤ | B. | ①③④⑤ | C. | ①②③④ | D. | ①②④⑤ |
18.表中的试剂与操作及现象对应关系错误的是( )
| 选项 | 试剂 | 操作及现象 |
| A | 氯水 | 滴加NaOH溶液,溶液颜色褪去,再加浓盐酸,溶液颜色恢复 |
| B | CaCl2 | 向两支盛有CaCl2溶液的试管中分别通入CO2和CO,均无沉淀产生 |
| C | AgNO3 | 滴加氨水,产生沉淀,继续滴加氨水,沉淀溶解 |
| D | 铝粉 | 滴加NaOH溶液,产生气体,继续滴加,产生白色沉淀 |
| A. | A | B. | B | C. | C | D. | D |
8.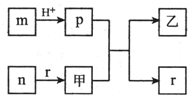 短周期主族元素W、X、Y、Z的原子半径依次增大,且X、Y原子序数之和是W、Z原子序数之和的2倍.m、n、p、r是由这些元素组成的二元化合物,甲、乙是其中两种元素对应的单质,n与乙均是淡黄色固体.上述物质的转化关系如图所示(部分反应物或生成物省略).下列说法错误的是( )
短周期主族元素W、X、Y、Z的原子半径依次增大,且X、Y原子序数之和是W、Z原子序数之和的2倍.m、n、p、r是由这些元素组成的二元化合物,甲、乙是其中两种元素对应的单质,n与乙均是淡黄色固体.上述物质的转化关系如图所示(部分反应物或生成物省略).下列说法错误的是( )
 短周期主族元素W、X、Y、Z的原子半径依次增大,且X、Y原子序数之和是W、Z原子序数之和的2倍.m、n、p、r是由这些元素组成的二元化合物,甲、乙是其中两种元素对应的单质,n与乙均是淡黄色固体.上述物质的转化关系如图所示(部分反应物或生成物省略).下列说法错误的是( )
短周期主族元素W、X、Y、Z的原子半径依次增大,且X、Y原子序数之和是W、Z原子序数之和的2倍.m、n、p、r是由这些元素组成的二元化合物,甲、乙是其中两种元素对应的单质,n与乙均是淡黄色固体.上述物质的转化关系如图所示(部分反应物或生成物省略).下列说法错误的是( )| A. | 热稳定性:p<r | |
| B. | X与Y组成的化合物一定有漂白性 | |
| C. | 含Y元素的盐溶液可能显酸性、中性或碱性 | |
| D. | Z与W、X、Y可形成离子化合物 |
15.能正确表示下列反应的离子方程式的是( )
| A. | 钠与水反应:2Na+2H2O═2Na++2OH-+H2↑ | |
| B. | 钠与CuSO4溶液反应:2Na+Cu2+═Cu+2Na+ | |
| C. | 钠与盐酸反应:2Na+2H2O═2Na++2OH-+H2↑ | |
| D. | 铝跟氢氧化钠溶液反应:2Al+2OH-+2H2O═2AlO2-+H2↑ |
12.下列有关电解质溶液中,物质的量浓度关系错误的是( )
| A. | pH=2的HA溶液与pH=12的MOH溶液任意比混合:c(H+)+c(M+ )=c(OH- )+c(A- ) | |
| B. | 25℃时,pH=4.7浓度均为0.1mol•L-1的CH3COOH、CH3COONa混合溶液中:(CH3COO-)+c(OH-)>c(CH3COOH)+c(H+) | |
| C. | 氢硫酸的酸性比碳酸弱,则NaHS溶液中:c(Na+)>c(HS-)>c(H+)>c(OH-) | |
| D. | ①0.2mol•L-1NH4Cl溶液②0.1mol•L-1(NH4)2Fe(SO4)2溶液③0.2mol•L-1NH4HSO4溶液④0.1mol•L-1(NH4)2CO3溶液中,c(NH4+ )大小:③>②>①>④ |
6.在体积为2L的恒容密闭容器中加入4molH2和一定量的CO后,发生反应:CO(g)+2H2(g)?CH3OH(g)△H<0,CO和CH3OH (g)的物质的量随时间的变化如下表表示:则下列说法错误的是( )
| t/min | 0 | 3 | 10 | 12 |
| n(CO)/mol | 2 | 1 | 0.5 | 0.5 |
| n(CH3OH)/mol | 0 | 1 | 1.5 | 1.5 |
| A. | 在0~3min内,用H2表示的平均反应速率为0.33mol•L-1•min-1 | |
| B. | 在该条件下,上述反应的平衡常数为3 | |
| C. | 反应达平衡时,CH3OH (g)的体积分数为50% | |
| D. | 要增大反应速率且增大 CH3OH (g)在混合物中的体积分数,可采用压缩体积,增大体系压强的措施 |