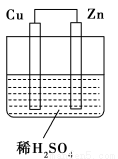
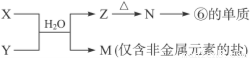
题目内容
下列说法正确的是( )
A.浓硫酸与亚硫酸钠反应制取二氧化硫,体现浓硫酸具有强氧化性
B.铵盐受热易分解,均有NH3产生
C.浓硝酸保存在棕色的细口瓶中
D.化工厂可通过加高烟囱排放废气,防止形成酸雨
C
【解析】
试题分析:A.Na2SO3 + H2SO4(浓)= Na2SO4+SO2↑+H2O.体现了浓硫酸具有强酸性。错误。B.铵盐受热易分解,但不是所有的铵盐分解都有NH3产生。错误。C.浓硝酸光照容易发生分解反应:4HNO3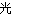 4NO2↑+2H2O。温度越高,浓度越大越容易分解。为了防止浓硝酸分解,所有应该保存在棕色的细口瓶中。正确。D.化工厂通过加高烟囱排放废气,只是减少在本地区的有害气体的含量,但是对于全局的环境保护无任何帮助。错误。
4NO2↑+2H2O。温度越高,浓度越大越容易分解。为了防止浓硝酸分解,所有应该保存在棕色的细口瓶中。正确。D.化工厂通过加高烟囱排放废气,只是减少在本地区的有害气体的含量,但是对于全局的环境保护无任何帮助。错误。
考点:考查物质的性质及应用、环境保护的知识。

练习册系列答案
相关题目
用下图所示装置进行实验,下列对实验现象的解释不合理的是
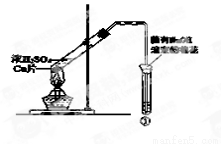
| ①中试剂 | ①中现象 | 解 释 |
A | Ba(NO3)2溶液 | 生成白色沉淀 | SO32-与Ba2+生成白色BaSO3沉淀 |
B | 品红溶液 | 溶液褪色 | SO2具有漂白性 |
C | 紫色石蕊溶液 | 溶液变红 | SO2与水反应生成酸 |
D | 酸性KMnO4溶液 | 紫色褪去 | SO2具有还原性 |