题目内容
6.已知:C(s)+O2(g)=CO2(g)△H1CO2(g)+C(s)=2CO(g)△H2
2CO(g)+O2(g)=2CO2(g)△H3
3CO(g)+Fe2O3(s)=3CO2(g)+2Fe(s)△H4
下列关于上述反应焓变的判断正确的是( )
| A. | △H1>0 | B. | △H2<0 | C. | △H3<0 | D. | △H4<0 |
分析 所有的燃烧反应属于放热反应,
以碳作为还原剂的反应通常为吸热反应,
一氧化碳高温条件下还原氧化铁属于吸热反应;
解答 解:所有的燃烧反应属于放热反应,C(s)+O2(g)=CO2(g)△H1,2 CO(g)+O2(g)=2CO2(g)△H3,△H1<0,△H3<0,
以碳作为还原剂的反应通常为吸热反应,CO2(g)+C(s)=2CO(g)△H2>0,
一氧化碳高温下还原氧化铁属于放热反应,3CO(g)+Fe2O3(s)=3CO2(g)+2Fe(s)△H4 >0,
故C.
点评 本题考查了常见的吸热反应和放热反应类型,难度中等,熟悉常见的吸热反应和放热反应类型,注意知识的积累.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
11.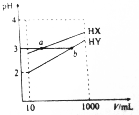 常温下,10mL浓度均为0.1mol/L的HX和HY两种一元酸溶液加水稀释过程中溶液的pH随溶液体积变化曲线如图所示.则下列说法正确的是( )
常温下,10mL浓度均为0.1mol/L的HX和HY两种一元酸溶液加水稀释过程中溶液的pH随溶液体积变化曲线如图所示.则下列说法正确的是( )
 常温下,10mL浓度均为0.1mol/L的HX和HY两种一元酸溶液加水稀释过程中溶液的pH随溶液体积变化曲线如图所示.则下列说法正确的是( )
常温下,10mL浓度均为0.1mol/L的HX和HY两种一元酸溶液加水稀释过程中溶液的pH随溶液体积变化曲线如图所示.则下列说法正确的是( )| A. | HX的电离常数K(HX)大于HY的电离常数K(HY) | |
| B. | a点水的电离程度大于b点水的电离程度 | |
| C. | a、b两点对应的两种酸等体积混合后溶液的pH大于混合前溶液的pH | |
| D. | 浓度均为0.1mol/L的NaX和NaY组成的混合溶液中c(Na+)>c(Y-)>c(X-)>c(OH-)>c(H+) |
11.用下列实验装置进行的实验中,能达到相应实验目的是( )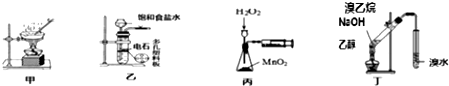

| A. | 用图甲蒸干CuCl2饱和溶液制备CuCl2晶体 | |
| B. | 用图乙制取乙炔气体 | |
| C. | 丙装置可定量测定 H2O2的分解速率 | |
| D. | 丁可用于证明实验中生成了乙烯 |
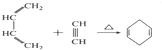
18.某有机化合物,只含碳、氢、氧三种元素中的两种或三种,相对分子质量为74,完全燃烧时产生等物质的量的CO2和H2O.它的分子式可能为( )
| A. | C4H10O | B. | C4H4O2 | C. | C3H6O2 | D. | C4H8O2 |
15.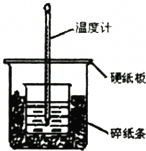 某实验小组用0.50mol/L NaOH溶液和0.50mol/L硫酸溶液进行中和热的测定.
某实验小组用0.50mol/L NaOH溶液和0.50mol/L硫酸溶液进行中和热的测定.
(1)从实验装置上看,图中尚缺少的一种玻璃用品是环形玻璃搅拌棒,仍存在的缺陷是大小烧杯间未用碎纸条填满,大小烧杯杯口未平.
(2)若将NaOH溶液改为相同体积、相同浓度的氨水,测得中和热为△H1,则△H1与△H的关系为:△H1>△H(填“<”、“>”或“=”).
(3)写出该反应的中和热的热化学方程式(中和热为57.3kJ/mol):NaOH(aq)+1/2H2SO4(aq)=l/2Na2SO4(aq)+H2O(aq)AH=-57.3kJ•mol-1.
(4)取50mL NaOH溶液和30mL硫酸溶液进行实验,装置已做改进.实验数据如表.
又已知0.50mol/L NaOH溶液和0.50mol/L硫酸溶液的密度都近似为1g/cm3,中和后生成溶液的比热容c=4.18J/(g•℃).则中和热△H=-43.5kJ.mol-1(取小数点后一位).
(5)上述实验数值结果与57.3kJ/mol有偏差,产生偏差的原因可能是(填字母)acd.
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把H2SO4溶液倒入盛有NaOH溶液的小烧杯中
d.用温度计测定NaOH溶液起始温度后未清洗直接测定H2SO4溶液的温度
e.实验当天气温较高.
 某实验小组用0.50mol/L NaOH溶液和0.50mol/L硫酸溶液进行中和热的测定.
某实验小组用0.50mol/L NaOH溶液和0.50mol/L硫酸溶液进行中和热的测定.(1)从实验装置上看,图中尚缺少的一种玻璃用品是环形玻璃搅拌棒,仍存在的缺陷是大小烧杯间未用碎纸条填满,大小烧杯杯口未平.
(2)若将NaOH溶液改为相同体积、相同浓度的氨水,测得中和热为△H1,则△H1与△H的关系为:△H1>△H(填“<”、“>”或“=”).
(3)写出该反应的中和热的热化学方程式(中和热为57.3kJ/mol):NaOH(aq)+1/2H2SO4(aq)=l/2Na2SO4(aq)+H2O(aq)AH=-57.3kJ•mol-1.
(4)取50mL NaOH溶液和30mL硫酸溶液进行实验,装置已做改进.实验数据如表.
| 起始温度/℃ | 终止温度/℃ | 温度差/℃ | |||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 25.5 | 25.0 | 25.25 | 28.5 | 3.25 |
| 2 | 24.5 | 24.2 | 24.35 | 27.6 | 3.25 |
| 3 | 25.0 | 24.5 | 24.75 | 26.5 | 1.75 |
(5)上述实验数值结果与57.3kJ/mol有偏差,产生偏差的原因可能是(填字母)acd.
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把H2SO4溶液倒入盛有NaOH溶液的小烧杯中
d.用温度计测定NaOH溶液起始温度后未清洗直接测定H2SO4溶液的温度
e.实验当天气温较高.

 B.
B.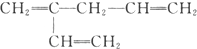 C.
C.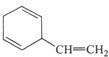 D.
D.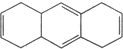
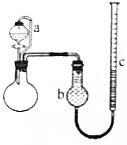 某研究性学习小组为了测定镀锌薄铁板(假设只含Fe和Zn)中锌的质量分数ω(Zn),用如图所示装置(夹持装置略去)进行实验,通过测定产生H2的体积计算ω(Zn).已知:①锌易溶于强碱溶液,发生反应为Zn+2NaOH═Na2ZnO2+H2↑.②所用的镀锌薄铁板均为m1g.回答下列问题:
某研究性学习小组为了测定镀锌薄铁板(假设只含Fe和Zn)中锌的质量分数ω(Zn),用如图所示装置(夹持装置略去)进行实验,通过测定产生H2的体积计算ω(Zn).已知:①锌易溶于强碱溶液,发生反应为Zn+2NaOH═Na2ZnO2+H2↑.②所用的镀锌薄铁板均为m1g.回答下列问题: