题目内容
3.在反应3Cl2+2FeBr2═2FeCl3+2Br2中被还原的元素是( )| A. | Fe | B. | Fe和Cl | C. | Cl | D. | Br |
分析 氧化还原反应中,若某元素的化合价降低,则得到电子,被还原,以此来解答.
解答 解:2FeBr2+3Cl2═2FeCl3+2Br2的反应中,Cl元素的化合价由0价降低为-1价,Fe元素的化合价由+2价升高为+3价,Br元素的化合价由-1价升高为0,则Cl元素得到电子被还原,
故选C.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化反应的考查,注意从元素化合价角度分析,题目难度不大.

练习册系列答案
相关题目
13.下列关于有机化合物的叙述中不正确的是( )
| A. | 甲烷中的任意三个原子都不共面 | |
| B. | CH2Cl2是纯净物说明甲烷是四面体结构而不是正方形结构 | |
| C. | 天然气、沼气、坑道气的主要成分均是甲烷 | |
| D. | 丙烷和甲烷一样能与氯气发生取代反应 |
14.向某溶液中投入铝片后有大量H2放出,则溶液中不可能大量存在的离子是( )
| A. | Cl- | B. | Na+ | C. | NO3- | D. | HCO-3 |
11.下列说法正确的是( )
| A. | 实验桌上的酒精灯倾倒并燃烧起来,应马上用水扑灭 | |
| B. | 分液操作时,分液漏斗中的下层液体从下口放出后再将上层液体从下口放出到另一烧杯中 | |
| C. | 用试管夹从试管底由下往上夹住距离管口约$\frac{1}{3}$处,手持试管夹长柄末端进行加热 | |
| D. | 为检验某溶液中是否含有NH4+,可在此溶液中加入足量的NaOH溶液,加热后用湿润的蓝色石蕊试纸检验 |
18.下列说法中正确的是( )
| A. | 1mol任何气体都约是22.4L | |
| B. | 1mol气态物质,当体积约为22.4L时,该气体一定处于标准状况下 | |
| C. | 在标准状况下,2mol酒精(CH3CH2OH)的体积为44.8L | |
| D. | 常温常压下,质量为32g的O2含有的原子数为2NA |
15.能够证明某卤代烃中存在氯元素的操作及现象是( )
| A. | 在卤代烃中直接加入稀硝酸酸化的AgNO3溶液,产生白色沉淀 | |
| B. | 加入NaOH的乙醇溶液,加热后加入AgNO3溶液,产生白色沉淀 | |
| C. | 加蒸馏水,充分搅拌后,加入AgNO3溶液,产生白色沉淀 | |
| D. | 加入NaOH溶液,加热一段时间后冷却,加入稀硝酸酸化,然后加入AgNO3溶液,产生白色沉淀 |
12.下列物质中含有非极性键的共价化合物是( )
| A. | 氯气 | B. | 过氧化氢 | C. | 过氧化钠 | D. | 氯化氢 |
13.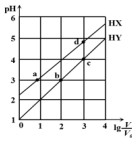 在浓度均为0.1mol/L、体积均为V0的HX、HY,分别加水稀释至体积V,pH随lg$\frac{V}{{V}_{0}}$的变化关系如图所示.下列叙述正确的是( )
在浓度均为0.1mol/L、体积均为V0的HX、HY,分别加水稀释至体积V,pH随lg$\frac{V}{{V}_{0}}$的变化关系如图所示.下列叙述正确的是( )
 在浓度均为0.1mol/L、体积均为V0的HX、HY,分别加水稀释至体积V,pH随lg$\frac{V}{{V}_{0}}$的变化关系如图所示.下列叙述正确的是( )
在浓度均为0.1mol/L、体积均为V0的HX、HY,分别加水稀释至体积V,pH随lg$\frac{V}{{V}_{0}}$的变化关系如图所示.下列叙述正确的是( )| A. | a、b两点的溶液中:c(X-)>c(Y-) | |
| B. | 相同温度下,电离常数K(HX):d>a | |
| C. | 溶液中水的电离程度:d>c>b>a | |
| D. | lg$\frac{V}{{V}_{0}}$=2时,若同时微热两种液体(不考虑HX、HY和H2O的挥发),则$\frac{c({X}^{-})}{c({Y}^{-})}$ 增大 |