题目内容
下列叙述正确的是( )
| A.无论是纯水,还是酸性、碱性或中性稀溶液,在常温下,其c(H+)·c(OH-)=1×10-14 |
| B.c(H+)=1×10-7mol·L-1的溶液一定是中性溶液 |
| C.0.2 mol·L-1CH3COOH溶液中的c(H+)是0.1 mol·L-1CH3COOH溶液中的c(H+)的2倍 |
| D.任何浓度的溶液都可以用pH来表示其酸性的强弱 |
A
KW=c(H+)·c(OH-),且KW只与温度有关,所以,在常温下,纯水、酸性、碱性或中性稀溶液,其KW=1×10-14;在温度不确定时,中性溶液里的c(H+)不一定等于1×10-7mol·L-1;0.2 mol·L-1 CH3COOH溶液中的CH3COOH电离程度比0.1 mol·L-1 CH3COOH溶液中的CH3COOH电离程度小,所以,0.2 mol·L-1 CH3COOH溶液中的c(H+)小于0.1 mol·L-1 CH3COOH溶液中的c(H+)的2倍;当c(H+)或c(OH-)大于1 mol·L-1时,用pH表示溶液的酸碱性就不简便了,所以,当c(H+)或c(OH-)大于1 mol·L-1时,一般不用pH表示溶液的酸碱性,而是直接用c(H+)或c(OH-)来表示。

练习册系列答案
 智能训练练测考系列答案
智能训练练测考系列答案
相关题目
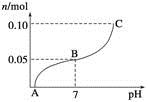
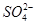 )>c(H+)=c(OH-)
)>c(H+)=c(OH-)
