题目内容
12.将溶质的质量分数为14%的KOH溶液加热蒸发掉100g水后,得到溶质的质量分数为28%的溶液80mL,此时溶液的物质的量浓度为( )| A. | 5 mol/L | B. | 6.25 mol/L | C. | 7 mol/L | D. | 6.75 mol/L |
分析 设14%KOH溶液的质量为m,根据溶质质量不变列方程计算溶液的质量,进而计算溶质的物质的量,根据c=$\frac{n}{V}$计算.
解答 解:设14%KOH溶液的质量为m,则:
m×14%=(m-100g)×28%,
解得m=200g,
m(KOH)=200g×14%=28g,
n(KOH)=$\frac{28g}{56g/mol}$=0.5mol,
c(KOH)=$\frac{0.5mol}{0.08L}$=6.25mol/L,
故选B.
点评 本题考查溶液浓度计算,涉及质量分数、物质的量浓度,侧重于学生的分析能力和计算能力的考查,注意把握相关计算公式的运用,难度不大.

练习册系列答案
相关题目
2.Cu片放入0.1 mol•L-1FeCl3溶液中,反应一定时间后取出Cu片,测得溶液中Fe3+和Fe2+的物质的量浓度为:c(Fe3+):c(Fe2+)=2:3,则溶液中Cu2+与Fe3+的物质的量之比为( )
| A. | 3:2 | B. | 3:5 | C. | 3:4 | D. | 4:3 |
3.精确配制一定物质的量浓度的NaOH溶液,下面实验操作正确的是( )
| A. | 称量时,将NaOH固体放在纸上 | |
| B. | 将称好的NaOH固体放入容量瓶中,加入少量水 | |
| C. | 在烧杯中溶解NaOH固体后,立即将溶液注入容量瓶中 | |
| D. | 将烧杯中已冷却的NaOH溶液注入未经干燥的容量瓶中 |
20.下面是碳在足量的氧气中燃烧的化学方程式,其中正确的是( )
| A. | C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2 | B. | 2C+O2$\frac{\underline{\;点燃\;}}{\;}$2CO | ||
| C. | CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO | D. | 2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2 |
7.足量铜与一定量浓硝酸反应,得到硝酸铜溶液和NO2、N2O4、NO的混合气体,将这些气体与1.68LO2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸.若向所得硝酸铜溶液中加入5mol•L-1NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是( )
| A. | 60mL | B. | 45mL | C. | 30mL | D. | 无法计算 |
17.糖类、油脂、蛋白质和维生素都是人类的基本营养物质.
①有些学生偏食,不爱吃水果、蔬菜,结果营养缺乏、发育不良,这主要是由于摄取维生素(选填“脂肪”、“维生素”或“蛋白质”)不足引起的.
②下表为某品牌燕麦片标签中的一部分.
燕麦片的营养成分中的蛋白质能水解成氨基酸;每克营养物质氧化时放出能量最多的是油脂;葡萄糖在人体内发生氧化反应的化学方程式:C6H12O6+6O2→6CO2+6H2O;人体必需的微量元素是锌.
①有些学生偏食,不爱吃水果、蔬菜,结果营养缺乏、发育不良,这主要是由于摄取维生素(选填“脂肪”、“维生素”或“蛋白质”)不足引起的.
②下表为某品牌燕麦片标签中的一部分.
| 每100g含有 营养成分 | 糖类 | 油脂 | 蛋白质 | 维生素C | 钙 | 镁 | 钠 | 锌 |
| 7.6g | 7.8g | 7.4g | 18mg | 201mg | 18.2mg | 30.8mg | 8.1mg |
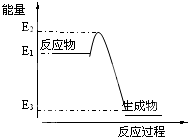
4.下列有关化学反应与能量变化的说法正确的是( )

| A. | 甲烷的燃烧热△H=-890.3kJ•mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+$\frac{3}{2}$O2(g)=CO(g)+2H2O(g)△H=-890.3kJ•mol-1 | |
| B. | 相同条件下,氢气和氧气反应生成液态水比生成等量的气态水所放出的热量少 | |
| C. | 根据图金刚石在一定条件下转化成石墨提供的信息,可知生成物比反应物稳定,向外界放出的热量为E2-E3 | |
| D. | 同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的△H相同 |
8.某元素原子序数为85,下面关于该元素说法不正确的是( )
| A. | 它的银盐不溶于水 | |
| B. | 它的氢化物很不稳定 | |
| C. | 它的单质是白色固体 | |
| D. | 该元素位于元素周期表第六周期、第十七列 |