题目内容
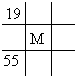
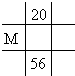
11.下列两种气体的分子数一定不相等的是( )| A. | 质量相等密度不等的N2和C2H4 | B. | 等体积等密度的CO和C2H4 | ||
| C. | 等温、等压,等体积的O2和N2 | D. | 常温常压下,等质量的NO和CO |
分析 根据N=nNA可知,气体分子数目不相等,则二者物质的量不相等.
A.根据n=$\frac{m}{M}$判断;
B.根据m=ρV,n=$\frac{m}{M}$判断;
C.同温同压下,体积之比等于物质的量之比;
D.根据n=$\frac{m}{M}$判断.
解答 解:A.二者的摩尔质量均为28g/mol,由n=$\frac{m}{M}$可知,二者质量相同,则二者物质的量相同,故含有分子数相等,故A不选;
B.相同体积、相同密度,根据m=ρV,可知二者的质量相同,二者摩尔质量相同,则由n=$\frac{m}{M}$可知,质量相同,则物质的量相同,分子数相等,故B不选;
C.相同温度、相同压强、相同体积的O2和N2,物质的量相同,则分子数相同,故C不选;
D.相同质量的NO和CO,二者摩尔质量分别为30g/mol、28g/mol,根据n=$\frac{m}{M}$可知二者的物质的量不同,则含有分子数不同,故D选;
故选D.
点评 本题考查阿伏伽德罗定律及推论,难度不大,注意利用pV=nRT理解阿伏伽德罗定律及推论.

练习册系列答案
相关题目
1.现有某氯化物与氯化镁的混合物,取95mg粉末完全溶于水后,与足量的硝酸银溶液反应后得到300mg氯化银沉淀,则该混合物中的另一氯化物是( )
| A. | NaCl | B. | KCl | C. | CaCl2 | D. | AlCl3 |
2.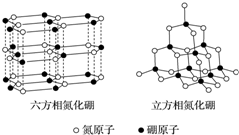 氮化硼(BN)晶体有多种相结构.六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,可作高温润滑剂.立方相氮化硼是超硬材料,有优异的耐磨性.它们的晶体结构如图所示.关于这两种晶体的说法,正确的是( )
氮化硼(BN)晶体有多种相结构.六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,可作高温润滑剂.立方相氮化硼是超硬材料,有优异的耐磨性.它们的晶体结构如图所示.关于这两种晶体的说法,正确的是( )
 氮化硼(BN)晶体有多种相结构.六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,可作高温润滑剂.立方相氮化硼是超硬材料,有优异的耐磨性.它们的晶体结构如图所示.关于这两种晶体的说法,正确的是( )
氮化硼(BN)晶体有多种相结构.六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,可作高温润滑剂.立方相氮化硼是超硬材料,有优异的耐磨性.它们的晶体结构如图所示.关于这两种晶体的说法,正确的是( )| A. | 六方相氮化硼与石墨一样可以导电 | |
| B. | 立方相氮化硼含有σ键和π键,所以硬度大 | |
| C. | 两种晶体均为分子晶体 | |
| D. | 六方相氮化硼晶体层内一个硼原子与相邻氮原子构成的空间构型为平面三角形 |
6.已知短周期元素的离子aW3+、bX+、cY2-、dZ-具有相同的电子层结构,则下列叙述正确的是( )
| A. | 还原性:Z->Y2- | B. | 原子半径:W>X>Y>Z | ||
| C. | 离子半径:Y2->Z->X+>W3+ | D. | 原子序数d>c>b>a |
16.已知下列元素原子的最外层电子排布式,其中不能表示该元素一定为主族元素的是( )
| A. | 3s2 3p3 | B. | 4s2 | C. | 4s2 4p1 | D. | 3s2 3p5 |
3.下列离子在溶液中能大量共存的是( )
| A. | H+、Fe2+、ClO-、Na+ | B. | Na+、H+、SO42-、CO32- | ||
| C. | Fe3+、Cl-、Br-、SCN- | D. | Al3+、NO3-、H+、NH4+ |
1.下列说法正确的是( )
| A. | H2O和H2O2互为同素异形体 | B. | O2和O3互为同位素 | ||
| C. | 乙醇和二甲醚互为同分异构体 | D. | 12C、13C为同一种核素 |