题目内容
106g Na2CO3和84g NaHCO3分别与足量的盐酸溶液反应,其中( )
| A、Na2CO3消耗的盐酸多 |
| B、NaHCO3放出的CO2多 |
| C、Na2CO3放出的CO2多 |
| D、NaHCO3消耗的盐酸多 |
考点:钠的重要化合物
专题:计算题,元素及其化合物
分析:计算106g Na2CO3和84g NaHCO3的物质的量,与足量盐酸发生Na2CO3+2HCl=2NaCl+H2O+CO2↑、NaHCO3+HCl=NaCl+H2O+CO2↑,结合反应的方程式计算该题.
解答:
解:n(Na2CO3)=
=1mol,n(NaHCO3)=
=1mol,
与足量盐酸发生Na2CO3+2HCl=2NaCl+H2O+CO2↑、NaHCO3+HCl=NaCl+H2O+CO2↑,
1mol 2mol 1mol 1mol 1mol 1mol
由反应的方程式可知,Na2CO3消耗的盐酸多,生成的二氧化碳一样多.
故选A.
| 106g |
| 106g/mol |
| 84g |
| 84g/mol |
与足量盐酸发生Na2CO3+2HCl=2NaCl+H2O+CO2↑、NaHCO3+HCl=NaCl+H2O+CO2↑,
1mol 2mol 1mol 1mol 1mol 1mol
由反应的方程式可知,Na2CO3消耗的盐酸多,生成的二氧化碳一样多.
故选A.
点评:本题考查了碳酸氢钠、碳酸钠的化学性质,为高频考点,侧重于学生的分析能力和计算能力的考查,要求学生熟练掌握碳酸钠、碳酸氢钠的化学性质,试题基础性强,侧重对学生基础知识的巩固和训练,题目难度不大.

练习册系列答案
相关题目
某同学参阅了“84消毒液”说明中的配方,欲用NaClO固体、容量瓶自己配制480mL含NaClO 25%密度为1.19g?cm-3的消毒液.下列说法正确的是( )
| A、配制过程只需要三种仪器即可完成 |
| B、容量瓶用蒸馏水洗净后可以不烘干立即用于溶液的配制 |
| C、所配得的NaClO消毒液在空气中光照久置后溶液中NaClO物质的量浓度增大 |
| D、需要称量NaClO固体的质量为140g |
若用NA表示阿伏伽德罗常数,则相对分子质量为M的物质的一个分子的质量(以克为单位)是( )
| A、MNA | ||
B、
| ||
C、
| ||
D、
|
一定条件下,通过下列反应可实现燃煤烟气中的硫的回收:SO2(g)+2CO(g)?2CO2(g)+S(l)△H<0
一定温度下,在容积为2L的恒容密闭容器中1molSO2和nmolCO发生反应,5min后达到平衡,生成2amolCO2.下列说法正确的是( )
一定温度下,在容积为2L的恒容密闭容器中1molSO2和nmolCO发生反应,5min后达到平衡,生成2amolCO2.下列说法正确的是( )
| A、反应前2min的平均速率v(SO2)=0.1amol/(L.min) |
| B、当混合气体的物质的量不再改变时,反应达到平衡状态 |
| C、平衡后保持其它条件不变,从容器中分离出部分硫,平衡向正反应方向移动 |
| D、平衡后保持其他条件不变,升高温度和加入催化剂,SO2的转化率均增大 |

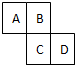 如图为元素周期表的一部分,已知A、B、C、D均为短周期元素,A与D原子序数之和是C的原子序数的1.5倍.
如图为元素周期表的一部分,已知A、B、C、D均为短周期元素,A与D原子序数之和是C的原子序数的1.5倍.


