题目内容
12.下列关于有机化合物的说法错误的是( )| A. | 液化石油气主要含乙烯、丙烯和甲烷 | |
| B. | 航空煤油中存在烷烃的同系物 | |
| C. | 相同碳原子数的醇与卤代烃比较,醇在水中溶解度更大 | |
| D. | 聚乙烯和聚甲荃丙烯酸甲酯都是通过加聚反应制得 |
分析 A、液化石油气是碳原子数在3-4的烷烃、环烷烃的混合物;
B、煤油是石油的分馏产物;
C、-OH是亲水基,而-X是憎水基;
D、聚乙烯的单体是乙烯,而聚甲醛丙烯酸甲酯的单体甲醛丙烯酸甲酯;
解答 解:A、液化石油气是通过石油分馏得到,而石油中不含烯烃,故液化石油气是烷烃、环烷烃的混合物,不含乙烯,故A错误;
B、煤油是石油的分馏产物,而石油是烷烃和环烷烃的混合物,故航空煤油中存在烷烃的同系物,故B正确;
C、-OH是亲水基,而-X是憎水基,相同碳原子数的醇与卤代烃比较,醇在水中溶解度更大,故C正确;
D、聚乙烯的单体是乙烯,故聚乙烯是乙烯通过加聚反应而得到的;而聚甲醛丙烯酸甲酯的单体是甲醛丙烯酸甲酯,故聚甲醛丙烯酸甲酯也是通过加聚反应得到的,故D正确.
故选A.
点评 本题考查了石油的综合利用以及加聚反应和有机物的水溶性等,难度不大,应注意的是石油主要是烷烃和环烷烃的混合物.

练习册系列答案
 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案
相关题目
2.下列有关叙述或化学用语表示正确的是( )
| A. | S2-的结构示意图: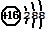 | |
| B. | 过氧化氢的电子式: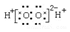 | |
| C. | Ge原子的简化电子排布式:[Ar]4s24p2 | |
| D. | 氯化钠的分子式:NaCl |
3.草酸钴可用于指示剂和催化剂的制备.用水钴矿(主要成分为Co2O3,含少量Fe2O3、A12O3、MnO、MgO、CaO、SiO2等)制取CoC2O4•2H2O工艺流程如图:

已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、Al3+等;
②酸性条件下,ClO3-不会氧化Co2+,ClO3-转化为Cl-;
③部分阳离子以氢氧化物形式沉淀时溶液的pH见表:
(1)浸出过程中加入Na2SO3的主要目的是将Co3+、Fe3+还原为Co2+、Fe2+.
(2)向浸出液中加入NaClO3的离子反应方程式:ClO3-+6Fe2++6H+=Cl-+6Fe3++3H2O.
(3)已知:常温下
NH3•H2O?NH4++OH- Kb=1.8×10-5
H2C2O4?H++HC2O4- Ka1=5.4×10-2
HC2O4-?H+C2O42- Ka2=5.4×10-5
则该流程中所用(NH4)2C2O4溶液的pH<7(填“>”或“<”或“=”).
(4)加入(NH4)2C2O4溶液后析出晶体,再过滤、洗涤,洗涤时可选用的试剂有:A.
A.蒸馏水B.自来水C.饱和的(NH4)2C2O4溶液D.稀盐酸
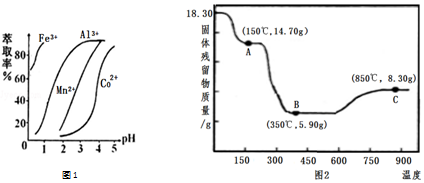
(5)萃取剂对金属离子的萃取率与pH的关系如右图1,萃取剂的作用是除去溶液中的Mn2+;其使用的适宜pH范围是B.
A.2.0~2.5B.3.0~3.5C.4.0~4.5
(6)CoC2O4•2H2O热分解质量变化过程如图2所示.其中600℃以前是隔绝空气加热,600℃以后是在空气中加热.A、B、C均为纯净物;C点所示产物的化学式是Co2O3.

已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、Al3+等;
②酸性条件下,ClO3-不会氧化Co2+,ClO3-转化为Cl-;
③部分阳离子以氢氧化物形式沉淀时溶液的pH见表:
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Co(OH)2 | Fe(OH)2 | Mn(OH)2 |
| 完全沉淀的pH | 3.7 | 5.2 | 9.2 | 9.6 | 9.8 |
(2)向浸出液中加入NaClO3的离子反应方程式:ClO3-+6Fe2++6H+=Cl-+6Fe3++3H2O.
(3)已知:常温下
NH3•H2O?NH4++OH- Kb=1.8×10-5
H2C2O4?H++HC2O4- Ka1=5.4×10-2
HC2O4-?H+C2O42- Ka2=5.4×10-5
则该流程中所用(NH4)2C2O4溶液的pH<7(填“>”或“<”或“=”).
(4)加入(NH4)2C2O4溶液后析出晶体,再过滤、洗涤,洗涤时可选用的试剂有:A.
A.蒸馏水B.自来水C.饱和的(NH4)2C2O4溶液D.稀盐酸
(5)萃取剂对金属离子的萃取率与pH的关系如右图1,萃取剂的作用是除去溶液中的Mn2+;其使用的适宜pH范围是B.
A.2.0~2.5B.3.0~3.5C.4.0~4.5
(6)CoC2O4•2H2O热分解质量变化过程如图2所示.其中600℃以前是隔绝空气加热,600℃以后是在空气中加热.A、B、C均为纯净物;C点所示产物的化学式是Co2O3.

20.进行化学实验,观察实验现象,通过分析推理得出正确的结论是化学学习的方法之一.下列说法不正确的是( )
| A. | 给试管中的铜与浓硫酸加热,发现试管底部有白色固体并夹杂有少量黑色物质,此白色固体为硫酸铜,黑色固体为氧化铜 | |
| B. | SO2通入足量的Fe(NO3)3稀溶液中,溶液有棕黄色变为浅绿色,但立即又变成棕黄色,说明氧化性:HNO3>Fe3+>稀硫酸 | |
| C. | 向偏铝酸钠溶液通入少量的二氧化碳,生成白色沉淀和碳酸钠,说明HCO3-和AlO2-不能共存 | |
| D. | 在铝制容器中加入食盐溶液,再将变量的银器浸入该溶液中,一段时间后发现黑色会褪去,是因为银器表面Ag2S和金属铝构成原电池而发生了反应 |
7.下列实验装置或方案不能达到实验目的是( )
| 编号 | A | B | C | D |
| 实验装置或 方案 | 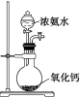 | 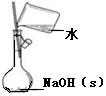 | 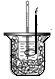 50mL0.5mol/LHCl与50mL0.55mol/LNaOH溶液 |  |
| 目的 | 制备少量氨气 | 配制0.10mol/L NaOH溶液 | 测定中和热 | 探究Ksp(AgCl)与Ksp(AgI)的大小 |
| A. | A | B. | B | C. | C | D. | D |
17.下列物质不能通过化合反应得到的是( )
| A. | FeCl2 | B. | Fe(OH)3 | C. | CuO | D. | CuS |
4.某小组设计如图装置研究电化学原理,下列说法中错误的是( )


| A. | 若开始时开关K与a连接,其反应与铁的吸氧腐蚀类似 | |
| B. | 若开始时开关K与b连接,则标准状况下B极产生2.24 L气体,转移电子0.2 mol | |
| C. | 若开始时开关K与b连接,则该装置是化学能转变为电能 | |
| D. | 若开始时开关K与b连接,其原理类似于钢铁防护中外加电流的阴极保护法 |
1.下列说法中正确的是( )
| A. | 得乙烯进入酸性KMnO4溶液和溴水,实验现象和反应类型相同 | |
| B. | 从苯的分子组成看苯远没有达到饱和,所以它应该能使溴的CCl4溶液褪色 | |
| C. | 苯环上的碳碳键是一种介于碳碳单链和碳碳双键之间的独特的键,但苯可以发生取代反应和加成反应 | |
| D. | 常温下,所有的碳原子数大于等于5的烷烃都不是气体 |
20.金属钠分别与下列物质的溶液反应时,既有气体又有沉淀产生的是( )
| A. | K2SO4 | B. | NaHCO3 | C. | BaCl2 | D. | CuSO4 |