题目内容
新型高能钠硫电池以熔融的钠、硫为电极,以导电的陶瓷为固体电解质.该电池放电时为原电池,充电时为电解池,反应原理为:2Na+xS
Na2Sx.
(1)放电时Na发生 反应(填:氧化或还原),S作 极
(2)充电时Na所在电极与直流电源的 极相连.
(3)放电时负极反应为 ;
(4)用此电池作电源电解饱和NaCl溶液,当阳极产生33.6L(标准状况)气体时,消耗金属Na的质量为 .
| 放电 |
| 充电 |
(1)放电时Na发生
(2)充电时Na所在电极与直流电源的
(3)放电时负极反应为
(4)用此电池作电源电解饱和NaCl溶液,当阳极产生33.6L(标准状况)气体时,消耗金属Na的质量为
考点:原电池和电解池的工作原理
专题:电化学专题
分析:在放电时,原电池正极发生得电子的还原反应,在反应2Na+xS=Na2Sx中,硫单质得电子,故正极反应为:xS+2e-=Sx2-;原电池负极发生失电子的氧化反应,在反应2Na+xS=Na2Sx中钠失电子,故负极反应为2Na-2e-=2Na+,在充电时,电解池的阳极发生的电极反应极为正极上的逆反应,阴极反应和负极互为逆反应,根据电极反应以及电子守恒进行计算即可.
解答:
解:(1)在反应2Na+xS=Na2Sx中钠失电子,故放电时Na发生氧化反应:2Na-2e-=2Na+,硫单质得电子,作正极,故答案为:氧化;正;
(2)充电时Na所在电极为电池的负极应该与直流电源的负极相连,故答案为:负;
(3)原电池负极发生失电子的氧化反应,在反应2Na+xS=Na2Sx中钠失电子,故负极反应为Na-e-=Na+,故答案为:Na-e-=Na+;
(4)电源电解饱和NaCl溶液,当阳极产生33.6L即1.5mol(标准状况)气体时,根据电极反应:2Cl--2e-=Cl2↑,转移电子是3mol,根据电极反应:Na-e-=Na+,所以耗金属钠的质量是3mol×23g/mol=69g,故答案为:69g.
(2)充电时Na所在电极为电池的负极应该与直流电源的负极相连,故答案为:负;
(3)原电池负极发生失电子的氧化反应,在反应2Na+xS=Na2Sx中钠失电子,故负极反应为Na-e-=Na+,故答案为:Na-e-=Na+;
(4)电源电解饱和NaCl溶液,当阳极产生33.6L即1.5mol(标准状况)气体时,根据电极反应:2Cl--2e-=Cl2↑,转移电子是3mol,根据电极反应:Na-e-=Na+,所以耗金属钠的质量是3mol×23g/mol=69g,故答案为:69g.
点评:本题考查学生原电池、电解池的工作原理等知识,注意电子守恒的应用是关键,难度中等.

练习册系列答案
 口算题天天练系列答案
口算题天天练系列答案
相关题目
下列说法正确的是( )
A、按系统命名法, 的名称为2,7,7-三甲基-3-乙基辛烷 的名称为2,7,7-三甲基-3-乙基辛烷 |
B、有机物 中,所有原子可能在同一平面上 中,所有原子可能在同一平面上 |
C、 与足量的NaOH溶液发生反应时,所得有机产物的化学式为C9H6O6Na4 与足量的NaOH溶液发生反应时,所得有机产物的化学式为C9H6O6Na4 |
| D、若两种二肽互为同分异构体,则二者的水解产物一定不相同 |
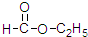
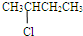
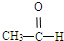
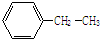

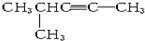
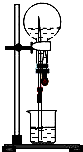 以下是针对喷泉实验所得溶液浓度问题的探讨,请根据题意回答问题.
以下是针对喷泉实验所得溶液浓度问题的探讨,请根据题意回答问题.