题目内容
氨水中存在电离平衡NH3?H2O?NH4++OH-,下列叙述不正确的是( )
分析:A.根据电荷守恒判断;
B.一水合氨是弱电解质,加水促进一水合氨电离,氢氧根离子浓度减小,氢离子浓度增大;
C.向氨水中加入含有铵根离子的物质抑制一水合氨电离;
D.向氨水中加入和氢氧根离子反应的物质促进一水合氨电离.
B.一水合氨是弱电解质,加水促进一水合氨电离,氢氧根离子浓度减小,氢离子浓度增大;
C.向氨水中加入含有铵根离子的物质抑制一水合氨电离;
D.向氨水中加入和氢氧根离子反应的物质促进一水合氨电离.
解答:解:A.任何溶液中都存在电荷守恒,根据电荷守恒得c(OH-)=c(H+)+c(NH4+),故A正确;
B.加水稀释氨水,促进一水合氨电离,但氢离子增大的物质的量小于溶液体积增大的量,所以氢氧根离子浓度减小,温度不变,水的离子积常数不变,则氢离子浓度增大,故B错误;
C.向氨水中加入含有铵根离子的物质抑制一水合氨电离,所以向氨水中加入氯化铵抑制一水合氨电离,平衡逆向移动,故C正确;
D.向氨水中加入和氢氧根离子反应的物质促进一水合氨电离,向氨水中加入盐酸,氢离子和氢氧根离子反应生成水,促进一水合氨电离,平衡正向移动,故D正确;
故选B.
B.加水稀释氨水,促进一水合氨电离,但氢离子增大的物质的量小于溶液体积增大的量,所以氢氧根离子浓度减小,温度不变,水的离子积常数不变,则氢离子浓度增大,故B错误;
C.向氨水中加入含有铵根离子的物质抑制一水合氨电离,所以向氨水中加入氯化铵抑制一水合氨电离,平衡逆向移动,故C正确;
D.向氨水中加入和氢氧根离子反应的物质促进一水合氨电离,向氨水中加入盐酸,氢离子和氢氧根离子反应生成水,促进一水合氨电离,平衡正向移动,故D正确;
故选B.
点评:本题考查了弱电解质的电离,明确弱电解质电离特点是解本题关键,注意水的离子积常数只与温度有关,与溶液的酸碱性无关.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
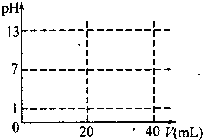 (2012?成都模拟)溶液中的化学反应大多是离子反应.根据要求回答下列问题.
(2012?成都模拟)溶液中的化学反应大多是离子反应.根据要求回答下列问题. c(Na+)= c(HCO3—)+
c(CO32—)+ c(H2CO3)
c(Na+)= c(HCO3—)+
c(CO32—)+ c(H2CO3) H++OH—。所以不论是酸还是碱均是抑制水的电离,②和④中氢离子和OH—的的浓度均相同,抑制水的电离程度是相同的,所以由水电离出来的c(H+)是相同的。
H++OH—。所以不论是酸还是碱均是抑制水的电离,②和④中氢离子和OH—的的浓度均相同,抑制水的电离程度是相同的,所以由水电离出来的c(H+)是相同的。