题目内容
17.在甲、乙两烧杯中,分别含有下列离子Cu2+、K+、H+、Cl-、CO32-、OH-中的三种离子.已知甲烧杯的溶液呈蓝色,则乙烧杯的溶液中大量存在的离子是( )| A. | Cu2+、H+、Cl- | B. | CO32-、OH-、Cl- | C. | K+、H+、Cl- | D. | K+、CO32-、OH- |
分析 甲溶液呈蓝色,应含有Cu2+,则与Cu2+反应的离子应存在于乙中,结合溶液的电中性原则及离子共存的条件进行解答.
解答 解:甲溶液呈蓝色,应含有Cu2+,因CO32-、OH-可与反应生成沉淀,则只能存在于乙中,乙中含有CO32-、OH-,则一定不存在H+,阳离子只能为K+,
则乙中含有的离子为:CO32-、OH-、K+,甲中含有的离子为:Cu2+、H+、Cl-,
故选D.
点评 本题考查离子共存问题,为高考常见题型,题目难度中等,侧重于学生的分析能力和元素化合物知识的综合运用的考查,注意把握离子之间发生复分解反应的特点.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
7.标准状况下,11.2升二氧化碳气体的质量是( )
| A. | 11克 | B. | 22克 | C. | 44克 | D. | 5.6克 |
5.分类法是一种行之有效、简单易行的科学方法.某同学用下表所示形式对所学知识进行分类,其中甲与乙关系正确的是( )
| 选项 | 甲 | 乙 |
| A | 电解质 | BaSO4、NaHSO4、SO3 |
| B | 弱电解质的电离 | 均分步电离 |
| C | 化学平衡影响因素 | 温度、压强、浓度、催化剂等 |
| D | 化学电源 | 一次电池、二次电池、燃料电池等 |
| A. | A | B. | B | C. | C | D. | D |
12.下列用来表示物质变化的化学用语中,正确的是( )
| A. | 用惰性电极电解饱和食盐水时,阳极的电极反应式为2Cl--2e-=Cl2↑ | |
| B. | 二氧化碳通入碳酸钠溶液中CO2+CO32-+H+=2HCO3- | |
| C. | 粗铜精炼时,与电源正极相连的是纯铜,阳极反应式为Cu-2e-=Cu2+ | |
| D. | 钢铁发生电化学腐蚀的正极反应式:Fe-2e-=Fe2+ |
9.下列有关物质性质、结构的表述均正确,且存在因果关系的是( )
| 表述1 | 表述2 | |
| A | 钠的金属性比铝强 | 钠原子核外电子数比铝少 |
| B | 金刚石的熔点高于晶体硅 | 原子半径Si大于C,键能Si-Si小于C-C |
| C | 离子晶体一般硬度较大,难压缩 | 离子晶体中阴、阳离子排列很有规律 |
| D | 相同条件下,分别完全燃烧等量的正丁烷和异丁烷,放出的热量相同 | 正丁烷与异丁烷互为同分异构体 |
| A. | A | B. | B | C. | C | D. | D |
3.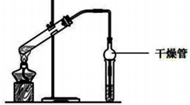 (1)乙酸乙酯是重要的有机合成中间体,广泛应用于化学工业实验室用如图的装置制备乙酸乙酯.
(1)乙酸乙酯是重要的有机合成中间体,广泛应用于化学工业实验室用如图的装置制备乙酸乙酯.
①与教材采用的实验装置不同,此装置中采用了球形干燥管,其作用是防止发生倒吸.
②己知表格数据:
③根据表数据分析,为什么乙醇需要过量一些,其原因是乙醇的沸点低,易挥发而损耗.
(2)按正确操作重新实验,该学生很快在小试管中收集到了乙_酸乙酯、乙酸、乙醇的混合物.现拟分离含乙酸、乙醇和水的乙酸乙酯粗产品,图是分离操作步骤流程图.在图中圆括号表示加入适当的试剂,编号表示适当的分离方法.
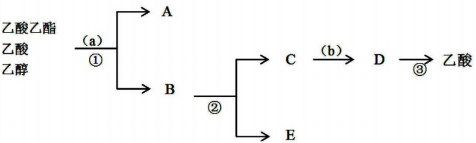
①写出加入的试剂名称:试剂(a)是饱和碳酸钠溶液;试剂(b)是稀硫酸溶液.
②写出有关的操作分离方法:①是分液,②是蒸馏,③是蒸馏.
 (1)乙酸乙酯是重要的有机合成中间体,广泛应用于化学工业实验室用如图的装置制备乙酸乙酯.
(1)乙酸乙酯是重要的有机合成中间体,广泛应用于化学工业实验室用如图的装置制备乙酸乙酯.①与教材采用的实验装置不同,此装置中采用了球形干燥管,其作用是防止发生倒吸.
②己知表格数据:
| 物质 | 熔点/℃ | 沸点/℃ | 密度/(g/cm3) |
| 乙醇 | -144 | 78 | 0.789 |
| 乙酸 | 16.6 | 117.9 | 1.05 |
| 乙酸乙酯 | -83.6 | 77.5 | 0.90 |
| 浓硫酸 | -- | 338 | 1.84 |
(2)按正确操作重新实验,该学生很快在小试管中收集到了乙_酸乙酯、乙酸、乙醇的混合物.现拟分离含乙酸、乙醇和水的乙酸乙酯粗产品,图是分离操作步骤流程图.在图中圆括号表示加入适当的试剂,编号表示适当的分离方法.

①写出加入的试剂名称:试剂(a)是饱和碳酸钠溶液;试剂(b)是稀硫酸溶液.
②写出有关的操作分离方法:①是分液,②是蒸馏,③是蒸馏.
4.中和滴定时,用于量取待测液体积的仪器是( )
| A. | 胶头滴管 | B. | 量筒 | C. | 滴定管 | D. | 移液管 |