题目内容
常温下,将等浓度的FeSO4和(NH4)2SO4两种浓溶液混合可制得一种晶体,该晶体是分析化学中常用的一种还原剂,称作摩尔盐,其强热分解反应化学方程式为:2(NH4)2Fe(SO4)2?6H2O
Fe2O3+2NH3↑+N2↑+
4SO2↑+17H2O.下列说法正确的是( )
| ||
4SO2↑+17H2O.下列说法正确的是( )
| A、该反应中氧化产物是N2、NH3,还原产物是SO2、Fe2O3 |
| B、1mol摩尔盐强热分解时转移电子的物质的量为4NA |
| C、向摩尔盐溶液中滴入足量浓NaOH溶液,最终得到刺激性气味的气体和白色沉淀 |
| D、常温下,摩尔盐的溶解度比FeSO4、(NH4)2SO4大 |
考点:氧化还原反应
专题:氧化还原反应专题
分析:2(NH4)2Fe(SO4)2?6H2O
Fe2O3+2NH3↑+N2↑+4SO2↑+17H2O中,Fe、N元素的化合价升高,S元素的化合价降低,以此来解答.
| ||
解答:
解:A.Fe、N元素的化合价升高,S元素的化合价降低,则该反应中氧化产物是N2、Fe2O3,还原产物是SO2,故A错误;
B.由S元素的化合价变化可知,1mol摩尔盐强热分解时转移电子的物质的量为1mol×2×(6-4)=4mol,故B正确;
C.向摩尔盐溶液中滴入足量浓NaOH溶液,因氢氧化亚铁易被氧化成氢氧化铁,最终可得刺激性气体和红褐色沉淀,故C错误;
D.常温下,将等浓度的FeSO4和(NH4)2SO4两种浓溶液混合可制得一种晶体,可知常温下,摩尔盐的溶解度比FeSO4、(NH4)2SO4小,故D错误;
故选B.
B.由S元素的化合价变化可知,1mol摩尔盐强热分解时转移电子的物质的量为1mol×2×(6-4)=4mol,故B正确;
C.向摩尔盐溶液中滴入足量浓NaOH溶液,因氢氧化亚铁易被氧化成氢氧化铁,最终可得刺激性气体和红褐色沉淀,故C错误;
D.常温下,将等浓度的FeSO4和(NH4)2SO4两种浓溶液混合可制得一种晶体,可知常温下,摩尔盐的溶解度比FeSO4、(NH4)2SO4小,故D错误;
故选B.
点评:本题考查氧化还原反应,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应基本概念的考查,注意从化合价角度和习题信息角度分析,题目难度不大.

练习册系列答案
 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案
相关题目
某烃的结构简式为CH3-CH2-CH=C(C2H5)-C≡CH分子中含有四面体结构的碳原子(即饱和碳原子)数为a,在同一直线上的碳原子数量最多为b,一定在同一平面内的碳原子数为c,则a、b、c分别为( )
| A、4、3、5 |
| B、4、3、6 |
| C、2、5、4 |
| D、4、6、4 |
下列说法正确的是( )
| A、等量的硫蒸气和硫固体分别完全燃烧,后者放出热量多 |
| B、由C(石墨)→C(金刚石)△H=+119 kJ?mol-1可知,石墨比金刚石稳定 |
| C、生成物中全部化学键形成时所释放的能量大于破坏反应物中全部化学键所吸收的能量时,反应为吸热反应 |
| D、在101 kPa时,2g H2完全燃烧生成液态水,放出285.8 kJ热量,则表示氢气燃烧热的热化学方程式为2H2(g)+O2(g)=2H2O(l)△H=-285.8 kJ?mol-1 |
3S+6KOH═2K2S+K2SO3+3H2O中,被氧化与被还原的S原子数之比为( )
| A、1:2 | B、2:1 |
| C、1:1 | D、3:2 |
PH3在常温下是无色有大蒜气味的气体,它的分子呈三角锥形,以下关于PH3的叙述中正确的是( )
| A、PH3是非极性分子 |
| B、PH3中有孤电子对 |
| C、PH3是一种强氧化剂 |
| D、PH3分子中P-H键是非极性键 |
下列判断正确的是( )
| A、离子键被破坏的变化一定是化学变化 |
| B、含有金属阳离子的晶体中一定有阴离子 |
| C、分子晶体中分子间作用力越大,分子越稳定 |
| D、NaCl熔化时离子键被破坏,冰熔化时分子中共价键没有断裂 |
用锌和1mol/L稀硫酸溶液制取氢气,欲提高制取氢气的速率,下列措施不可行的是( )
| A、改用98%的浓硫酸 |
| B、使用更小颗粒的锌粒 |
| C、滴入少量CuSO4溶液 |
| D、加热 |
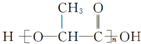 ,有关W的信息如下,其中B能使溴水褪色,C是一个六元状化合物,据此回答下列问题.
,有关W的信息如下,其中B能使溴水褪色,C是一个六元状化合物,据此回答下列问题.